篇一 :高中化学必修一知识点总结
高中化学必修一全册基本内容梳理
第一章、从实验学化学
一、化学实验安全
1、(1)做有毒气体的实验时,应在通风厨中进行,并注意对尾气进行适当处理(吸收或点燃等)。进行易燃易爆气体的实验时应注意验纯,尾气应燃烧掉或作适当处理。
(2)烫伤宜找医生处理。
(3)浓酸撒在实验台上,先用Na2CO3 (或NaHCO3)中和,后用水冲擦干净。浓酸沾在皮肤上,宜先用干抹布拭去,再用水冲净。浓酸溅在眼中应先用稀NaHCO3溶液淋洗,然后请医生处理。
(4)浓碱撒在实验台上,先用稀醋酸中和,然后用水冲擦干净。浓碱沾在皮肤上,宜先用大量水冲洗,再涂上硼酸溶液。浓碱溅在眼中,用水洗净后再用硼酸溶液淋洗。
(5)钠、磷等失火宜用沙土扑盖。
(6)酒精及其他易燃有机物小面积失火,应迅速用湿抹布扑盖。
二.混合物的分离和提纯
分离和提纯的方法
过滤 用于固液混合的分离 一贴、二低、三靠 如粗盐的提纯
蒸馏 提纯或分离沸点不同的液体混合物 防止液体暴沸,温度计水银球的位置,如石油的蒸馏中冷凝管中水的流向 如石油的蒸馏
萃取 利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法 选择的萃取剂应符合下列要求:和原溶液中的溶剂互不相溶;对溶质的溶解度要远大于原溶剂 用四氯化碳萃取溴水里的溴、碘
…… …… 余下全文
篇二 :高中化学选修一知识点总结
《选修1·化学与生活》
第一章 关注营养平衡第一节 生命的基础能源—糖类
1、糖类是绿色植物光合作用的产物。由C、H、O三种元素组成的一类有机化合物,也叫碳水化合物(通式为Cn(H20)m),但其实此名称并不能真实反应糖类的组成和特征,如鼠李糖C6H12O5是糖却不符合此通式,而符合此通式的,如甲醛HCHO、乙酸CH3COOH却不是糖类。
2、葡萄糖分子式C6H12O6,是一种白色晶体,有甜味,能溶于水
3、葡萄糖的还原性:
和银氨溶液反应: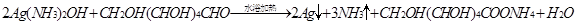 ;
;
和新制Cu(OH)2反应: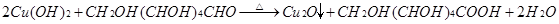 。
。
4、葡萄糖为人体提供能源
①葡萄糖提供能量的方程式: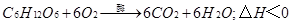 ;
;
②粮食中的糖类在人体中转化成葡萄糖而被吸收,在体内有三条途径,即:a、直接氧化供能;b、转化成糖元被肝脏和肌肉储存,当血液中的葡萄糖即血糖的质量分数比正常值低时,糖元就释放出来维持血糖浓度的相对稳定;c、转变为脂肪,储存在脂肪组织里。
5、蔗糖和麦芽糖是二糖,它们水解的化学方程式分别是: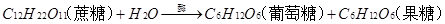
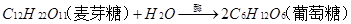
6、淀粉是一种重要的多糖,分子式(C6H10O5)n,是一种相对分子质量很大的天然高分子有机化合物,没有甜味,是一种白色粉末,不溶于冷水,但在热水中一部分淀粉溶解在水中,一部分悬浮在水里,长时间或高温可产生糊化。它能水解。淀粉在人体内的水解过程可表示为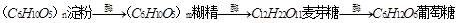 ,也可在酸的催化下逐步水解,其方程式
,也可在酸的催化下逐步水解,其方程式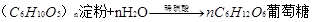 。 淀粉的特性:I2能使淀粉溶液变成蓝色。这是实验室检验淀粉或I2存在的重要原理。
。 淀粉的特性:I2能使淀粉溶液变成蓝色。这是实验室检验淀粉或I2存在的重要原理。
…… …… 余下全文
篇三 :高中化学必修一知识点总结
高中化学必修1复习提纲
( 注:A----了解 B----理解 C---综合应用)

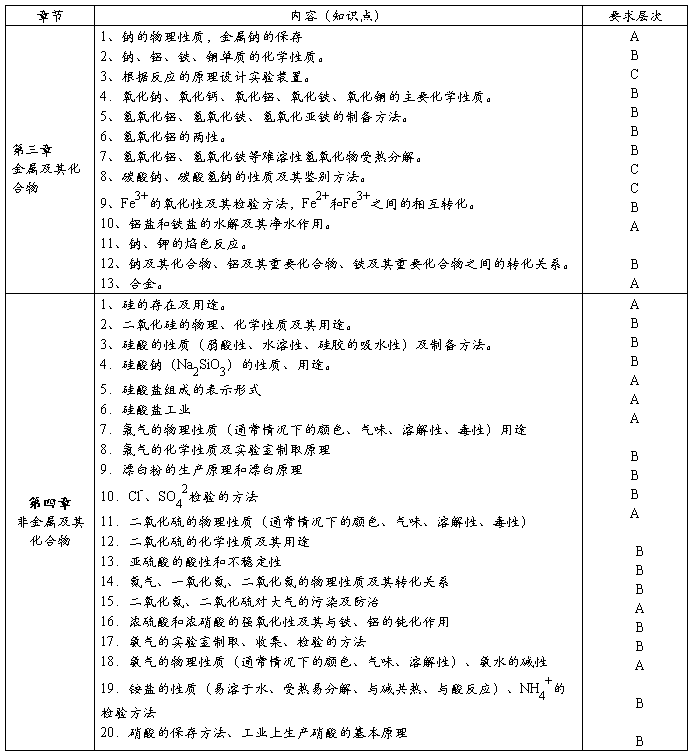
必修1全册基本内容梳理
一、从实验学化学
(一) 化学实验安全
1、(1)做有毒气体的实验时,应在通风厨中进行,并注意对尾气进行适当处理(吸收或点燃等)。进行易燃易爆气体的实验时应注意验纯,尾气应燃烧掉或作适当处理。
(2)烫伤宜找医生处理。
(3)浓酸撒在实验台上,先用Na2CO3 (或NaHCO3)中和,后用水冲擦干净。浓酸沾在皮肤上,宜先用干抹布拭去,再用水冲净。浓酸溅在眼中应先用稀NaHCO3溶液淋洗,然后请医生处理。
(4)浓碱撒在实验台上,先用稀醋酸中和,然后用水冲擦干净。浓碱沾在皮肤上,宜先用大量水冲洗,再涂上硼酸溶液。浓碱溅在眼中,用水洗净后再用硼酸溶液淋洗。
(5)钠、磷等失火宜用沙土扑盖。
(6)酒精及其他易燃有机物小面积失火,应迅速用湿抹布扑盖。
(二) 混合物的分离和提纯
分离和提纯的方法 分离的物质 应注意的事项 应用举例
…… …… 余下全文
篇四 :高中化学知识点总结离子反应
四、离子反应
1、电解质的概念
1.1 电解质与非电解质(辨析并举例)
电解质:在水溶液里或熔融状态下能够导电的化合物。包括酸、碱、盐活泼金属的氧化物某些非金属氢化物,某些有机物。
举例NaCl固体不导电,溶于水后可以导电,所以是电解质。CaSO4、BaSO4等难溶物质在水中溶解度很小,在熔融状态下可以导电,所以这些物质也是电解质。
非电解质:在水溶液里和熔融状态下不能够导电的化合物。包括大多数有机物非金属氧化物某些非金属氢化物等。
举例:CO2、SO3、NH3、蔗糖、酒精
注:我们讨论的电解质和非电解质都是化合物,单质或混合物既不是电解质也不是非电解质。
1.2 强电解质与弱电解质(辨析并举例)
强电解质: 在水溶液里或熔融状态下全部电离成离子的电解质。包括大多数盐类、强酸、强碱。在溶液中的粒子主要是离子。
弱电解质:在水溶液里部分电离成离子的电解质包括弱酸(如HAc、H2S)、中强酸(H3PO4)弱碱(如NH3·H2O)、水。
例题:CH3COOH极易溶于水,为什么它是弱电解质, Ca(OH)2微溶于水,为什么它是强电解质?
…… …… 余下全文
篇五 :高中化学会考知识点总结
20##年化学学业水平测试知识点总结
1、化合价(常见元素的化合价):
碱金属元素、Ag、H:+1 F:—1
Ca、Mg、Ba、Zn:+2 Cl:—1,+1,+5,+7
Cu:+1,+2 O:—2
Fe:+2,+3 S:—2,+4,+6
Al:+3 P:—3,+3,+5
Mn:+2,+4,+6,+7 N:—3,+2,+4,+5
3、金属活动性顺序表
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
还 原 性 逐 渐 减 弱
…… …… 余下全文
篇六 :高中化学选修4知识点总结
高中化学选修4知识点总结
第1章、化学反应与能量转化
化学反应的实质是反应物化学键的断裂和生成物化学键的形成,化学反应过程中伴随着能量的释放或吸收。
一、化学反应的热效应
1、化学反应的反应热
(1)反应热的概念:
当化学反应在一定的温度下进行时,反应所释放或吸收的热量称为该反应在此温度下的热效应,简称反应热。用符号Q表示。
(2)反应热与吸热反应、放热反应的关系。
Q>0时,反应为吸热反应;Q<0时,反应为放热反应。
(3)反应热的测定
测定反应热的仪器为量热计,可测出反应前后溶液温度的变化,根据体系的热容可计算出反应热,计算公式如下:
Q=-C(T2-T1)
式中C表示体系的热容,T1、T2分别表示反应前和反应后体系的温度。实验室经常测定中
和反应的反应热。
2、化学反应的焓变
(1)反应焓变
物质所具有的能量是物质固有的性质,可以用称为“焓”的物理量来描述,符号为H,单位为kJ·mol-1。
反应产物的总焓与反应物的总焓之差称为反应焓变,用ΔH表示。
(2)反应焓变ΔH与反应热Q的关系。
对于等压条件下进行的化学反应,若反应中物质的能量变化全部转化为热能,则该反应的反应热等于反应焓变,其数学表达式为:Qp=ΔH=H(反应产物)-H(反应物)。
…… …… 余下全文
篇七 :高一化学全册知识点总结
必修1全册化学基本内容梳理
从实验学化学
一、化学实验安全
1、(1)做有毒气体的实验时,应在通风厨中进行,并注意对尾气进行适当处理(吸收或点燃等)。进行易燃易爆气体的实验时应注意验纯,尾气应燃烧掉或作适当处理。
(2)烫伤宜找医生处理。
(3)浓酸撒在实验台上,先用Na2CO3 (或NaHCO3)中和,后用水冲擦干净。浓酸沾在皮肤上,宜先用干抹布拭去,再用水冲净。浓酸溅在眼中应先用稀NaHCO3溶液淋洗,然后请医生处理。
(4)浓碱撒在实验台上,先用稀醋酸中和,然后用水冲擦干净。浓碱沾在皮肤上,宜先用大量水冲洗,再涂上硼酸溶液。浓碱溅在眼中,用水洗净后再用硼酸溶液淋洗。
(5)钠、磷等失火宜用沙土扑盖。
(6)酒精及其他易燃有机物小面积失火,应迅速用湿抹布扑盖。
二.混合物的分离和提纯
分离和提纯的方法 分离的物质 应注意的事项 应用举例
过滤 用于固液混合的分离 一贴、二低、三靠 如粗盐的提纯
蒸馏 提纯或分离沸点不同的液体混合物 防止液体暴沸,温度计水银球的位置,如石油的蒸馏中冷凝管中水的流向 如石油的蒸馏
萃取 利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法 选择的萃取剂应符合下列要求:和原溶液中的溶剂互不相溶;对溶质的溶解度要远大于原溶剂 用四氯化碳萃取溴水里的溴、碘
…… …… 余下全文
篇八 :高中化学必修2知识点归纳总结律
高中化学必修2知识点归纳总结
第一章 物质结构 元素周期律
一、原子结构
 质子(Z个)
质子(Z个)
 原子核 注意:
原子核 注意:
中子(N个) 质量数(A)=质子数(Z)+中子数(N)
 1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
核外电子(Z个)
★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
…… …… 余下全文