篇一 :分析化学总结
分析化学知识点总结
第二章:光学分析法
1
2、量子吸收由高能级到低能级是发射,由低能级到高能级是吸收。
3、原子吸收光谱法:是基于基态原子外层电子对其共振发射的吸收的定量分析方法,其定量基础是朗伯-比尔定律。
核心技术:原子化技术、锐线光源技术。
4、原子发射光谱法:是基于受激原子或离子外层电子发射特征光学光谱而回到叫低能级的定量和定性分析方法。
核心技术:原子化及原子激发技术。
5、原子吸收光谱法:气态自由原子吸收特征波长的辐射后,原子外层电子从基态或低能态跃迁到高能态,又跃迁到基态或低能态,同时发射出与原子激发波长相同或不同的辐射。
6测系统、信号处理或读出系统。
7硅碳棒)。
8、线光源(空心阴极灯)
9、光栅的分辨率:R=Nn(N刻线数、n级次)
10、光栅和棱镜的分光原理及区别:本质都是利用不同波长的光在发生反射折射衍射等时的不同表现分光。 光栅是利用衍射与干涉的总体效果,棱镜是利用折射。
一般说来,光栅光谱更精细,分辨率更高。
第三章:原子发射光谱法
1、共振线:原子中外层电子从基态被激发到激发态后,由该基态跃迁回基态所发射出来的辐射线。
…… …… 余下全文
篇二 :分析化学总结
第一章
分析方法的分类 (化学分析、仪器分析;定性、定量分析;常量、半微量、微量分析)
第二章 要点
1、灵敏度的表达方式及其换算关系
2、空白试验和对照实验的含义及其应用
3、阳离子分析特性及其分离方案
有色离子
各组所包含的离子及其分析特性
组试剂及分离条件控制
沉淀颜色
常用分离反应及鉴定反应
特殊反应
4、阴离子分析方案
5、试验结果的合理性判断
第三章 要点
1、误差的分类、特点、产生的原因及其消除方法 (系统误差、随机误差)
2、误差的表示方法(相对误差、标准偏差,平均值的标准偏差)
3、精确度与准确度的关系
4、有效数字的处理规则
5、随机误差的正态分布
6、随机误差出现的区间概率
7、置信区间的含义及其计算
8、可疑值的取舍(G检验,Q检验)
9、显著性检验 (t检验)
第四章要点
1、滴定反应的要求及几种滴定方式
2、基准物质的要求
3、标准溶液的配置:直接法,间接法
第五章 要点
1、酸碱质子理论
2、共扼酸碱对平衡常数之间的关系
3、酸碱各型体的分布分数
4、溶液中氢离子浓度的计算(弱酸碱、两性物质)
…… …… 余下全文
篇三 :高职环保03定量分析化学总结
高职环保03分析化学综合实验总结
本次分析化学综合实验严格按照教研室的安排,实习前制定了详细的计划,并召开了动员大会,会上布置并强调了计划中安排的各项任务,在实验室中顺利并圆满的完成了一周的综合实验。
为了能确保本次综合实验的圆满完成,作为指导教师,实习前对实验内容作了精心安排,内容安排上坚决贯彻以全面素质为基础、以能力培养为本位的教学思想,坚持理论与实践相结合,培养学生的专业技能和实践能力,内容选题侧重和生产实践紧密联系的题目,难度适中,并按我院实际的实验条件进行了调整。实习中,坚持每日检查学生的实习情况,对没有预习的学生坚决不允许进入实验室,对操作不规范的学生坚决予以纠正;严格纪律,认真考勤,并对实验中存在的问题及时给予解决;督促学生按时完成实验报告,并对实验报告做了及时的批改。
通过本次综合实验,基本上达到了预期目的,规范了学生分析化学实验的基本操作技能,掌握了常用分析方法的操作;培养了学生的实验动手能力;养成了良好的实验习惯;提高了学生的专业技能,使学生的基础理论更加扎实,提高了学生独立分析问题、解决问题的能力。
指导教师:李纯毅 从晓英
20xx.6.20
高职工艺03生产实习总结
…… …… 余下全文
篇四 :分析化学总结题
3. 根据置信度为95%对某项分析结果计算后,写出的合理分析结果表达式应为( b )
a.(25.48±0.1)% b.(25.48±0.13)% c.(25.48±0.135)% d.(25.48±0.1348)%
4. 测定NaCl+Na3PO4中 Cl含量时,选用( c )标准溶液作滴定剂。
a.NaCl b.AgNO3 c.NH4SCN d.Na2SO4
6.已知在 1mol/L H2SO4溶液中,MnO4-/Mn2+和 Fe3+/Fe2+电对的条件电极电位分别为 1.45V和0.68V。在此条件下用KMnO4标准溶液滴定 Fe2+,其化学计量点的电位值为( c )。
a. 0.73V b. 0.89V c. 1.32V d. 1.49V
8. 下列阴离子的水溶液,若浓度相同,则( b )碱度最强。 a. CN-(KCN= 6.2×10-10)
b. S2-(KHS- = 7.1×10-15, KH2S=1.3×10-7)
…… …… 余下全文
篇五 :分析化学总结
第一章
系统误差的性质:由固定原因造成的,有单向性特征,通过数理统计的方法不能除去。
系统误差的来源:仪器、试剂、实验方法、实验操作
系统误差的解决办法:针对仪器的要校准仪器;针对试剂的要做空白试验,因实验方法而带来系统误差的要改进实验方法或重新选定实验方法。
随机误差具有偶然性,随机性,也是必然存在的,随机误差只能通过多次平行实验来减小随机误差
在没有系统误差的情况下,无限次平行测定结果的平均值等于真值。
在没有系统误差的情况下,无限次平行测定结果的随机误差遵循正态分布规律,有限次的采用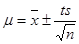 来处理。
来处理。
为了检验两组数据之间的精密度是否有显著性差异,用F检验
为了检验平均值和真值或标准值之间是否显著性差异,用t检验。
为了考察两组数据之间显著性差异,先用F检验,后用t检验。F检验不合格就不用t检验,只有F检验合格了才可以进行t检验。
处理数据要注意四舍六入五成双
计算平均值时要注意可疑值的取舍,取舍有两种方法,Q值检验法和4d法。会计算标准偏差以及置信区间。
第二章 酸碱滴定法
…… …… 余下全文
篇六 :分析化学(第六版)总结
分析化学(第六版)总结
第二章 误差和分析数据处理
第一节 误差
定量分析中的误差就其来源和性质的不同,可分为系统误差、偶然误差和过失误差。
一、系统误差
定义:由于某种确定的原因引起的误差,也称可测误差
特点:①重现性,②单向性,③可测性(大小成比例或基本恒定)
分类:
1. 方法误差: 由于不适当的实验设计或所选方法不恰当所引起。
2. 仪器误差: 由于仪器未经校准或有缺陷所引起。
3. 试剂误差: 试剂变质失效或杂质超标等不合格 所引起
4. 操作误差: 分析者的习惯性操作与正确操作有一定差异所引起。
操作误差与操作过失引起的误差是不同的。
二、偶然误差
定义:由一些不确定的偶然原因所引起的误差,也叫随机误差. 偶然误差的出现服从统计规律,呈正态分布。
特点:
①随机性(单次)
②大小相等的正负误差出现的机会相等。
③小误差出现的机会多,大误差出现的机会少。
三、过失误差
1、过失误差:由于操作人员粗心大意、过度疲劳、精神不集中等引起的。其表现是出现离群值或异常值。
…… …… 余下全文
篇七 :分析化学笔记总结
第一章.定量分析化学概论
§1.1 概述
一.定量分析过程
任务:测定物质中某种或某些组分的含量。
步骤:①取样(选择具有代表性的试样)。
②试样分解和分析试液的制备。
③分离及测定。
④分析结果的计算及评价。
二.分析试样的制备及分解
1.分析试样的采集与制备:
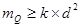
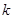 :缩分常数的经验值,试样均匀度越差,
:缩分常数的经验值,试样均匀度越差,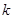 越大,通常
越大,通常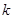 为
为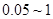
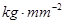 。
。
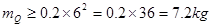
2.试样的分解:
①溶解法:溶剂为水、酸、碱、混合酸等
②熔融法:
三.定量分析结果的表示
1.待测组分的化学表示形式
2.待测组分含量的表示方法
①固体试样:

 (
(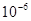 );
);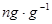 (
(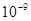 );
); (
( )
)
②液体试样:
a.物质的量浓度: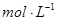
b.质量摩尔浓度:待测组分的物质的量除以溶剂的质量,单位: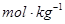
c.质量分数:量纲为1
d.体积分数:
e摩尔分数:
f.质量浓度:单位体积中某种物质的质量, 、
、
③气体试样:
体积分数表示。
§1.2 分析化学中的误差
…… …… 余下全文
篇八 :分析化学(第六版)总结
分析化学(第六版)总结
第一章 绪论
第一节 分析化学及其任务和作用
定义:研究物质的组成、含量、结构和形态等化学信息的分析方法及理 论的科学,是化学学科的一个重要分支,是一门实验性、应用性很强的学科
第二节 分析方法的分类
一、按任务分类
定性分析:鉴定物质化学组成(化合物、元素、离子、基团)
定量分析:测定各组分相对含量或纯度
结构分析:确定物质化学结构(价态、晶态、平面与立体结构)
二、按对象分类:无机分析,有机分析
三、按测定原理分类
(一)化学分析
定义:以化学反应为为基础的分析方法,称为化学分析 法.
 分类: 定性分析
分类: 定性分析
 重量分析:用称量方法求得生成物W重量
重量分析:用称量方法求得生成物W重量
定量分析
…… …… 余下全文