篇一 :物理化学第五版上册公式归纳和知识点整理
定义式:
H=U+pv=U+nRT
G=H-TS=A+pv
A=U-TS
基本公式:
dU=TdS-pdv
dH=TdS+vdp
dA=-SdT-pdv
dG=-SdT+vdp
Maxwell关系式:
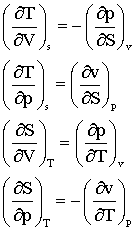
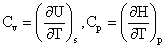 特征函数:
特征函数:
U(S,v);H(S,p);A(T,v);G(T,p);S(U,v)
等温可逆过程:
△U=0,△H=0
W=-nRT ln
Q=-W
△A=△G=W
绝热可逆过程:
Q=0,
γ=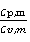 ,Cp,m+Cv,m=nR
,Cp,m+Cv,m=nR
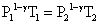
△H=nCp,m(T2-T1)
△U=nC,m(T2-T1)
W=△U
△S=0
△A=△U-S△T
△G=△H-S△T
等外压膨胀:
W=-p△V
△H=nCp,m(T2-T1)
△U=nC,m(T2-T1)
Q=W+△U

△A=△U-△(TS)
△G=△H-△(TS)
多方可逆:
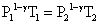
△H=nCp,m(T2-T1)
△U=nCv,,m(T2-T1)

Raoult定律:
pA=pA*xA=pA*(1-xB)
p=pA*xA+pB*xB
…… …… 余下全文
篇二 :物理化学(下)总结
《物理化学》(下) (南京大学第五版)总结
第八章 电解质溶液
一、基本概念与定义
1. 离子迁移数t
电解质溶液导电时,溶液中的i离子运载的电流Ii与总电流之比(即i离子所承担的导电任务的分数)。

2. 离子电迁移率(离子淌度)ui:单位电位梯度时离子的运动速率。
3. 电导与电导率
电导G(W-1):电阻R的倒数。a
电导率k(W-1·m-1):电阻率r的倒数。
电导池常数Kcell:Kcell = L/A
L: 电极之间的距离;A:电极的面积
4. 摩尔电导率Lm(S·m2·mol-1)
含1mol电解质的溶液置于相距单位距离的2个平行电极之间的电导池所具有的电导。
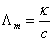
5.电解质的平均活度和平均活度因子
对于任意价型的强电解质Mn+Bn-
平均活度因子 g± =[ (g+)n+ (g-)n-]1/(n+ +n-)
a± = m±g±
m± =[ (m+)n+ (m-)n-]1/(n+ +n-)
m+ = n+m;m- = n-m
…… …… 余下全文
篇三 :大学物理化学下册(第五版傅献彩)知识点分析归纳 (1)
第八章 电解质溶液




第九章
1.可逆电极有哪些主要类型?每种类型试举一例,并写出该电极的还原反应。对于气体电极和氧化还原电极在书写电极表示式时应注意什么问题?
答:可逆电极有三种类型:
(1)金属气体电极 如Zn(s)|Zn2+ (m) Zn2+(m) +2e- = Zn(s)
(2)金属难溶盐和金属难溶氧化物电极 如 Ag(s)|AgCl(s)|Cl-(m), AgCl(s)+ e- = Ag(s)+Cl-(m)
(3)氧化还原电极 如: Pt|Fe3+(m1),Fe2+(m2) Fe3+(m1) +e- = Fe2+(m2)
对于气体电极和氧化还原电极,在书写时要标明电极反应所依附的惰性金属。
2.什么叫电池的电动势?用伏特表侧得的电池的端电压与电池的电动势是否相同?为何在测电动势时要用对消法?
答:正、负两端的电势差叫电动势。不同。当把伏特计与电池接通后,必须有适量的电流通过才能使伏特计显示, 这样电池中发生化学反应, 溶液浓度发生改变, 同时电池有内阻,也会有电压降,所以只能在没有电流通过的情况下才能测量电池的电动势。
…… …… 余下全文
篇四 :物理化学各章节总结
物理化学每章总结
第1章热力学第一定律及应用
1.系统、环境及性质
热力学中把研究的对象(物质和空间)称为系统,与系统密切相关的其余物质和空间称为环境。根据系统与环境之间是否有能量交换和物质交换系统分为三类:孤立系统、封闭系统和敞开系统。

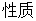

2.热力学平衡态
系统的各种宏观性质不随时间而变化,则称该系统处于热力学平衡态。必须同时包括四个平衡:力平衡、热平衡、相平衡、化学平衡。
3.热与功
(1) 热与功的定义
热的定义:由于系统与环境间温度差的存在而引起的能量传递形式。以Q表示,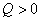 表示环境向系统传热。
表示环境向系统传热。
功的定义:由于系统与环境之间压力差的存在或其它机、电的存在引起的能量传递形式。以W表示。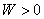 表示环境对系统做功。
表示环境对系统做功。
(2) 体积功与非体积功
功有多种形式,通常涉及到是体积功,是系统体积变化时的功,其定义为: 
…… …… 余下全文
篇五 :物理化学重点(总结好累啊)
第一章 热力学第一定律
1、热力学三大系统:
(1)敞开系统:有物质和能量交换;
(2)密闭系统:无物质交换,有能量交换;
(3) 隔绝系统(孤立系统):无物质和能量交换。
2、状态性质(状态函数):
(1)容量性质(广度性质):如体积,质量,热容量。
数值与物质的量成正比;具有加和性。
(2)强度性质:如压力,温度,粘度,密度。
数值与物质的量无关;不具有加和性,整个系统的强度性质的数值与各部分的相同。
特征:往往两个容量性质之比成为系统的强度性质。
3、热力学四大平衡:
(1)热平衡:没有热隔壁,系统各部分没有温度差。
(2)机械平衡:没有刚壁,系统各部分没有不平衡的力存在,即压力相同
(3)化学平衡:没有化学变化的阻力因素存在,系统组成不随时间而变化。
(4)相平衡:在系统中各个相(包括气、液、固)的数量和组成不随时间而变化。
4、热力学第一定律的数学表达式:
…… …… 余下全文
篇六 :物理化学总结
指出下列各过程中,物系的?U、?H、?S、?A、?G中何者为零?
⑴ 理想气体自由膨胀过程;
⑵ 实际气体节流膨胀过程;
⑶ 理想气体由(p1,T1)状态绝热可逆变化到(p2,T2)状态;
⑷ H2和Cl2在刚性绝热的容器中反应生成HCl;
⑸ 0℃、 时,水结成冰的相变过程;
时,水结成冰的相变过程;
⑹ 理想气体卡诺循环。
(1) ΔU = ΔH = 0; (2) ΔH = 0; (3) ΔS = 0; (4) ΔU = 0;
(5) ΔG = 0; (6) ΔU、ΔH、ΔS、ΔA、ΔG都为 0。
熵差ΔS就是过程的热温商。7. ×; 熵差ΔS是可逆过程的热温商.
在孤立系统中发生的任何过程都是自发过程。√
…… …… 余下全文
篇七 :物理化学重要概念公式总结
第一章 热力学第一定律
一、基本概念
系统与环境,状态与状态函数,广度性质与强度性质,过程与途径,热与功,内能与焓。
二、基本定律
热力学第一定律:ΔU=Q+W。
焦耳实验:ΔU=f(T) ; ΔH=f(T)
三、基本关系式
1、体积功的计算 δW= -pedV
恒外压过程:W= -peΔV
可逆过程: W=nRT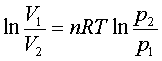
2、热效应、焓
等容热:QV =ΔU(封闭系统不作其他功)
等压热:Qp =ΔH(封闭系统不作其他功)
焓的定义:H=U+pV ; dH=dU+d(pV)
焓与温度的关系:ΔH=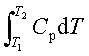
3、等压热容与等容热容
热容定义: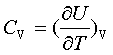 ;
;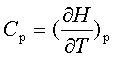
定压热容与定容热容的关系:
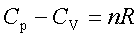
热容与温度的关系:Cp=a+bT+c’T2
四、第一定律的应用
1、理想气体状态变化
等温过程:ΔU=0 ; ΔH=0 ; W=-Q= pedV
pedV
等容过程:W=0 ; Q=ΔU=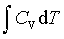 ; ΔH=
; ΔH=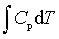
等压过程:W=-peΔV ; Q=ΔH=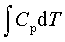 ; ΔU=
; ΔU=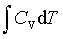
可逆绝热过程:
Q=0 ; 利用p1V1γ=p2V2γ求出T2,
…… …… 余下全文
篇八 :物理化学下册总结
第七章
1. 法拉第定律:Q=zFξ
2. 迁移数计算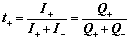
【例】用铜电极电解CuSO4溶液,通电一定时间后测得银电量计中析出0.7512g银,并测得阳极区溶液中CuSO4质量增加0.3948g。试求CuSO4溶液中离子的迁移数t(Cu2+)和t(SO42-)。(已知摩尔质量M (Ag) = 107.868 g·mol-1,M (CuSO4) =159.604 g·mol-1。)
解:电量计中析出银的物质的量即为通过总电量:n (电) =0.7512g/M(Ag)= 6.964×10-3 mol
阳极区对Cu2+ 进行物料衡算:n (原) + n (电)-n (迁出) = n (后)
n (迁出) = n (原) -n (后) + n (电)
n (迁出) =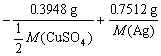
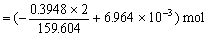 =2.017×10-3 mol
=2.017×10-3 mol
t (Cu2+) = 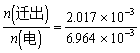 =0.2896
=0.2896
t (SO42-) =1-t (Cu2+) = 0.7164
3. 电导(G):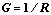 ,电导率
,电导率 ,摩尔电导率:
,摩尔电导率:
【例】已知25℃时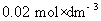 KCl溶液的电导率为0.2768 S·m-1。一电导池中充以此溶液,在25 ℃时测得其电阻为453Ω。在同一电导池中装入同样体积的质量浓度为0.555g.dm-3的CaCl2溶液,测得电阻为1050Ω。计算(1)电导池系数;(2)CaCl2溶液的电导率;(3)CaCl2溶液的摩尔电导率。
KCl溶液的电导率为0.2768 S·m-1。一电导池中充以此溶液,在25 ℃时测得其电阻为453Ω。在同一电导池中装入同样体积的质量浓度为0.555g.dm-3的CaCl2溶液,测得电阻为1050Ω。计算(1)电导池系数;(2)CaCl2溶液的电导率;(3)CaCl2溶液的摩尔电导率。
…… …… 余下全文