篇一 :物质的量知识点总结
物质的量知识点复习
1、 摩尔
物质的量是国际规定的七个基本物理量之一,用来表示含一定数目粒子的集体,符号是n,单位是mol。
摩尔是计量原子、分子、或离子等微观粒子的物质的量的单位。 阿伏伽德罗常数是任何粒子的粒子数,符号是NA,常用6.02×1023
这个近似值。
2、 摩尔质量
1mol任何粒子或物质的质量以克为单位时,在数值上都与相对原子质量或相对分子质量相等。
摩尔质量是指单位物质的量的物质所具有的质量,符号是M,常用单位是g〃mol-1
3、 使用摩尔这个概念时应注意的事项
(1) 摩尔是物质的量单位,每摩尔物质含有阿伏伽德罗常数个粒子,
摩尔简称摩,符号mol。
(2) 摩尔的量度对象是构成物质的基本粒子,这里的“粒子”是指
“基本单元”,这个基本单元可以是分子、原子、离子、电子、质子、中子等单一粒子,也可以是这些粒子的特定组合。如1molCaCl2可以说含1molCa2+,2molCl-或3mol阴、阳离子,或
含54mole-等。
(3) 摩尔概念只适用微观不适用于宏观。
(4) 使用摩尔表示物质的量时,应该用化学式指明粒子种类,而不
是使用该粒子的中文名称。
…… …… 余下全文
篇二 :物质的量单元知识点复习小结
物质的量单元知识点复习小结
一、有关概念:
1、物质的量(n)
①物质的量是国际单位制中七个基本物理量之一。
②用物质的量可以衡量组成该物质的基本单元(即微观粒子群)的数目的多少,它的单位是摩尔,即一个微观粒子群为1摩尔。
③摩尔是物质的量的单位。摩尔是国际单位制中七个基本单位之一,它的符号是mol。
④ “物质的量”是以摩尔为单位来计量物质所含结构微粒数的物理量。 ⑤摩尔的量度对象是构成物质的基本微粒(如分子、原子、离子、质子、中子、电子等)或它们的特定组合。如1molCaCl2可以说含1molCa2+,2molCl-或3mol
阴阳离子,或含54mol质子,54mol电子。摩尔不能量度宏观物质,如果说“1mol氢”就违反了使用准则,因为氢是元素名称,不是微粒名称,也不是微粒的符号或化学式。
⑥使用摩尔时必须指明物质微粒的名称或符号或化学式或符号的特定组合。
2.阿伏加德罗常数(NA):
①定义值(标准):以0.012kg(即12克)碳-12原子的数目为标准;1摩任何物质的指定微粒所含的指定微粒数目都是阿伏加德罗常数个。
②近似值(测定值):经过科学测定,阿伏加德罗常数的近似值一般取6.02×1023,单位是mol-1,用符号NA表示。
…… …… 余下全文
篇三 :高一化学物质的量知识点归纳2
化学计量在实验中的应用
国际单位制(SI)的7个基本单位
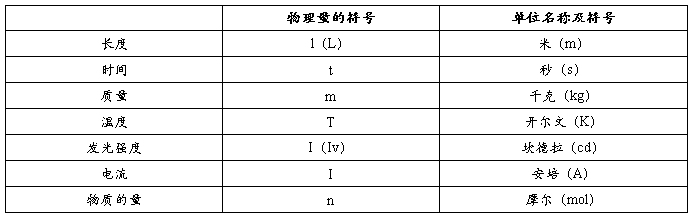
考点一:物质的量与摩尔质量
1.物质的量
1.定义:表示物质所含微粒多少的物理量,也表示含有一定数目粒子的集合体。
2.物质的量是以微观粒子为计量的对象。
3.物质的量的符号为“n”。
3.符号是mol(摩尔)。
4.使用摩尔表示物质的量时,应该用化学式指明粒子的种类。
例如:1molH表示mol氢原子,1mol H2表示1mol氢分子(氢气),1mol H+表示1mol氢离子,但如果说“1mol氢”就违反了使用标准,因为氢是元素名称,不是微粒名称,也不是微粒的符号或化学式。不能说1 mol氢,应该说1 mol氢原子(或分子或离子)。
5.“物质的量”四个字是一个整体概念,不得简化或增添任何字,如不能说成“物质量”“物质的质量”或“物质的数量”等。
6.物质的量表示的是微观粒子或微观粒子的特定组合的集合体,不适用于宏观物质,如1 mol苹果的说法是错误的。
7.物质的量中所指粒子包括分子、原子、离子、质子、中子、电子、原子团等微观粒子或微观粒子的特定组合(如NaCl、Na2SO4等)。
2.阿伏加德罗常数NA
…… …… 余下全文
篇四 :物质的量知识点小结
物质的量知识点小结
有关概念:
1、物质的量(n)
①物质的量是国际单位制中七个基本物理量之一。
②用物质的量可以衡量组成该物质的基本单元(即微观粒子群)的数目的多少,它的单位是摩尔,即一个微观粒子群为1摩尔。
③摩尔是物质的量的单位。摩尔是国际单位制中七个基本单位之一,它的符号是mol。
④ “物质的量”是以摩尔为单位来计量物质所含结构微粒数的物理量。
⑤摩尔的量度对象是构成物质的基本微粒(如分子、原子、离子、质子、中子、电子等)或它们的特定组合。如1molCaCl2可以说含1molCa2+,2molCl-或3mol阴阳离子,或含54mol质子,54mol电子。摩尔不能量度宏观物质,如果说“1mol氢”就违反了使用准则,因为氢是元素名称,不是微粒名称,也不是微粒的符号或化学式。
⑥使用摩尔时必须指明物质微粒的名称或符号或化学式或符号的特定组合。
2.阿伏加德罗常数(NA):
①定义值(标准):以0.012kg(即12克)碳-12原子的数目为标准;1摩任何物质的指定微粒所含的指定微粒数目都是阿伏加德罗常数个。
②近似值(测定值):经过科学测定,阿伏加德罗常数的近似值一般取6.02×1023,单位是mol-1,用符号NA表示。
3.摩尔质量(M):
①定义:1mol某微粒的质量
…… …… 余下全文
篇五 :物质的量知识点整理
第六讲 物质的量
1. 复习重点
1.理解质量守恒定律的涵义。
2.明确摩尔的概念,掌握摩尔质量与相对分子质量、相对原子质量之间的区别与联系、理解阿伏加德罗常数的涵义,其中阿伏加德罗常数是命题的热点
2.难点聚焦
一、质量守恒定律
1.内容 参加化学反应的物质的质量总和等于反应后生成的物质的质量总和。
2.实质 化学反应前后元素的种类和原子的个数不发生改变。
二、阿伏加德罗定律
1.内容
在同温同压下,同体积的气体含有相同的分子数。即“三同”定“一同”。
2. 推论:
⑴同温同压下,V1/V2=n1/n2
…… …… 余下全文
篇六 :物质的量相关知识点总结
一、物质的量及单位——摩尔
1. 物质的量
以________中所含的_________数为标准来衡量其他微粒集体所含微粒数目多少的物理量,符号为________,单位是________.当使用该单位时,应指明对象是___________包括_______________________.
2. 阿伏伽德罗常数
________所含的________称为阿伏伽德罗常数,符号为________,其值约为________,单位是________.
3. 物质的量、阿伏伽德罗常数与微粒数目(N)之间的数学表达式为n=N/NA。
4. 摩尔质量
________的物质所具有的质量叫摩尔质量,符号为________,单位为________或________.当摩尔质量的单位用________表示时,其数值等于该粒子的________.
5. 摩尔质量、物质的量与物质的质量之间的关系可用数学表达式表示为________.
二、气体摩尔体积
1. 气体摩尔体积:________所占的体积,符号为Vm,单位为________或________,它取决于气体所处的________和________,其中在标准状况下,即为_______℃、________kPa下,约为________.
…… …… 余下全文
篇七 :物质的量知识点小结
物质的量知识点小结
有关概念:
1、物质的量(n)
①物质的量是国际单位制中七个基本物理量之一。
②用物质的量可以衡量组成该物质的基本单元(即微观粒子群)的数目的多少,它的单位是摩尔,即一个微观粒子群为1摩尔。
③摩尔是物质的量的单位。摩尔是国际单位制中七个基本单位之一,它的符号是mol。
④ “物质的量”是以摩尔为单位来计量物质所含结构微粒数的物理量。
⑤摩尔的量度对象是构成物质的基本微粒(如分子、原子、离子、质子、中子、电子等)或它们的特定组合。如1molCaCl2可以说含1molCa2+,2molCl-或3mol阴阳离子,或含54mol质子,54mol电子。摩尔不能量度宏观物质,如果说“1mol氢”就违反了使用准则,因为氢是元素名称,不是微粒名称,也不是微粒的符号或化学式。
⑥使用摩尔时必须指明物质微粒的名称或符号或化学式或符号的特定组合。
2.阿伏加德罗常数(NA):
①定义值(标准):以0.012kg(即12克)碳-12原子的数目为标准;1摩任何物质的指定微粒所含的指定微粒数目都是阿伏加德罗常数个。
②近似值(测定值):经过科学测定,阿伏加德罗常数的近似值一般取6.02×1023,单位是mol-1,用符号NA表示。
3.摩尔质量(M):
①定义:1mol某微粒的质量
…… …… 余下全文
篇八 :物质的量知识点总结
一、物质的量及其单位:
1、物质的量:与质量、长度等一样,是科学上来研究微粒的物理量。它的单位是摩尔。即:摩尔是表示物质的量的单位。(mol)
2、摩尔的基准:科学上以12克 所含的原子数作为摩尔的基准。即每摩尔物质含有阿伏加德罗常数个微粒,近似值为6.02×1023。
所含的原子数作为摩尔的基准。即每摩尔物质含有阿伏加德罗常数个微粒,近似值为6.02×1023。
小结:物质的量n(mol)=N/NA
二、摩尔质量:1mol物质中,微粒数是确定的,因而其总质量也随之确定。
定义:1mol物质的质量叫该物质的摩尔质量。单位:
小结:物质的量n(mol)=
例:33g二氧化碳的物质的量是?与多少克氢气所含的分子数相等?
三、气体摩尔体积:
1、固体和液体的摩尔体积:
2、气体的摩尔体积:
气体体积由分子间的平均距离决定,在相同条件下分子间平均距离相等,则体积相等。
定义:在标准状况下,1mol的任何气体所占的体积都约是22.4升,这个体积叫做气体摩尔体积。单位“升/摩”。
小结:物质的量n(mol)=V/Vm
四、阿伏加德罗定律及其应用:
定义:在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子,这就是阿伏加德罗定律(即三同和一同)。
PV=nRT
…… …… 余下全文