20xx初中化学考点总结
初三化学方程式总结
与氧有关的化学方程式:
(1)2Mg+O2点燃====2MgO 现象:
(2)S+O2 点燃====SO2 现象:
(3)C+O2(充足)点燃====CO2 现象:
(4)2C+O2(不充足)点燃====2CO
(5)4P+5O2点燃====2P2O5 现象:
(6)3Fe+2O2点燃====Fe3O4 现象:
(7)2H2+O2点燃====2H2O 现象:
(8)2HgO△====2Hg+O2↑ 现象:(9)实验室制取氧气的三种方法:
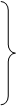 2H2O2MnO2====2H2O+O2↑ (“固+液”不加热型------制氧气)
2H2O2MnO2====2H2O+O2↑ (“固+液”不加热型------制氧气)
2KClO3MnO2====2KCl+3O2↑ (“固+固”加热型------制氧气) 实验室制氧气的三种方法
2KMnO4△====K2MnO4+MnO2+O2↑ (“固+固”加热型------制氧气)
跟氢有关的化学方程式:
(10)实验室制取氢气的方法:锌粒与稀硫酸反应实验室
Zn+H2SO4==ZnSO4+H2↑ 现象:
(11)Mg+H2SO4==MgSO4+H2↑ 现象:
(12)Fe+H2SO4 ==FeSO4+H2↑ 现象:
(13)2Al+3H2SO4 ==Al2(SO4)3+3H2↑ 现象:
(14)Zn+2HCl==ZnCl2+H2↑ 现象:
(15)Mg+2HCl==MgCl2+H2↑ 现象:
(16)Fe+2HCl==FeCl2+H2↑ 现象:
(17)2Al+6HCl==2AlCl3+3H2↑ 现象:
(18)氢气还原氧化铜:H2+CuO△====Cu+H2O
现象:
(19)氢气还原氧化铁:
3H2+2Fe2O高温====2Fe+3H2O 现象:
跟碳有关的化学方程式:
(20)碳高温还原氧化铜:
高温
C+2CuO=====2Cu+CO2↑ 现象:
(21)碳高温还原氧化铁:
高温
3C+2Fe2O3=====4Fe+3CO2↑现象:
(22)CO2+C高温====2CO 现象:
(23)C+H2O高温====H2+CO(生成的混和气体叫水煤气,都是可以燃烧的气体)
跟二氧化碳有关的化学方程式:
(24)用澄清石灰水检验二氧化碳气体:
Ca(OH)2+CO2===CaCO3↓+H2O 现象:
(25)用氢氧化钠溶液吸收二氧化碳气体:
2NaOH+CO2===Na2CO3+H2O
(26)2KOH+CO2===K2CO3+H2O
(27)碳酸钙与二氧化碳、水反应生成碳酸氢钙:
CaCO3+CO2+H2O===Ca(HCO3)2 现象:
(28)碳酸氢钙加热分解:
Ca(HCO3) △====CaCO3+CO2↑+H2O
(29)铜绿加热分解:
Cu2(OH)2CO3△====2CuO+H2O+CO2↑ 现象:
(30)高温煅烧石灰石:
CaCO3高温====CaO+CO2↑ (工业上制取二氧化碳的方法)
现象:
跟一氧化碳有关的,但同时也跟二氧化碳有关:
(31)一氧化碳高温还原四氧化三铁:
高温
Fe3O4+4CO====3Fe+4CO2现象:
(32)一氧化碳高温还原氧化亚铁:
高温
FeO+CO===Fe+CO2 现象:
(33)一氧化碳高温还原氧化铁:
高温
Fe2O3+3CO====2Fe+3CO2 (炼铁的原理)
现象:
(34)一氧化碳加热还原氧化铜:
CuO+CO△====Cu+CO2 现象:
跟盐酸有关的化学方程式:
(35)NaOH+HCl==NaCl+H2O (中和反应)
(36)KOH+HCl==KCl+H2O (中和反应)
(37)稀盐酸与硝酸银溶液反应:
HCl+AgNO3==AgCl↓+HNO3 现象:(此反应用于检验氯离子)
用AgNO3溶液和稀硝酸(HNO3)
(38)实验室制取二氧化碳的方法:
CaCO3+2HCl==CaCl2+H2O+CO2↑ (实验室制取二氧化碳的方法)
现象:
(39)碳酸纳与稀盐酸反应:
Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:
(40)碳酸氢钠与稀盐酸反应:
NaHCO3+HCl==NaCl+H2O+CO2↑ 现象:
治疗胃酸过多的一种盐的是:NaHCO3 反应的化学方程式:NaHCO3+HCl==NaCl+H2O+CO↑
(41)Al(OH)3+3HCl==AlCl3+3H2O (治疗胃酸的方法)
治疗胃酸过多的一种碱是:Al(OH)3 反应的化学方程式:Al(OH)3+3HCl==AlCl3+3H2O
(42)用稀盐酸除铁锈:
Fe2O3+6HCl==2FeCl3+3H2O 现象:
(除去铁锈的方法―――用酸来除:稀盐酸、稀硫酸、硝酸、醋酸等都行)
(43)氢氧化铁与稀盐酸反应:
Fe(OH)3+3HCl==FeCl3+3H2O 现象:
(44)氢氧化铜与稀盐酸反应:
Cu(OH)2+2HCl==CuCl2+2H2O 现象:
(45)氧化铜与稀盐酸反应:
CuO+2HCl==CuCl2+H2O 现象:
跟硫酸有关的化学方程式:
(46)2NaOH+H2SO4==Na2SO4+2H2O (中和反应)
(47)2KOH+H2SO4==K2SO4+2H2O (中和反应)
(48)用稀硫酸来除铁锈:
Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 现象:
(49)CuO+H2SO4==CuSO4+H2O 现象:
(50)Cu(OH)2+H2SO4==CuSO4+2H2O 现象:
(51)H2SO4+BaCl2==BaSO4↓+2HCl 现象:(检验硫酸根离子)
(52)CaCO3+H2SO4==CaSO4+H2O+CO2↑
(53)Na2CO3+H2SO4==Na2SO4+H2O+CO2↑ 现象:
(54)2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑ 现象:
跟硝酸有关的化学方程式:
(55)Fe2O3+6HNO3==2Fe(NO3)3+3H2O 现象:
氧化铜溶于稀硝酸中:
CuO+2HNO3==Cu(NO3)2 +H2O 现象:
(56)氢氧化铜与稀硝酸反应:
Cu(OH)2+2HNO3==Cu(NO3)2+2H2O 现象:
(57)氢氧化钠溶液与稀硝酸反应:
NaOH+HNO3==NaNO3+H2O
(58)氢氧化钾溶液与稀硝酸反应:
KOH+HNO3==KNO3+H2O
(59)氢氧化镁与稀硝酸反应:
Mg(OH)2+2HNO3==Mg(NO3)2+2H2O 现象:
(60)大理石与稀硝酸反应:
CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑现象:
(61)碳酸钠与稀硝酸反应:
Na2CO3+2HNO3==2NaNO3+H2O+CO2↑ 现象:
(62)碳酸氢钠与稀硝酸反应:
NaHCO3+HNO3==NaNO3+H2O+CO2↑ 现象:
跟碱有关的化学方程式:
(63)氢氧化钠与稀盐酸反应:
NaOH+HCl==NaCl+H2O
(64)生石灰与水反应:
CaO+H2O==Ca(OH)2 现象:放出大量的热
扩充:
放热的物质:
吸热的物质:
(65)氢氧化钠与氯化铁溶液反应:
NaOH+FeCl3==Fe(OH)3↓+NaCl 现象:
(66)氢氧化钾溶液与氯化铁溶液反应:
KOH+FeCl3==Fe(OH)3↓+KCl
(67)氢氧化钾与硝酸铁溶液反应:
3KOH+Fe(NO3)3==Fe(OH)3↓+3KNO3
(68)氢氧化钠与硝酸铁溶液反应:
3NaOH+Fe(NO3)3==Fe(OH)3↓+3NaNO3
(69)氢氧化钠与硫酸铁溶液反应:
6NaOH+Fe2(SO4)3==2Fe(OH)3↓+3Na2SO4
(70)氢氧化钾与硫酸铁溶液反应:
6KOH+Fe2(SO4)3==2Fe(OH)3↓+3K2SO4
(71)2NaOH【KOH】+CuCl2【Cu(NO3)2、CuSO4】==Cu(OH)2↓+2NaCl
现象:
【括号里面的反应过程相似,产物相对应就行了】
(72)NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl
现象:
【括号里反应产物相对应】
(73)MgCl2【Mg(NO3)2、MgSO4】+NaOH【KOH】==Mg(OH)2↓+NaCl
现象:生成白色沉淀【括号里面的反应过程相似,产物相对应就行了】
(74)用氢氧化钠溶液来吸收二氧化碳:
2NaOH+CO2==Na2CO3+H2O (用于吸收或除去混合气体中的二氧化碳气体)
(75)用澄清石灰水来检验二氧化碳:
Ca(OH)2+CO2==CaCO3↓+H2O 现象:产生白色沉淀(此反应用于检验二氧化碳)
(76)硫酸氢纳溶液与氢氧化钠溶液反应: NaHSO4+NaOH==Na2SO4+H2O
(77)用氢氧化钠溶液来吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O
(78)氢氧化钠溶液与三氧化硫反应: 2NaOH+SO3==Na2SO4+H2O
跟钡盐有关的化学方程式:
(79)氯化钡溶液与硫酸钠溶液反应:
BaCl2+Na2SO4==BaSO4↓+2NaCl 现象:有白色沉淀产生且不溶于稀硝酸
(80)氯化钡溶液与碳酸钠溶液反应:
BaCl2+Na2CO3==BaCO3↓+2NaCl 现象:有白色沉淀生成但可溶于稀硝酸
跟钙盐有关的化学方程式:
(81)氯化钙溶液与碳酸钠溶液反应:
CaCl2+Na2CO3==CaCO3↓+2NaCl 现象:生成白色沉淀
(82)向澄清石灰水中通入过量的二氧化碳气体
Ca(OH)2+CO2==CaCO3↓+H2O
CaCO3+CO2+H2O==Ca(HCO3)2
现象:
跟几种金属及其盐有关的化学方程式:
铜:
(83)白色硫酸铜固体与水反应生成蓝色晶体
CuSO4+5H2O === CuSO4?5H2O (用于检验混合气体中的水蒸气)
现象:
(84)蓝色晶体五水硫酸铜加热生成白色固体无水硫酸铜
CuSO4?5H2O△====CuSO4+5H2O↑ 现象:
(85)一氧化碳还原氧化铜:
CuO+CO△====Cu+CO2
现象:
(86)氢气还原氧化
H2+CuO△====Cu+H2O 现象:
(87)铜丝与硝酸银溶液反应:
Cu+2AgNO3==Cu (NO3)2+2Ag 现象:
(88)氯化铜溶液与氢氧化钠溶液反应:
CuCl2+2NaOH==Cu (OH) 2↓+2NaCl 现象:
(89)氧化铜溶于稀硫酸中:
CuO+H2SO4==CuSO4+H2O 现象:
(90)氢氧化铜与稀硫酸反应:
(91)铁丝插入硫酸铜溶液中:
Fe+CuSO4==FeSO4+Cu 现象:铁丝表面有红色物质生成,溶液由蓝色变为浅绿色
(92)锌片插入硫酸铜溶液中:
Zn+CuSO4== ZnSO4+Cu
(93)加热铜绿 Cu2(OH)2CO3△====2CuO+H2O+CO2↑
现象:
铁:
(94)铁粉与稀盐酸反应:
Fe+2HCl==FeCl2+H2 现象:
(95)氯化亚铁溶液与氢氧化钠溶液反应:
FeCl2+2NaOH==Fe(OH)2↓+NaCl 现象:
(96)氢氧化亚铁不稳定,在空气中放置一段时间后会发生化学变化:
4Fe(OH)2+O2+2H2O==4Fe(OH)3 现象:
(97)氢氧化铁与稀盐酸反应:
Fe (OH) 3+3HCl==FeCl3+3H2O 现象:
(98)氢氧化亚铁与稀盐酸反应:
Fe (OH) 2+2HCl==FeCl2+2H2O 现象:
(99)铁钉与硫酸铜溶液反应:
Fe+CuSO4==FeSO4+Cu 现象:
(100)铁钉与硝酸银溶液反应
Fe+AgNO3==Fe(NO3)2+Ag 现象:
银:
硝酸银溶液与稀盐酸反应:(此反应用于检验氯离子)
AgNO3+HCl==AgCl↓+HNO3 现象:有白色沉淀生成,且不溶于强酸
硝酸银溶液与氯化钠溶液反应:
AgNO3+NaCl==AgCl↓+NaNO3 现象:有白色沉淀生成,且不溶于强酸
铜与硝酸银溶液反应:
Cu+2AgNO3==Cu(NO3)2+2Ag 现象:红色的铜逐渐溶解,同时有银白色物质生成,溶液变蓝
补充化学方程式:
3Ag+4HNO3(稀)==3AgNO3+NO↑+2H2O 现象:银逐渐溶解,生成气体遇空气变红棕色
Ag+2HNO3(浓)==AgNO3+NO2↑+H2O 现象:银逐渐溶解,生成红棕色气体
Cu+2H2SO4(浓)==CuSO4+SO2↑+2H2O 现象:铜逐渐溶解,生成有刺激性气味的气体,溶液变蓝
2FeCl3+Fe==3FeCl2 现象:铁粉逐渐溶解,溶液由黄色变成浅绿色
2Na2O2(过氧化钠)+2H2O=4NaOH+ O2↑现象:有能使带火星的木条复燃的气体生成
化学方程式练习
一 化学方程式的基础知识:
配平下列的各个化学反应的方程式:
(1) KMnO4 — K2MnO4 + MnO2 + O2↑
(2) Al + CuSO4 — Al2(SO4)3 + Cu
(3) Zn + HCl — ZnCl2 + H2↑
(4) Al2O3 + H2SO4 Al2(SO4)3 + H2O
(5) Fe2(SO4)3 + NaOH — Na2SO4 + Fe(OH)3
(6) Fe(OH)3 + H2SO4 Fe2(SO4)3 + H2O
(7) CH4 + O2点燃 CO2 + H2O
(8) C + CO2高温 CO
(9) NH3 + O2催化剂 NO + H2O
(10) CO + Fe2O3高温 Fe + CO2
二 练习
1 在X + 2O2===CO2 + 2H2O的反应中,根据质量守恒定律可判断出X的化学式为:
A CO B CH4 C CH3OH D C2H4
2 某纯净物X在空气中完全燃烧,反应式为: X + 3 O2=== 2CO2 + 3 H2O,根据质量守恒定律可判断出X的化学式为:
A C2H4 B C2H4O C C2H6 D C2H6O
3 在4Cu + 10HNO3 = 4Cu(NO3)2 + X + 5H2O反应方程式中,X的化学式为:
A NO B NO2 C N2O D N2O3
4 物质X和B2能发生下列反应:2X + B2 = 2 AB3,则X的化学式是:
A AB2 B A2B2 C AB3 D A2B3
5 某化合物R在空气燃烧后生成二氧化碳和水,下列关于R化学式叙述正确的是:
A R一定含有碳,氢,氧三种元素
B R一定含有碳和氢元素,不含有氧元素
C R一定含有碳和氢元素,可能含有氧元素
D R不一定含有碳和氢元素,但一定不含有氧元素
6 某物质W在氧气中充分燃烧后,生成了4.4克CO2和3.6克的水,消耗的氧气为6.4克 ,则W中所含有的元素判断正确的是:
A 一定含有C H元素,不含O元素
B 一定含有 C H 元素,可能有O元素
C 一定含有C H O三种元素
D 条件不足,不能判断
7 氢气与氧气反应生成水的反应过程中,氢气与氧气的质量之比是:
A 1 :1 B 2 :1 C 2 :32 D 4 : 32
8 对于质量守恒定律的解释不正确的是:
A 化学反应前后,分子的数目不变
B 化学反应前后,原子的种类不变。
C 化学反应前后,原子的数目不变。
D 化学反应前后,参加反应的物质的总质量和生成物的总质量相等
9 白色固体粉末氯酸钾(KClO3)在二氧化锰(MnO2)作催化剂并加热的条件下能较快地生成 氯化钾(KCl)和氧气,试写出该反应的化学方程式:
10 发射卫星的火箭用联氨(N2H4)作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成。该反应的化学方程式为____________________________________ __。
11 剧烈运动后血液中产生了较多乳酸(C3H6O3),使人肌肉酸痛,经过一段时间放松,由于乳酸与吸入的氧气反应,生成二氧化碳和水,酸痛感消失。该反应的化学方程式为____________________________________________。
12 汽车尾气(含有CO,SO2与NO等物质)是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个“催化转换器”,其特点是使CO和NO反应,生成一种空气中含量最多的气体,另一种可参与植物光合作用的气体。写出CO与NO反应的化学方程式是
___ ____ _。
13 镁是一种活泼的金属,点燃后,既能在氮气中燃烧也能在二氧化碳中继续燃烧。已知镁在氮气中燃烧,生成一种叫氮化镁(氮显-3价)固体的化合物;镁在二氧化碳中燃烧,生成黑色炭粒与一种白色固体粉末。试写出以上发生的两条化学方程式:
① ,② 。
14 简答题:镁条在空气中燃烧后生成氧化镁,理论上生成物多一种元素,质量应比镁条重,但同学们实验后称量收集的氧化镁反而轻,原因是:___ ____
___ ____ ___ ____ 一、 选择题
1、对质量守恒定律的解释正确的是
A、化学反应前后原子种类不变,原子数目改变
B、化学反应前后原子种类改变,原子个数不变
C、在一切化学反应里,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量也没有变化
D、在化学反应中反应物的分子数等于生成物的分子数
2、在A+B=C+D反应中,5克A和4克B恰好完全反应生成3克C,则生成D的质量为
A、 4克
B、 3克
C、 5克
D、 6克
3、在化学反应前后,下列哪一种微粒的总数可能改变
A、质子
B、原子
C、电子
D、分子
4、根据化学方程式:3AB+C2B3=2C+3X,确定X的化学式为
A、 A3B2
B、 A2B3
C、 AB2
D、 AB3
5、某化合物密封加热完全分解后生成氨气、水和二氧化碳,则该物质中一定含有的元素是
A、O、H、C
B、N、H、O
C、N、O、H
D、C、H、O、N
6、在化学反应A+B→C,3克A跟足量的B充分反应,生成11克C,则参加反应的B的质量是
A、3克
B、5克
C、 8克
D、 11克
7、将物质A、B、C各10克混和后加热,A全部参加反应,生成3克D,同时增加9克C,则反应中A与B的质量比为
A、1 :5
B、1 :4
C、4 :1
D、5 :1
8、某元素R的单质在纯氧中燃烧后,所得生成物式量为94,已知R的原子量为39,则该生成物的化学式是
A、 R2O3
B、 R2O
C、 RO
D、 RO2
9、根据质量守恒定律判断,在2AB2+B2=2C这一反应中,C物质的化学式是
A、A2B
B、 AB2
C、 AB3
D、 AB
10、充分加热a克氯酸钾与b克二氧化锰的混合物,留下残余固体c克,则生成氧气的质量为
A、(a-b)克
B、(a-b-c)克
C、(a+b-c)克
D、(a-b+c)克
二 填空题
1、将氯酸钾和二氧化锰的混合物加热后,固体混合物中二氧化锰的质量和原来相比_____;二氧化锰的质量百分含量和原来相比_____(填增加、减少、不变)
2、 _______的各物质的质量总和,等于________生成的各物质的_________。这个规律叫质量守恒定律。
3、在A+B=C+D中,若1.6克A和B的混合物完全反应,生成C和D的质量比为3 : 5,则D为_______克
4、一定量的镁条在空气中完全燃烧后,生成的固体的质量_______镁条的质量(填大于、小于、等于),这与质量守恒定律__________(填符合或不符合)
5、 A+B=C+D生成物C和D的质量比为1 : 3,若反应物A与B在反应中消耗2.4克。则生成物中C的质量为____克,D的质量为_____克。
-
中考化学知识点总结归纳(完整版)
中考化学知识点全面总结完整版第1单元走进化学世界1化学是研究物质的组成结构性质以及变化规律的基础科学2我国劳动人民商代会制造青铜器…
-
中考化学总复习基础知识详细总结
一基本概念和基本理论一物质的变化和性质1物质的变化物理变化没有生成其他物质的变化化学变化生成了其他物质的变化化学变化和物理变化常常…
- 天津中考化学近五年考点汇总
-
中考化学知识点汇总
中考化学知识点汇总第一单元走进化学世界1化学是研究物质的组成结构性质以及变化规律的基础科学2我国劳动人民商代会制造青铜器春秋战国时…
-
初三化学中考考点归纳与点拨
初三化学中考考点归纳与点拨考点1物质的变化性质反应类型1判别物理变化还是化学变化的依据是有无新物质生成发光放热爆炸既可能是化学变化…
-
初中化学中考复习知识点总结
初中化学中考复习知识点总结一基本概念1化学变化生成了其它物质的变化2物理变化没有生成其它物质的变化3物理性质不需要发生化学变化就表…
-
20xx中考化学知识点总复习
20xx中考化学知识点总复习一基本概念和基本理论一物质的变化和性质1物质的变化物理变化没有生成其他物质的变化化学变化生成了其他物质…
-
20xx年中考化学知识点汇总人教版
20xx年中考化学知识点汇总第1单元走进化学世界知识点1化学是研究物质的组成结构性质以及变化规律的基础科学2我国劳动人民商代会制造…
-
20xx.3.12初三化学酸碱盐知识点总结
初三化学酸碱盐知识点总结一酸碱盐的组成酸是由氢元素和酸根组成的化合物如硫酸H2SO4盐酸HCl硝酸HNO3碱是由金属元素和氢氧根组…
-
20xx年人教版初中化学新版上、下册知识点系统归纳
20xx级人教版初中化学知识点绪言化学使世界变得更加绚丽多彩一什么是化学化学是研究物质的组成结构性质以及变化规律的科学化学的研究对…
-
初中化学知识点总结
中学化学工作室http://zt.jnedu.net.cn/web/20xx12956934400/app/第1页共5页中学化学工…