《环境分析化学实验》实验报告格式

《环境分析化学实验》
实验报告
专 业 环境科学
班 级 环科1201
姓 名 帕沙古丽
成 绩
东华大学环境科学与工程学院实验中心
二0一三年 月
诚信做人;数据真实;分析合理;富于创新


诚信做人;数据真实;分析合理;富于创新

6、固体KMnO 4
7、 500ml容量瓶,250 ml容量瓶,称量瓶,分析天平, 玻璃棒,棕色细口瓶,
25ml量筒,5ml 移液管 ,25ml移液管,洗瓶,
三、实验原理
? 水的硬度的测定可分为水的总硬度的测定和钙镁硬度的测定两种.总硬
度的测定是滴定Ca2+,Mg2+离子的总含量,并以Ca2+进行计算.通常以每升水中所含Ca2+离子的毫摩尔数表示,规定1升水中含1mmol Ca2+为1度.后一种是分别测定Ca2+和Mg2+的含量.测定水的总硬度,一般采用配位滴定法.最常用的配位剂是乙二胺四乙酸二钠盐,用Na2H2Y2H2O表示,习惯上称为EDTA,它在溶液中以Y4-的形式与Ca2+,Ma2+离子配位,形成1:1的无色配合物方程为 Ca2+ +Y4 =CaY2- Mg2++Y4=MgY2-
? 用EDTA滴定时,必须借助于金属指示剂确定滴定终点.常用的指示剂为铬黑
T,它在 pH=10的缓冲液中,以纯蓝色游离的HIn2-形式存在,与Ca2+,Mg2+离子形成酒红色的配合物,通式为:
? M2+ + HIn2=MIn-+ H+
(蓝色) (酒红色)
? Ca2+,Mg2+离子与EDTA及铬黑T形成配合物的稳定性不同,其稳定性大小的循
序序CaY2- >MgY2- >MgIn- >CaIn- ,用EDTA测定Ca、Mg时,通常在两个等分溶液中分别测定Ca量以及Ca和Mg的总量,Mg量则从二者所用EDTA量的差数求出。
? 在测定Ca时,先用NaOH调节溶液到pH=12~13,使Mg生成难溶的Mg(OH)
沉淀,然后加入钙指示剂与Ca配位呈红色。滴定时,EDTA先与游离Ca
2+2+2+2+22+2+2+2+2+2+2+配位,然后夺取已经和指示剂配位的Ca,使溶液的红色变成蓝色,达到终
点。从EDTA标准溶液的用量可计算Ca的含量。
滴定Ca、Mg总量时,在pH=9~10的缓冲溶液中,以铬黑T为指示剂,用EDTA滴定。因稳定性CaY> MgY>MgIn> CaIn,铬黑T先与部分Mg配位为MgIn(酒红色)。而当EDTA滴入时,EDTA首先与Ca和Mg配位,然后再夺取MgIn中的Mg,使铬黑T游离,因此到达终点时,溶液由酒红色变为天蓝色。从EDAT标准溶液的用量,即可以计算样品中的钙镁总量,然后换算为相应的硬度单位。
各国对水的硬度的表示方法各有不同。其中德国硬度是较早的一种,它以度
诚信做人;数据真实;分析合理;富于创新 2+2+2+2-2-2+2+2+2+

数计,1°表示1L水中含10mgCaO。为方便起见,我国也常以来mg/L表示。此实验中,我们采用CaCO的含量单位ppm来表 3
四、实验步骤
(一) 配制0.01MEDTA标准溶液
1、在分析天平上准确称取EDTA基准物质1.9g,于150ml的干净烧杯中。
2、加适量水溶解,用玻璃棒小心转移至500ml容量瓶中。
3、溶液全部转移到容量瓶中后,用洗瓶淋洗烧杯3~5次,淋洗液亦要小心沿玻璃棒转移入容量瓶中,不能有所损失。
4、加水至容量瓶刻度线以下,再改用小滴管滴加蒸馏水,准确至刻度线(液面最底处与刻度线相切),充分摇匀。
5、计算所配制的EDTA溶液的准确浓度,用标签标示于容量瓶上。
注意
配制EDTA标准溶液时,溶液的转移是浓度准确与否的关键。烧杯中的溶液要沿玻璃棒及容量瓶壁小心倒入,玻璃棒要从原路小心放回烧杯中,以防溶液流失。烧杯要用蒸馏水充分润洗,淋洗液应全部小心转入容量瓶中。
(二) Ca、Mg总量的测定
1、从指导教师处领取未知水样,定容于250ml容量瓶中,摇匀。
2、用未知水样润洗25ml移液管3次,注意擦干外壁,吹干内壁。
3、准确吸取25ml水样于250ml锥形瓶中,加蒸馏水50ml,加NH·HO-NHCl3242+2+缓冲溶液5ml,调节溶液pH=9~10。
4、加铬黑T指示剂3滴,摇匀。
5、用EDTA溶液滴定,当溶液由酒红色变为纯蓝色时,即为终点。记下所用体积V。 1
6、用同样方法平行测定三份。
(三) Ca的测定
1、用移液管准确吸取水样25ml于250ml锥形瓶中,加蒸馏水50ml,加6M NaOH
诚信做人;数据真实;分析合理;富于创新 2+

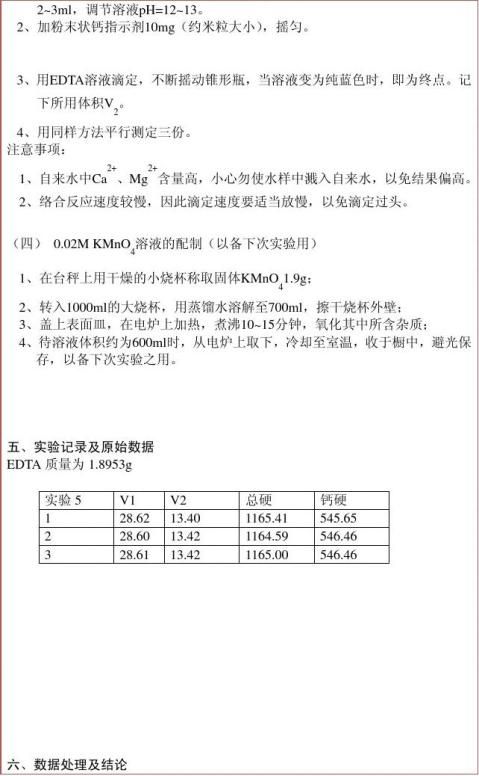
诚信做人;数据真实;分析合理;富于创新

w .1000 M EDTA=
mEDTA .500
?
=0.01018mol/L
诚信做人;数据真实;分析合理;富于创新

思考题
1、如果只有铬黑T指示剂,能否测定Ca的含量?如何测量? 答:如果只有铬黑2+T指示剂能。测定Ca2+含量时,用移液管移取水样25.00ML于锥形瓶中,加入2ML40g.L-1NAOH,调节溶液PH为12~13,使Mg2+生成Mg(OH)2沉淀,再加3~4滴铬黑T,用EDTA标准溶液滴定至溶液由酒红色变为纯蓝色为终点,记取EDTA耗用的体积
2、 Ca、Mg与EDTA的配合物,哪一个稳定?为什么滴定Mg时要控制pH=9~10,而Ca则需控制pH=12~13? 2+2+2+2+
答: Ca2+,Mg2+离子与EDTA及铬黑T形成配合物钙离子配合物稳定性大 其稳定性大小的循序序CaY2- >MgY2- >MgIn- >CaIn-
3、若测定的水样中Mg含量过高,对终点会有什么影响?如何消除其影响? 答:氢氧化镁的溶度积大约是10^-11;PH>10后容易沉淀。就测不出来了。2+即PH不得大于10。否则沉淀。氢氧化钙的溶度积大约是10^-6,-6/3+14=12,即PH=12也不会沉淀。可以测定。严格的计算结果是:氢氧化镁沉淀的最小PH=10.42;氢氧化钙沉淀的最小PH=12.24。显然,当PH>=13时,钙会沉淀,不能准确测定钙
诚信做人;数据真实;分析合理;富于创新

1
诚信做人;数据真实;分析合理;富于创新

诚信做人;数据真实;分析合理;富于创新

诚信做人;数据真实;分析合理;富于创新


诚信做人;数据真实;分析合理;富于创新
第二篇:分析化学实验 铵盐中氮含量的测定实验报告
实 验 报 告
姓名: 班级: 同组人:
项目 铵盐中氮含量的测定 课程: 分析化学 学号:
一、实验目的
1、掌握酸碱滴定法测定碱度的原理和方法。
2、学习用邻苯二甲酸氢钾标定氢氧化钠的方法。
3、了解甲醛法测定氮含量的原理。
4、了解酸碱滴定的实际应用。
二、实验原理
氢氧化钠标准溶液和盐酸标准溶液一样,只能用间接法配配制,其浓度的确定也可以用基准物质来标定。常用的有草酸和邻苯二甲酸氢钾等。本实验采用邻苯二甲酸氢钾,它与氢氧化钠的反应为:
达到化学计量点时,溶液呈弱碱性,可用酚酞作指示剂。
铵盐中氮含量的测定有蒸馏法和甲醛法两种,用甲醛法测定时,应用的是酸碱滴定中的间接滴定方法。
甲醛与铵盐作用后,可生成等物质的量的酸,例如:
2(NH4)2SO4+6HCH O=(CH2)6 N4+2H2SO4+6H2O
反应生成的酸可用氢氧化钠标准溶液滴定,由于生成的另一种产物六次甲基四胺(CH2)6 N4是一个很弱的碱,化学计量点时PH约为8.8,因此用酚酞作指示剂。
w(N)= C(NaOH)×V(NaOH)×14.01/1000/ m [(NH4)2SO4] ×100%
式中质量单位为g,体积单位为mL,浓度单位为moI/L。
三、仪器和药品
仪器:电子天平(3个)、称量瓶(3个)、50mL碱式滴定管(1个)、250mL锥形瓶(3个)250mL容量瓶(1个)、5mL刻度吸管(1个)。
药品:0.1moL/L NaOH溶液、邻苯二甲酸氢钾、酚酞指示剂、硫酸铵试样、40%中性甲醛溶液等 。
四、内容及步骤
准确称取纯净邻苯二甲酸氢钾一份,重约为3-3.5g,称至小数点后四位,置于小烧杯中,蒸馏水使之溶解、定容成250mL。用25mL移液管准确移取此溶液三份,分别置于250mL锥形瓶中,再滴入酚酞指示剂2滴,用欲标定的0.1moL/L NaOH溶液滴定至恰好呈红色,在30秒内不褪色为止。记录数据,计算氢氧化钠溶液的准确浓度。
准确称取0.12-0.15g左右的硫酸铵试样三份,分别置于锥形瓶中,加入40mL蒸馏水使之溶解,再加4mL甲醛中性水溶液,再滴入酚酞指示剂1-2滴,充分摇匀后静置1分钟,使反应完全,最后用0.1moL/L NaOH标准溶液滴定至粉红色。在30秒内不褪色为止。记录数据,计算硫酸铵中氮的含量。
五、实验数据记录及计算
实验数据记录(一)

实验数据记录(二)
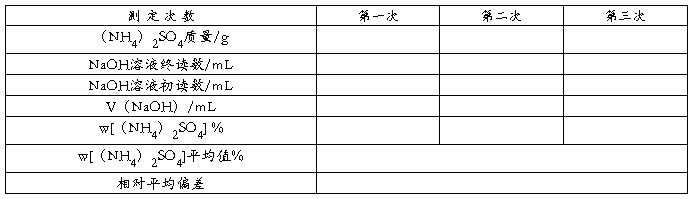
六、思考题:
1、用HCl滴定NaOH标准溶液时是否可用酚酞作指示剂?
2、为什么要排出滴定管空气泡?如何排出?
3、为什么分别将两滴定管调节至0.00mL刻度,或零点稍下处?
教师评语: 年 月 日
-
分析化学实验报告
分析化学实验报告20xx0218200858分类理工类标签字号大中小订阅盐酸和氢氧化钠标准溶液的配制和标定时间12月15号指导老师…
-
分析化学实验报告(武汉大学第五版)
分析化学实验报告陈峻贵州大学矿业学院贵州花溪550025摘要熟悉电子天平的原理和使用规则同时可以学习电子天平的基本操作和常用称量方…
-
分析化学实验报告
级名分析化学实验报吉林农业大学告班姓同组人实验酸碱标准溶液的配制和比较滴定实验目的实验原理实验步骤1酸碱标准溶液的配制101mol…
-
分析化学实验报告样本
实验名称游标卡尺的使用实验目的1掌握游标卡尺的使用方法2了解游标卡尺的结构原理3学习数据处理的相关内容4养成良好的写实验报告的习惯…
-
分析化学实验报告本模版
分析化学实验报告实验一电子分析天平的操作及称量练习学院专业班级姓名学号实验日期年月日教师评定实验目的掌握电子分析天平的基本操作和粉…
-
大学生物化学实验报告标准格式汇总
生物化学实验报告班级姓名实验一血清蛋白质醋酸纤维薄膜电泳目的原理仪器组成操作与结果结果粘贴实验二酶的特异性目的原理操作与结果将以上…
- 大学化学实验报告格式
-
大学化学实验报告模板
物理化学实验报告院系班级学号姓名实验名称姓名日期成绩实验名称姓名日期成绩实验名称姓名日期成绩实验名称姓名日期成绩实验名称姓名日期成…
-
西安交通大大学 化学实验报告模板
西安交通大学化学实验报告第页共页课程实验日期年月日专业班号组别交报告日期年月日姓名学号报告退发订正重做同组者教师审批签字实验名称化…
-
福州大学实验室危险化学品安全检查报告
福州大学实验室危险化学品专项安全检查报告为了认真贯彻教育部办公厅关于进一步加强高等学校实验室危险化学品安全管理工作的通知教技厅20…
-
分析化学实验报告七
硫酸铜中铜含量的测定摘要:利用间接碘量法测定铜离子的含量。旨在掌握硫代硫酸钠溶液的配制和保存,并掌标定握硫代硫酸钠溶液浓度的原理和…