大学物理热力学论文
由麦克斯韦速率分布律推出平动动能分布律
况勋朋(2013071034)
成都信息工程学院
控制工程学院(测控技术与仪器)
大学物理论文
由麦克斯韦速率分布律推出平动动能分布律
摘要:麦克斯韦首先把统计学的方法引入分子动理论,首先从理论上导出了气体分子的速率分布率,现根据麦克斯韦速率分布函数,求出相应的气体分子平动动能分布律,并导出与麦克斯韦分布函数类似的一些性质,求出平动动能的最概然值及平均值。并比较相似点和不同点。
前言:麦克斯韦把统计方法引入了分子动理论,首先从理论上导出了气体分子的速分分布律。这是对于大量气体分子才有的统计规律。现做进一步研究,根据其成果麦克斯韦速率分布函数,导出相应的平动动能分布律,并导出与麦克斯韦分布函数类似的一些性质并求出平动动能的最概然值及平均值,并且由此验证其正确性。
方法:采用类比的方法,用同样的思维,在麦克斯韦速率分布函数的基础上,作进一步研究,导出能反映平均动能在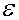 附近的单位动能区间内的分子数与总分子数的比的函数
附近的单位动能区间内的分子数与总分子数的比的函数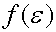 的表达式。并由此进一步推出与麦克斯韦分布函数相对应的一些性质,并比较分析一些不同点。
的表达式。并由此进一步推出与麦克斯韦分布函数相对应的一些性质,并比较分析一些不同点。
麦克斯韦速率分布律
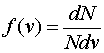
这个函数称为气体分子的速率分布函数麦克斯韦进一步指出,在平衡态下,分子速率分布函数可以具体地写为
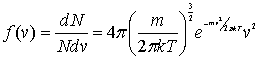
式中T是气体系统的热力学温度,k是玻耳兹曼常量,m是单个分子的质量。式(8-30)称为麦克斯韦速率分布律。 图像如下
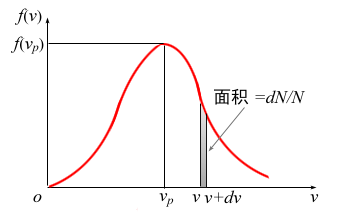
图1 麦克斯韦速率分布函数
图1画出了f (v)与v的关系曲线,这条曲线称为速率分布曲线。由图可见,曲线从坐标原点出--发,随着速率的增大,分布函数迅速到达一极大值,然后很快减小,随速率延伸到无限大,分布函数逐渐趋于零。速率在从v1到v2之间的分子数比率DN/N,等于曲线下从v1到v2之间的面积, 如图中阴影部分所示。显然,因为所有N个分子的速率必然处于从0到 ¥之间,也就是在速率间隔从0到 ¥的范围内的分子数占分子总数的比率为1,即
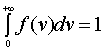
这是分布函数f (v)必须满足的条件,称为归一化条件。
而 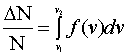
表示在平衡态下,理想气体分子速率在v1到v2 区间的分子数占总分子数的比率。
而应用麦克斯韦速率分布函数可以求出气体分子三个重要的速率:
(1)最概然速率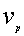 ,f(v)的极大值所对应的速率
,f(v)的极大值所对应的速率 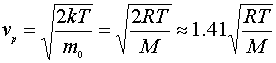
其物理意义为:在平衡态的条件下,理想气体分子速率分布在附近的单位速率的分布区间内的分子数占气体总分子的百分率最大。
(2) 平均速率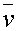 ,用于研究分子碰撞
,用于研究分子碰撞
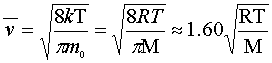
(3) 方均根速率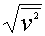 ,用于研究分子平均平动动能,
,用于研究分子平均平动动能,
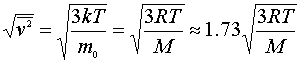
反映的是大量分子无规则运动速率的二次方的平均值的二次方根称为方均根速率。
推导及演绎:
由于分子的平动动能可表示为 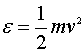
两边同时取微分有 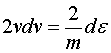
带入到麦克斯韦速率函数有
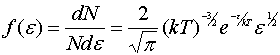
现定义为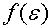 为气体分子的平动动能的分布函数。
为气体分子的平动动能的分布函数。
平动动能在从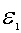 到
到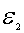 之间的分子数比率DN/N,等于曲线下从
之间的分子数比率DN/N,等于曲线下从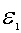 到
到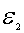 之间的面积, 如图中阴影部分所示。显然,因为所有N个分子的速率必然处于从0到 ¥之间,也就是在速率间隔从0到 ¥的范围内的分子数占分子总数的比率为1,
之间的面积, 如图中阴影部分所示。显然,因为所有N个分子的速率必然处于从0到 ¥之间,也就是在速率间隔从0到 ¥的范围内的分子数占分子总数的比率为1,
即 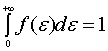
这说明和麦克斯韦分布率相似平动动能分布函数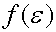 同样必须满足归一化条件。
同样必须满足归一化条件。
而 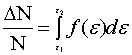 表示在平衡态下,理想气体分子速率在
表示在平衡态下,理想气体分子速率在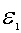 到
到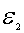 区间的分子数占总分子数的比率。
区间的分子数占总分子数的比率。
同样我们也可以根据平动动能分布函数求出最概然平动动能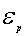 以及平均平动动能
以及平均平动动能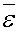
(1)粒子的最概然平动动能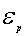
同样地,最概然平动动能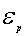 也是对应着
也是对应着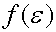 的极值
的极值
由 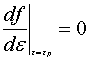
化简 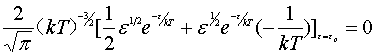
解出 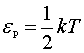
而其所对应的速率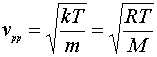
由此我们看到,最概然平动动能所对应的速率并不是麦克斯韦速率所求得的最概然速率。初看起来似乎很奇怪,可仔细想想,最概然速率代表的是速率分布在附近的单位速率的分布区间内的分子数占气体总分子的百分率最大时的速率。而最平动动能的概然值代表的是平动动能分布在附近的单位动能的分布区间内的分子数占气体总分子的百分率最大时的动能,其对应的速率却不是最该然速率。而计算发现这是其实是由于两个方程求极大值时对应的导函数不同。很显然求的的极大值也不同。
(2)粒子的平均平动动能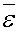
同样的,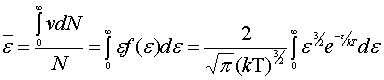
其中因为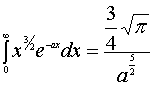
所以 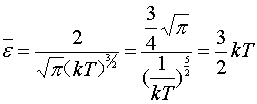
这个结果是显然的:有麦克斯韦分布律已经得到,这也证明了上面的推导的正确性。
总结:通过以上的讨论和分析,我们不仅进一步了解了麦克斯韦速率分布函数,及其结论,还能挖掘出衍生出来的气体平动动能的分布情况,这样我们会对气体动理论的本质有跟家深刻的理解。
引文:要善于在前人已有的基础之上做进一步试探性的研究,才能衍生出新的知识点,也能有助于深刻的理解原有的知识。
第二篇:大学物理热力学论文1
由麦克斯韦速率分布律推出平动动能分布律
麦克斯韦首先把统计学的方法引入分子动理论,首先从理论上导出了气体分子的速率分布率,现根据麦克斯韦速率分布函数,求出相应的气体分子平动动能分布律,并导出与麦克斯韦分布函数类似的一些性质,求出平动动能的最概然值及平均值。并比较相似点和不同点。
麦克斯韦把统计方法引入了分子动理论,首先从理论上导出了气体分子的速分分布律。这是对于大量气体分子才有的统计规律。现做进一步研究,根据其成果麦克斯韦速率分布函数,导出相应的平动动能分布律,并导出与麦克斯韦分布函数类似的一些性质并求出平动动能的最概然值及平均值,并且由此验证其正确性。
方法:采用类比的方法,用同样的思维,在麦克斯韦速率分布函数的基础上,作进一步研究,导出能反映平均动能在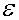 附近的单位动能区间内的分子数与总分子数的比的函数
附近的单位动能区间内的分子数与总分子数的比的函数 的表达式。并由此进一步推出与麦克斯韦分布函数相对应的一些性质,并比较分析一些不同点。
的表达式。并由此进一步推出与麦克斯韦分布函数相对应的一些性质,并比较分析一些不同点。
麦克斯韦速率分布律

这个函数称为气体分子的速率分布函数麦克斯韦进一步指出,在平衡态下,分子速率分布函数可以具体地写为
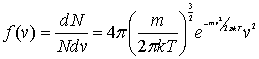
式中T是气体系统的热力学温度,k是玻耳兹曼常量,m是单个分子的质量。式(8-30)称为麦克斯韦速率分布律。 图像如下
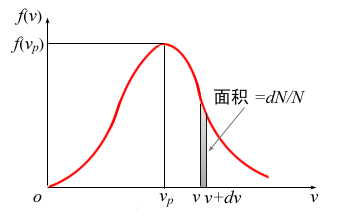
图1 麦克斯韦速率分布函数
图1画出了f (v)与v的关系曲线,这条曲线称为速率分布曲线。由图可见,曲线从坐标原点出--发,随着速率的增大,分布函数迅速到达一极大值,然后很快减小,随速率延伸到无限大,分布函数逐渐趋于零。速率在从v1到v2之间的分子数比率?N/N,等于曲线下从v1到v2之间的面积, 如图中阴影部分所示。显然,因为所有N个分子的速率必然处于从0到 ?之间,也就是在速率间隔从0到 ?的范围内的分子数占分子总数的比率为1,即
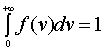
这是分布函数f (v)必须满足的条件,称为归一化条件。
而 
表示在平衡态下,理想气体分子速率在v1到v2 区间的分子数占总分子数的比率。
而应用麦克斯韦速率分布函数可以求出气体分子三个重要的速率:
(1)最概然速率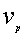 ,f(v)的极大值所对应的速率
,f(v)的极大值所对应的速率 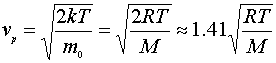
其物理意义为:在平衡态的条件下,理想气体分子速率分布在附近的单位速率的分布区间内的分子数占气体总分子的百分率最大。
(2) 平均速率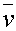 ,用于研究分子碰撞
,用于研究分子碰撞
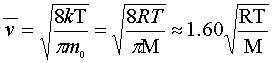
(3) 方均根速率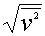 ,用于研究分子平均平动动能,
,用于研究分子平均平动动能,
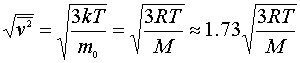
反映的是大量分子无规则运动速率的二次方的平均值的二次方根称为方均根速率。
推导及演绎:
由于分子的平动动能可表示为 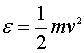
两边同时取微分有 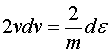
带入到麦克斯韦速率函数有
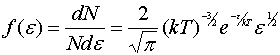
现定义为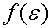 为气体分子的平动动能的分布函数。
为气体分子的平动动能的分布函数。
平动动能在从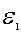 到
到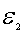 之间的分子数比率?N/N,等于曲线下从
之间的分子数比率?N/N,等于曲线下从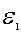 到
到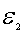 之间的面积, 如图中阴影部分所示。显然,因为所有N个分子的速率必然处于从0到 ?之间,也就是在速率间隔从0到 ?的范围内的分子数占分子总数的比率为1,
之间的面积, 如图中阴影部分所示。显然,因为所有N个分子的速率必然处于从0到 ?之间,也就是在速率间隔从0到 ?的范围内的分子数占分子总数的比率为1,
即 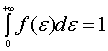
这说明和麦克斯韦分布率相似平动动能分布函数 同样必须满足归一化条件。
同样必须满足归一化条件。
而  表示在平衡态下,理想气体分子速率在
表示在平衡态下,理想气体分子速率在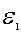 到
到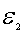 区间的分子数占总分子数的比率。
区间的分子数占总分子数的比率。
同样我们也可以根据平动动能分布函数求出最概然平动动能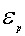 以及平均平动动能
以及平均平动动能
(1)粒子的最概然平动动能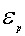
同样地,最概然平动动能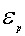 也是对应着
也是对应着 的极值
的极值
由 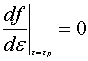
化简 
解出 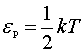
而其所对应的速率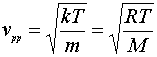
由此我们看到,最概然平动动能所对应的速率并不是麦克斯韦速率所求得的最概然速率。初看起来似乎很奇怪,可仔细想想,最概然速率代表的是速率分布在附近的单位速率的分布区间内的分子数占气体总分子的百分率最大时的速率。而最平动动能的概然值代表的是平动动能分布在附近的单位动能的分布区间内的分子数占气体总分子的百分率最大时的动能,其对应的速率却不是最该然速率。而计算发现这是其实是由于两个方程求极大值时对应的导函数不同。很显然求的的极大值也不同。
(2)粒子的平均平动动能
同样的,
其中因为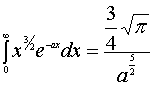
所以 
这个结果是显然的:有麦克斯韦分布律已经得到,这也证明了上面的推导的正确性。
总结:通过以上的讨论和分析,我们不仅进一步了解了麦克斯韦速率分布函数,及其结论,还能挖掘出衍生出来的气体平动动能的分布情况,这样我们会对气体动理论的本质有跟家深刻的理解。
-
大学物理论文
大学物理论文参考题目:1.惯性质量与引力质量相等的实验验证。2.谈谈伽利略的相对性原理。3.惯性系与非惯性系中物理学规律之间联系的…
-
大学物理论文
牛158xxxxxxxx关于经典力学的论述专业:土木工程091班学号:5601109053学生姓名:丁筛筛指导教师:余天宝目录I.…
-
大学物理论文
题目:《论大学物理》作者:经济262121802150孙榕摘要:本文从一个大学生的视角来看待大学物理学习对经济与金融专业的影响,并…
-
大学物理课程论文1
大学物理课程论文大学物理课程与电子信息工程专业的关系及大学物理的重要性作者学校专业电子信息工程班级电信114班学号指导教师日期大学…
-
【大学物理实验论文格式范例】
金属铝的热导率的测量班级机111姓名XXX学号3111111111在做大学物理实验稳态法测量不良导体的热导率时老师提问是否可以用稳…
-
大学物理课程总结
在大二上学期,我们学习了大学物理这门课程,物理学是一切自然科学的基础,处于诸多自然科学学科的核心地位,物理学研究的粒子和原子构成了…
-
大学物理热学题库
练习四热学一、填空题1.质量为M,摩尔质量为Mmol,分子数密度为n的理想气体,处于平衡态时,状态方程为___pV?M状态方程的另…
-
大学物理热学试题
热学(四)循环过程热二律专业班级学号姓名一、选择题1、一定量的某种理想气体起始温度为T,体积为V,该气体在下面循环过程中经过三个平…
-
大学物理热学读书心得
读《关于直接利用地球大气层中的热和冷的设想》有感作为工业革命标志的蒸汽机的发明将热的应用提到了一个新的高度。其中,热的获取的来源为…
-
0zxmqk大学物理热力学论文
-+懒惰是很奇怪的东西,它使你以为那是安逸,是休息,是福气;但实际上它所给你的是无聊,是倦怠,是消沉;它剥夺你对前途的希望,割断你…