20xx年高三化学教学总结
20xx年高三化学教学总结
莫毅娟
本学年,我担任高三(9)班、高三(10)班的化学教学,根据一年以来的高考备考,我总结如下:
1、以长远的目光看三年,高考备考应该从高一开始规划,以3年为一个轮回。要打好学生的基础,必须从高一开始,高一的教学重抓高考中常常考的知识点,平时练习或试卷中,让高一学生见识高考题或高考改编题,以便让学生心中对高考有所了解。
2、高三复习应该从高二第二学期的最后一个月开始。曾记得高二下学期最后一个月,我们已经把高二选修5《有机化学》上完,但东莞教育局统一进行期末考试,考试的范围包括选修4《化学反应原理》和选修5《有机化学》。为了学生考好期末考试,我们用2周时间来复习高二上学期学过选修4《化学反应原理》,时间匆忙,加上学生已经一个学期没有复习这本书了,可以想象学生复习的效果如何,这样导致了我们既没有把刚学完《有机化学》复习好,同时也草草复习了《化学反应原理》。如果当时我们明智的用1个月进行《有机化学》的复习和提升的话,相应高三每次的周测和月考我们都有意识的出高考题型有机题,这将为高考有机题特别是30题大题(16分)做好长达一年的充分复习时间,这也将为我们高三总复习《有机化学》专题复习赢回时间和效果,绝对有利于提高学生平均分。
3、把握好选择题复习难道,以免浪费复习时间和误导学生。根据20xx年-20xx年广东省理综高考卷化学选择题,6道单选题和2道双选题,分值共36分,难道不大,大多数学生可以做对5-6题,好的学生可以全对。选择题主要存在的难度是双选题,学生答对率还不够理想。为此,高考备考复习中,根据20xx年-20xx年广东省各市的模拟题,有必要对8道选择题知识点进行专题式的强化训练,同
时再通过周二的选择题测试和周日的全卷测试进一步强化和提高选择题的得分率。
4、大题是我们学生的弱项,依据高考4道大题的知识点分布,计划好3轮的大题复习。第一轮基础复习(高三补课开始至高三上学期期末统考);第二轮专题复习(高三上学期寒假补课至高三下学期广州一模之前);第三轮复习复习(继续强化,查漏补缺,回归课本)。根据大题难度,我们学校的学生比较容易拿到分数的是30题(有机题)、31题(速率和平衡、化学反应和能量),难拿分的是32(题化工)、33题(实验)。为此,重点复习和训练学生大题是非常有必要的,熟能生巧,多做题,从而提高学生知识的运用能力和应变能力。
5、抓临界生,提高班级平均分。对于我们学校而异,优生相对而言是很少的,要提高平均分,主要靠2B和3A的学生,为此,我扩大临界生的面,对成绩位于班名前30位学生进行临界生套题测试(每周一次),利用晚修前18:00-18:50(50分钟)强化训练套题,测试完后及时批阅学生的测试卷,重点对2B学生存在的问题,有针对性进行个人辅导,随着测试次数增加,我发现学生答题速度和答题得分都有普遍提高,使学生学习化学的信心和积极性有了明显提高,这样使整个班级的高分和平均分能够保持平稳。
第二篇:20xx高三化学教学总结
20##高三化学教学总结
赵雪梅
高三化学总复习是中学化学学习非常重要的时期,也是巩固基础、优化思维、提高能力的重要阶段,高三化学总复习的效果将直接影响高考成绩。为了今后更好的工作我把本学期的教学总结一下。
一、研究信息,看准方向
怎样着手进行化学总复习,复习的目的和任务是什么?这是刚刚进入高三的同学所面临的第一个问题,也是教师在高三化学教学过程中所面临的第一个问题。要解决好这个问题,就必须对一些信息进行研究,从中领会出潜在的导向作用,看准复习方向,为完成复习任务奠定基础。
1.研究高考化学试题。纵观每年的高考化学试题,可以发现其突出的特点之一是它的连续性和稳定性,始终保持稳中有变的原则。只要根据近几年来海南的高考试题,就能发现它们的一些共同特点,如试卷的结构、试题类型、考查的方式和能力要求等,从而理清复习的思路,制定相应的复习计划。
2.关注新教材和新课程标准的变化。熟悉新教材和新课程标准的变化,将有利于把握复习的方向和深难度,有利于增强复习的目的性。
3.熟悉考试说明。考试说明(即考纲)是高考的依据,是化学复习的“总纲”,不仅要读,而且要深入研究,以便明确高考的命题指导思想、考查内容、试题类型、深难度和比例以及考查能力的层次要求等。不仅如此,在整个复习过程中要不断阅读,进一步增强目的性,随时调整复习的方向。
二、抓纲务本,摆正关系
进入高三化学教学,很容易走进总复习的怪圈:“迷恋”复习资料,陷入“题海”。虽然投入了大量的时间和精力,但收效甚微,效果不佳。对此,高三化学教学过程中必须保持清醒的头脑,努力处理好下面几种关系。
1.教材和复习资料的关系。教材是化学总复习的根本,它的作用是任何资料都无法替代的。在化学总复习中的抓纲务本就是指复习以考试说明作指导,以教材为主体,通过复习,使中学化学知识系统化、结构化、网络化,并在教材基础上进行拓宽和加深,而复习资料的作用则是为这种目的服务,决不能本末倒置,以复习资料代替教材。通常的做法是精选一套复习资料(一般是教师指定)作为主要参考书,供整理知识、练习使用,在复习的过程中应随时回归教材,找到知识在教材中的落脚点和延伸点,不断完善和深化中学化学知识。
2.重视基础和培养能力的关系。基础和能力是相辅相成的,没有基础,能力就缺少了扎根的土壤。通常中学化学知识和技能分成五大块:化学基本概念和基本理论、元素及其化合物、有机化学、化学实验和化学计算。如对化学概念、理论的复习,要弄清实质和应用范围,对重点知识如物质的组成、结构、性质、变化等要反复记忆不断深化,对元素及其化合物等规律性较强的知识,则应在化学理论的指导下,进行总结、归纳,使中学化学知识和技能结构化、规律化,从而做到在需要时易于联系和提取应用。同时注意规范化学用语的使用(如化学反应方程式、离子方程式、电极反应式、电离方程式以及化学式、结构式、电子式等),规范语言文字的表达能力,力争使基础知识和技能一一过手。
3.练习量和复习效率的关系。练习是化学总复习的重要组成部分,是运用知识解决问题的再学习、再认识过程,也是促进知识迁移、训练思维、提高分析问题和解决问题能力的重要途径,但练习量必须合理,以保证质量为前提,避免简单的机械重复和陷入“题海”。通过练习要达到强化记忆、熟练地掌握知识、找出存在的问题、弥补薄弱环节、扩大知识的应用范围和提高能力的目的,从而提高复习效率。
三、多思善想,提高能力
化学总复习的范围是有限的,要想在有限的时间里达到最佳复习效果,只能采用科学的方法,在教师的教学中、学生的学习过程中都必须开动脑筋,多思善想。在化学教学过程中采用分层教学,有平时的正常面上的教学,有优秀生的提高,和学习有困难学生的加强基础等不同的形式。
1.精读教材,字斟句酌。
系统复习,自始至终都应以教材为本,注意知识的全面性、重点性、精确性、联系性和应用性。对中学(初、高中)化学知识和技能都要一一复习到位;对教材中的关键性知识(我们常说的考点),进行反复阅读、深刻理解,以点带面形成知识结构;对化学知识的理解、使用和描述要科学、准确和全面,如规范地使用化学用语,正确、全面地表达实验现象和操作要点等(尤其适合中等以下的学生,利用年级组统一安排的基础加强课时间);对知识点之间的相互关系及其前因后果。如与离子反应有关的知识有离子反应方程式的书写和正误判断、离子共存问题、离子浓度大小比较、离子的检验和推断、溶液的导电性变化等。应用性是指通过复习要学会运用知识解决实际问题的方法,如元素周期律、周期表涵盖的内容相当丰富,可以进行元素位、构、性相互推断,预测未知元素的性质,比较各种性质的强弱等。
2.学会反思,提高能力。
能力的培养是化学总复习的另一个重要任务,它通常包括观察能力、思维能力、实验能力和计算能力,其中思维能力是能力的核心。要善于从学生的实际出发,有针对性地进行知识复习和解题训练,而不是做完练习题简单地对对答案就万事大吉了,而是进一步思考:该题考查了什么内容,其本质特征是什么,还有其他更好的解法吗?对典型习题、代表性习题更要多下功夫,不仅一题一得,更要一题多得,既能促使知识得到不断地弥补、完善,又能举一反三,从方法上领会解题过程中的审题、破题、答题的方式和奥秘等,以此培养良好的思维品质。
四、端正心态,培养素质
健康向上、勇于进取、自信自强的积极心态是搞好复习的重要保证,也是高考成功的关键。而积极的心态有赖于平时的不断调整和锤炼。
1.正确对待考试。在高三复习过程中,考试是频繁的。平时的每一次考试都是练兵的绝好机会,都能够暴露学生存在的问题,有利于在后续复习中进行针对性的查漏补缺,总结经验教训,以便学生在高考中不犯错误或少犯错误,所以既不能因一时失误或遇到困难而气馁,也不能因成绩进步而沾沾自喜。
2.合理安排学习的时间。指导学生要动静结合,既要勤奋学习,也要学会放松、休息、锻炼,只有劳逸结合、生活得有规律,才能轻松自如地渡过难关。
3.创设良好的学习心理环境。在化学教学过程中要使学生正确地认识自己,从自己的基础和实际出发,扎扎实实地复习;愉快地接纳自己,充分肯定自己的进步,找出存在的问题及时弥补;自觉地控制自己,以明确的目标、良好的意志力调节自己,变压力为动力,全面提高自己的素质。
五、存在的不足和问题
1、我是首次使用新教材,对教材的把握和知识内容体系的“度”的控制,以及教学进度的掌握均存在一定的缺憾。
2、练习的训练量还是多了些,由于招生的原因,基础差的学生多,教学进度总是滞后,要做到段段清,节节过关就显得前宽后紧的局面。
总之,化学总复习要为高考做好知识准备和精神准备,要有目标、有计划、讲究方法、注重落实,千方百计地提高化学总复习的效益。我们高三化学备课组始终坚守原则,争取在高考中取得好成绩
第三周
20##年5月20日
物理:
1.(15分)一质量为 的平顶小车,以速度
的平顶小车,以速度 沿水平的光滑轨道作匀速直线运动。现将一质量为
沿水平的光滑轨道作匀速直线运动。现将一质量为 的小物块无初速地放置在车顶前缘。已知物块和车顶之间的动摩擦系数为
的小物块无初速地放置在车顶前缘。已知物块和车顶之间的动摩擦系数为 。
。
1. 若要求物块不会从车顶后缘掉下,则该车顶最少要多长?
2. 若车顶长度符合1问中的要求,整个过程中摩擦力共做了多少功?
化学:
1.V L Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为( )。
A. mol/L
mol/L  B.
B. mol/L
mol/L
C. mol
mol /L D.
/L D. mol/L
mol/L
2.下列说法中错误的是( )。
A.从1L 1mol·L-1的NaCl溶液中取出10mL,其浓度仍是1mol·L-1
B.制成0.5L 10mol·L-1的盐酸,需要氯化氢气体112L(标准状况)
C.0.5L 2mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D.10g 98%硫酸(密度为1.84g·cm-3)与10mL 18.4mol·L-1硫酸的浓度是不同的
3.在aL Al2(SO4)3和(NH4)2SO4的混合溶液中加入bmol BaCl2,恰好使溶液中的SO42-离子完全沉淀:如加入足量强碱并加热可得到cmol NH3气,则原溶液中的Al3+离子浓度(mol/L)为( )。
A. B.
B. C.
C. D.
D.
4.标准状况下,将VL A气体(摩尔质量为M g·mol-1)溶于0.1L水中,所得溶液密度为ρg·mL-1。则此溶液物质的量浓度为( )。
A. mol·L-1 B.
mol·L-1 B.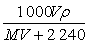 mol·L-1
mol·L-1
C. mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1
5.若NA表示阿佛加德罗常数,下列说法正确的是 ( )
A.1 mol Cl2作为氧化剂得到的电子数为NA
B.在0℃,101kPa时,22.4L氢气中含有NA个氢原子
C.14g氮气中含有7NA个电子
D.NA个一氧化碳分子和0.5 mol 甲烷的质量比为7︰4
6.用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA
B.标准状况下,22.4 L己烷中共价键数目为19NA
C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
D.1 L浓度为1 mol·L-1的Na2CO3溶液中含有NA个CO32-
7.用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
 A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
 B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
 C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
 D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
8.相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是 ( )
A.Al B.Al(OH)3 C.AlCl3 D.Al2O3
“绿色奥运”
最有可能考的“2008中国奥运”相关选择题及答案
1、下列措施符合“绿色奥运”这一主题的是:①多使用电动汽车;②工业和生活污水处理后排放;③推广使用无铅汽油;④市区禁止机动车通行;⑤奥运村禁止使用高分子材料。
A.①②③④⑤ B.②④⑤ C.①②③ D. ①④⑤
2、为实现“绿色奥运”,下列环保建议中,你认为不能采纳的是
A.开发、使用无磷洗涤剂
B.用天然气代替汽油和柴油作发动机燃料
C.禁止未经处理的工业废水和生活污水的任意排放
D.使用添加剂抑制水中所有动植物的生长
3、2008夏季奥运会将在我国举行,这次奥运会要突出“绿色奥运、科技奥运、人文奥运”的理念,其中“绿色奥运”是指
A.把环境保护作为奥运设施规划和建设的首要条件
B.严禁使用兴奋剂,使运动员公平竞争
C.所有奥运用品全都是绿色的
D.奥运场馆建设均使用天然材料,不使用合成材料
4、为“绿色奥运”某同学提出了下列环保建议,其中你认为可以采纳的是
① 用气态燃料代替液态和固态燃料作为发动机动力来源;
② 开发生产无汞电池;
③ 提倡使用一次性发泡塑料餐具和塑料袋;
④ 分类回收垃圾;
⑤ 开发无磷洗涤剂;
⑥ 提倡使用手帕,减少餐巾纸的使用
A.①②③④ B.②③④⑤ C.①②④⑤⑥ D.全部
5、即将在北京举行的20##年奥运会提出了“科技奥运、人文奥运、绿色奥运”的口号。为了将北京奥运会办成绿色奥运会,下列做法不可取的是
① 因为油价上涨,所以使用价格较低的含铅汽油
② 开发新能源,减少矿物燃料的燃烧
③ 关闭所有的化工企业
④ 提倡使用一次性发泡塑料餐具和塑料袋
⑤ 开发、生产无汞电池
⑥ 机动车安装尾气净化器
⑦ 为了体现人民生活水平的提高,提倡每个家庭都买小汽车
A.①②③ B.①③④⑦ C.①②④⑤⑥ D.全部
6、针对20##年的奥运会,我国政府提出要承办“绿色奥运”。那么,“绿色化学”在化学工业生产中是指
A. 废水、废气、废渣进行严格的处理,不得排放
B. 减少和消除对环境的污染
C. 在化工厂周围种绿色植物
D. 以绿色植物为原料,用生物催化剂进行化工生产,且原子利用率达到100%
7、“绿色奥运”是2008北京奥运会的主题之一。为减轻污染,北京为汽车加装了“三效催化净化器”,可将尾气中的一氧化碳、一氧化氮转化为参与大气循环的无毒混合气体,该气体是
A、二氧化碳和氮气
B、二氧化碳和二氧化氮
C、二氧化碳和氧气
D、二氧化碳和氮气和氧气
8、20##年在北京举行的奥运会提出了“科技奥运、人文奥运、绿色奥运”的口号。为了使北京奥运会办成绿色奥运会,下列做法正确的是
①开发新能源,减少矿物燃料的燃烧
②关闭所有的化工企业
③禁止使用超簿塑料购物袋
④开发、生产无汞电池
⑤机动车安装尾气净化器
A.①②③④ B.②③④⑤ C.①③④⑤ D.①②③⑤
“水 立 方”
1、2008 年北京奥运场馆中,国家游泳中心的外墙体可以使用15至20年仍保持完好如初。这是我国第一个采用ETFE[聚氟乙烯(C2H2F2)n]塑料膜作为立面维护建筑体系的材料。下列关于ETFE的判断正确的是
A.它是易降解的新型塑料,不会形成白色污染
B.它是使常规建筑材料保持整洁美观的保护层
C.它的组成中含有碳分子、氢分子和氟分子
D.它属于天然有机高分子材料
2、美丽的“水立方”(Water Cube)是北京奥运会游泳馆。设计灵感来自于有机细胞的天然图案以及肥皂泡的形成。在这个中心的蓝色气泡墙之内,钢结构的基本单位是一个由12个正五边形和2个正六边形所组成的几何细胞。覆盖这个框架的是半透明的气泡,称为PTFE膜(聚四氟乙烯),它能为场馆带来更多的自然光。下列说法不正确的是
A. PTFE可以使溴水褪色
B. PTFE是通过加聚反应合成的
C. PTFE的单体是CF2=CF2
D. PTFE化学稳定性、耐磨性良好
3、美丽的 “水立方”是北京奥运会游泳馆,设计灵感来自于有机细胞的天然图案以及肥皂泡的形成。在这个中心的蓝色泡墙之内,钢结构的基本单位是一个由12个正五边形和2个正六边形组成的几何细胞,覆盖这个框架的是半透明的“气泡”,称为ETFE,该材料为四氟乙烯(CF2=CF2)与乙烯的共聚物,它能为场馆内带来更多的自然光。根据以上信息,下列说法不正确的是
A.若设想将一个结构单元用钢棍焊成足球形状“碳笼”,它与C24形状相似
B.若设想将一个结构单元用钢棍焊成足球形状“碳笼”,需钢棍(相当于键)36根
C.ETFE在空气中易被氧气氧化
D.四氟乙烯中既含有极性键又含有非极性键
4、将用于20##年北京奥运会的国家游泳中心(水立方)采用了高分子膜材料“ETFE”,该材料是四氟乙烯(CF2=CF2)与乙烯(CH2=CH2)发生聚合反应得到的高分子材料。下列说法不正确的是
A.“ETFE”分子中可能存在“—CH2—CH2—CF2—CF2”的连接方法
B.合成“ETFE”的反应为加聚反应
C.CF2=CF2和CH2=CH2均是平面型分子
D.CF2=CF2可由CH3CH3与F2两种物质直接反应制得
5、将用于20##年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成全氟乙丙烯。下列说法错误的是
A.ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式
B.合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应
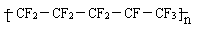 C.聚全氟乙丙烯分子的结构简式可能为
C.聚全氟乙丙烯分子的结构简式可能为
D.四氟乙烯中既含有极性键又含有非极性键
6、20##年北京奥运标志性场馆之一——国家游泳中心(水立方)已建成,其独特的膜水泡结构令人耳目一新。该膜材料为ETFE塑料(聚四氟乙烯-乙烯共聚物),具有环保节能、自洁能力强等特点。下列有关ETFE的说法正确的是
A、 可以与氢气发生加成反应
B、 其单体都是烯烃
C、是一种合成高分子材料
D、是纯净物,有固定的熔点
7、20##年北京奥运会主体育场鸟巢形建筑和毗邻的游泳馆的“水立方”是在国内首次采用的膜结构建筑,以钢材为支架,覆盖ETFE薄膜。ETFE是乙烯和四氟乙烯的共聚物,是一种轻质透明的新材料。下列说法错误的是 ( )
A.ETFE是一种可焊接的塑料
B.ETFE极易分解,符合环保要求
C.ETFE韧性好拉伸强度高
D.ETFE比玻璃轻、安全
“火 炬”
1、自第十一届奥运会以来,开幕式都要举行隆重的火炬接力仪式。火炬的可燃物是丁烷 (化学式为C4H10),它燃烧时,火苗高且亮,即使在白天,二百米以外也能清晰可见。下列关于丁烷的叙述不正确的是
A丁烷由碳、氢两种元素组成
B丁烷由4个碳原子和10个氢原子构成
C丁烷中碳、氢元素的质量比是24∶5
D丁烷分子由碳原子和氢原子构成
2、20##年北京奥运会“祥云”火炬用的是环保型燃料——丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为2221.5 kJ/mol,下列有关说法正确的是
A.奥运火炬燃烧主要是将化学能转变为热能和光能
B.丙烷的沸点比正丁烷高
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为
C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H= -2221.5kJ/mol
3、20##年北京奥运会火炬以中国传统祥云符号和纸卷轴为创意,由铝合金制成,使用的燃料为丙烷。下列说法不正确的是
A.丙烷与甲烷互为同系物
B.丙烷燃烧是吸热反应
C.铝柄有一层致密的氧化膜可防止其腐蚀
D.火炬燃料用丙烷比用煤油更环保
4、20##年北京奥运会“祥云”火炬用的是环保型燃料——丙烷(C3H8),
悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,
下列有关说法正确的是
A.丙烷分子中三个碳原子共平面
B.符合通式CnH2n+2的物质均属于烷烃
C.丁烷的一氯代物有5种
D.以上说法均不正确
“鸟 巢”
1.2008 年北京奥运会主体育场的外形好似“鸟巢” ( The Bird Nest )。有一类硼烷也好似鸟巢,故称为巢式硼烷。巢式硼烷除 B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化。下图是三种巢式硼烷,有关说法正确的是
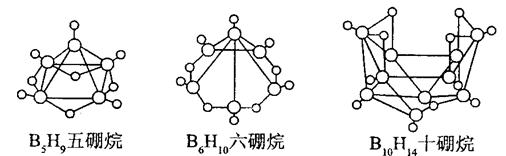
A.这类巢式硼烷的通式是 BnH n + 4
B.2B5H9 + 12O2 5B2O3 十9H2O ,l molB5H9完全燃烧转移25mol电子
5B2O3 十9H2O ,l molB5H9完全燃烧转移25mol电子
C.8 个硼原子的巢式棚烷化学式应为 B8H10
D.硼烷与水反应是非氧化还原反应
“福 娃”
1、20##年奥运吉祥物福娃外材为纯羊毛线,内充物为无毒的聚酯纤维下列说法正确的是
A.羊毛与聚酯纤维的化学成分相同
B.聚酯纤维和羊毛一定条件下均能水解
C.该聚酯纤维单体为对苯二甲酸和乙醇
D.由单体合成聚酯纤维的反应属加聚反应
2、制作奥运吉祥物福娃的外装饰材料为纯羊毛线,内充物材料为无毒的聚酯纤维,下列有关这二种材料描述正确的是
A 二者都是天然纤维
B 二者可通过灼烧进行鉴别
C 二者都是合成纤维
D 二者均有固定的熔点
3、下图是2008奥运吉祥物,其外材料为纯羊毛,内充聚酯纤维,该聚酯纤维的化学式为 (COC6H4COOCH2CH2O)n。下列说法中不正确的是

A.羊毛与聚酯纤维的化学成分不相同
B.由单体合成聚酯纤维的反应属加聚反应
C.该聚酯纤维单体为对苯二甲酸和乙二醇
D.聚酯纤维和羊毛一定条件下均能水解
“兴 奋 剂”
1、在20##年8月的雅典奥运会上个别运动员仍服用兴奋剂。可卡因是一种兴奋剂,其化学式为C17H21NO4.下列有关说法错误的是
A.长期服用兴奋剂会给身体造成很多危害
B.可卡因由C、H、N、O四种元素组成
C.可卡因分子中C、H、N、O的原子个数之比为17:21:1:4
D.可卡因分相对子分子质量的计算式为12+1+14+16
2、20##年的雅典奥运会上个别运动员使用了兴奋剂,而被奥委会严厉处罚。丙胺类药物是兴奋剂中的一类,有强烈兴奋中枢神经的作用,属于体育运动员的违禁药物。对于其中化学式为C9H13N的化合物兴奋剂,下列说法中,错误的是
A.由C、H、N三种元素组成
B.燃烧产物只有CO2和H2O
C.属于有机物
D.分子中C、H、N原子个数比是9﹕13﹕1
3、我国预计将20##年奥运会办成人文奥运、环保奥运、科技奥运。兴奋剂检测是奥运会对运动员的一项重要检验。其中一种兴奋剂的化学式为C20H26O2,下列关于该兴奋剂的说法正确的是 ( )
A.该兴奋剂属于氧化物
B.该兴奋剂是由多原子构成的化合物
C.该兴奋剂是由碳、氢、氧三个元素组成的
D.该兴奋剂中碳、氢、氧三种元素的质量比为l 20:13:16
4、“人文奥运、科技奥运、绿色奥运”是20##年北京奥运会的重要特征。其中禁止运动员使用兴奋剂是其重要举措之一。以下两种兴奋剂的结构分别为:


①利尿酸 ②兴奋剂X
则关于它们的说法中正确的是
A.它们遇FeCl3溶液均显紫色,均为芳香族化合物
B. 1 mol利尿酸分别与浓溴水和H2反应时最多消耗Br2 和H2分别为4 mol、7 mol
C.两种兴奋剂中滴入KMnO4(H+)溶液,观察紫色均会变浅
D.两种分子中的所有碳原子均不可能共平面
 5、“坚决反对运动员服用兴奋剂”是“人文奥运会” 的重要体现。某兴奋剂的结构简式如下图:下列有关它的说法正确的是( )
5、“坚决反对运动员服用兴奋剂”是“人文奥运会” 的重要体现。某兴奋剂的结构简式如下图:下列有关它的说法正确的是( )
A、该分子中的所有碳原子不可能共平面
B、该物质遇FeCl3溶液显紫色,因为该物质属于苯酚 的同系物
C、该物质能与小苏打溶液反应,因为该物质中存在 酚羟基结构
D、1mol该物质分别与浓溴水和H2反应时最多消耗 Br2和H2分别为4mol、7mol
 6、利尿酸在北京20##年奥运会上被禁用,它是一种兴奋剂,其结构简式如下图所示。下列叙述正确的是
6、利尿酸在北京20##年奥运会上被禁用,它是一种兴奋剂,其结构简式如下图所示。下列叙述正确的是
A.该有机物分子式为C13H16O4Cl2
B.1mol利尿酸能与6molH2发生加成反应
C.利尿酸能使溴水褪色
D.利尿酸能与氯化铁溶液发生显色反应
其 他
1、20##年夏季奥运会即将在北京进行,下列有关说法中,明显错误的是
A、奥运吉祥物—福娃的材质是PVC(聚氯乙烯),其单体为CH2==CHCl
B、奥运火炬—祥云火炬的燃料为丙烷,1mol丙烷完全燃烧至少需5mol氧气
C、奥运会将使用锂电池公交车为奥运村、媒体村等处服务,这种高能电池的最显著特点是提供相同的电量所需的金属正极质量最轻
D、奥运会国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯中既含有极性键又含有非极性键
2、20##年奥运会将在北京举行,届时可能会用大型遥控飞艇作为宣传工具以渲染活动气氛,为了使飞艇在空中安全而有效,你认为飞艇内充入哪种气体最好
A.氮气 B.氦气 C.氢气 D.二氧化碳
答 案
“绿色奥运”: 1.C 2.D 3.A 4.C 5. B 6.B 7.A 8.C
“水 立 方”: 1.B 2.A 3.C 4.D 5.C 6.C 7.B
“火 炬”: 1.B 2.A 3.B 4.D
“鸟 巢”: 1.A
“兴 奋 剂”: 1.B 2.B 3.B
“福 娃” 1.D 2.B 3.D
其 他: 1.A 2.B
-
高三化学教学总结.doc
高三化学教学总结杨店子高中王小玲高三化学总复习是中学化学学习的关键时期,是巩固基础、优化思维、提高能力的重要阶段,高三化学总复习的…
-
高三化学教学总结
关于高考化学总复习的几点教学体验福州三中金山校区化学组郭婧文高三化学总复习是学生是巩固基础、优化思维、提高能力的重要阶段,高三化学…
-
20xx年高三化学教学总结
莫毅娟本学年,我担任高三(9)班、高三(10)班的化学教学,根据一年以来的高考备考,我总结如下:1、以长远的目光看三年,高考备考应…
-
高三化学教学总结
高三化学复习是学生是巩固基础,优化思维,提高能力的重要阶段,高三化学复习的效果将直接影响高考成绩.为了使学生对高三化学复习有良好的…
-
高三化学教学总结
20xx年的高考落下了大幕,在这一年的高三教学中有得也有失,但我们总算是顺利得完成了学校交给的教学任务。现将一年来的高三化学教学工…
-
下学期高三化学教学工作总结
20xx-20xx学年下学期高三化学教学工作总结这学年我继续担任高三23、24两个的班的化学教学工作,随着高考一落幕,我们的工作也…
-
高三化学教学工作总结
20xx-20xx学年度第一学期化学教师:陆智东本学年度,我担任高三化学(19班、20班)的化学教学。按照教学计划,以及新的课程标…
-
高三化学教学工作总结
化学教师:杨颖本学年度,我担任高三化学(3班、6班)的化学教学。按照教学计划,以及新的课程标准,本人已经如期地完成了高三化学第一、…
-
高三化学教学工作总结
高三化学教学工作个人总结安徽省太和中学彭友明时间过得真快,随着20xx年高考一落幕,我们的工作也就此告一段落。在这一年里我继续体会…
-
高三化学教学工作总结与反思
本学期我任教高三(3)、(4)班的化学,半年来的高三教学使我深深地认识到:在复习中要充分发挥教师集体的力量和学生的主体作用,着力自…