高一必修2月考化学试题
高一年级第一次月考化学试题
说明:1、本试卷分第I卷和第II卷两部分;满分100分,考试时间70分钟。
2、请将第I卷和第II卷两部分的答案用黑笔写在试卷答题卷上。
可能用到的相对原子质量:H:1 C:12 N:14 O: 16 Cu: 64 Zn: 65
第I卷 (选择题 共44分)
一、选择题(本题共计10小题,每小题只有一个正确答案,每小题2分,共计20分)
1、20xx年1月15日,我国广西省龙江河检测出重金属镉含量严重超标,重金属镉具有毒性,长期过量接触镉会引起慢性中毒,影响人体肾功能。镉元素有多种核素,下列关于95
48Cd和97 48Cd说法正确的是( )
97 95 97 A.95
48Cd和48Cd互为同素异形体 B. 48Cd和48Cd质量数相同
97 95 97 C.95
48Cd和48Cd是同一种核素 D. 48Cd和48Cd互为同位素 --2、已知短周期元素的离子aX2+、bY+、cZ2、dW 都具有相同的电子层结构,则下列叙述正确的是( ) - - A.原子半径:X>Y>W>Z B.离子半径:Z2> W > Y+ > X2+
C.原子序数:d > c > b > a D.原子的最外层电子数目:X>Y>W>Z
3、原子序数为a的元素位于周期表中的第ⅡA族,则原子序数为a+1的元素不可能处在
A. 第ⅢA族 B.第三周期 C. 第一周期 D.第ⅢB族
4、硒为第四周期VIA族元素,根据它在元素周期表中的位置推断,硒不可能具有的性质是( )
A.H2SeO4的酸性比H2SO4的酸性强 B.其单质在通常状况下是固体
C.硒元素有+4、+6、-2三种常见化合价 D. SeO3的水化物为酸
5、同族元素所形成的同类型的化合物,其结构和性质往往相似。化合物PH4I是一种白色晶体,下列对它的描述中正确的是( )
A.它是一种共价化合物 B.在加热时此化合物不能分解
C.这种化合物不能跟碱反应 D.这种化合物可以由PH3和HI化合而成
6、在下列变化过程中,既有离子键被破坏又有共价键被破坏的是( )
A.加热I2使其升华 B.加热NaCl使其熔融
C.将HCl通入水中 D.NaHSO4固体溶于水发生电离
7、下列各组性质比较中,不正确的是( )
A.酸性:HClO4>HBrO4>HIO4 B.碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
C.单质的氧化性:F2<Cl2<Br2<I2 D.单质的还原性:Al<Mg<Na<K
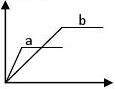
8、在四个不同容器中且不同条件下进行N2 + 3H2
结果判断生成氨的速率最快的是( )
A.V(NH3)=0.5 mol ?L-1-?min-1 B.V(H2)=0.02mol ?L-1-? s -1
C.V(N2)=0.2 mol ?L-1-?min-1 D.V(H2)=0.3 mol ?L-1-?min-1
9、下列变化过程中,需要吸收能量的是( ) 2NH3反应,根据在相同时间内测定的
A.H+H→H2 B.I2→I+I C. Al +H+ →Al3++H2 D.C+O2→CO2
10、把镁条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是( )
A.溶液的温度 B.盐酸的浓度 C.镁条的表面积 D.加少量Na2SO4固体
二、选择题(本题共计8小题,每小题只有一个正确答案,每小题3分,共计24分)
35 11、某元素的一种核素X的质量数为A,含N个中子,它与35
Cl原子组成X Clm分子,则ag
X35
Clm中所含质子的物质的量是( )
aaA.A+35m-N+17m) mol B.(A-N+17m) mol A+m
aC.(A-N) mol A+m aD.A+35m-N) mol
12、下列事实中,能说明氯元素的非金属性比硫元素的非金属性强的是( )
①盐酸的酸性比氢硫酸(H2S水溶液)酸性强 ②HCl的稳定性比H2S强 ③相同条件下,Cl2与铁反应生成FeCl3 ,而S与铁反应生成FeS ④Cl2能与H2S反应生成S ⑤酸性强弱:硫酸<高氯酸
A.①②③④ B.②③④ C.①②③④⑤ D.②③④⑤
13、右图是质量相等且形状相同的CaCO3固体与不同浓度盐酸反应放出CO2的图像,
(纵坐标表示CO2的体积,横坐标表示反应时间),其中对 盐酸浓度的判断正确的是( )
A.a的浓度大 B.b的浓度大
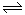
C.a与b浓度相同 D. 无法比较大小
14、某同学对“CO2是共价化合物和NH4Cl是离子化合物”, 有下列四点感悟,其
中不正确的是( ) ...
A.离子化合物中可能含共价键 B.共价化合物中一定不含离子键
C.离子化合物中不一定含金属元素
15、可逆反应2NO2
说法:
①反应混合物中各物质的物质的量浓度相等
②单位时间内生成n mol O2 的同时生成2n mol NO2
③用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2:2:1的状态 ④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均摩尔质量不再改变的状态
其中表示达到平衡状态的表述是( )
A.①④ B.②④⑥ C.①②③ D.①②④⑤
△ 16、已知C(s)+ CO2(g) 2CO(g)正反应为吸热反应,下列措施能使正反应速率
加快的是( ) D.离子化合物中一定不含共价键 2NO + O2在体积不变的密闭容器中反应,现有以下几种
①增加少量C(s) ②升高温度 ③容器不变,再通入CO2 ④缩小体积增大压强
A.①②③ B.①②③④ C.②③ D. ②③④
17、下列关于指定粒子构成的几种描述中,不正确的是( )
A.37Cl与39K具有相同的中子数
298
B.第116号元素的一种核素116X与84Po具有相同的最外层电子数
C.H3O+与OH-具有相同的质子数和电子数
?2-D.O22与S具有相同的质子数和电子数
18、将4 mol A和2 mol B在2L的密闭容器中混合并在一定的条件下发生如下反应:
2A(g)+ B(g)下几种说法:
①用物质A表示的该反应的平均反应速率为0.3 mol ?L-1? s -1 ②用物质B表示的该反应的平均反应速率为0.6 mol ?L-1? s -1 ③2s时物质B的物质的量的浓度为0.7 mol ?L1 ④2s时物质A的转化率为70% 其中表述正确的是( )
A. ①④ B.①③ C.②③ D.③④
-
2C(g),经2秒后测得C的浓度为0.6 mol ?L-1,现有以
第Ⅱ卷(非选择题,共56分)
三、填空题(本大题分3小题,共计35分)
19、(8分)下列几种物质中① Ar ②HCl ③NH4Cl ④ N2 ⑤ Na2O2 ⑥ CaCl2 ⑦H2O⑧KOH只存在共价键的是 ,只存在离子键的是 ,既存在共价键又存在离子键的是 ,不存在化学键的是 (填写序号)。
20、(14分)下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素
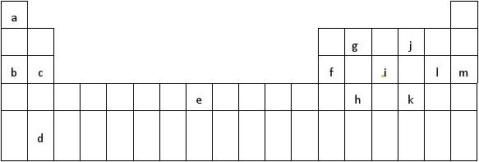
(1)表中所列元素中属于主族元素的有 ;
属于金属元素的有 ;e在元素周期表中的位置是 。
(2)下列_____组元素的单质可能都是电的良导体。
A.d、e、f B.b、c、i C.c、d、g D.a、g、k (3)表中某元素的最高价氧化物对应水化物呈两性的化学式是 , 它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式
是 ;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是 。
21、(13分)有A、B、C、D、E五种短周期元素, 它们的原子序数依次增大。 已知A和B
原子具有相同的电子层数, 且A的最外层电子数是次外层电子数的两倍, C是该周期中原子半径最大的元素, C的单质在加热下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物,E与D相邻。 试根据以上叙述回答:
(1)元素名称: A C __________ E
(2)写出AB2与过量氢氧化钠溶液反应的离子方程式 ; 写出 C2B2与AB2反应的化学方程式 ;
(3)画出D的原子结构示意图 ,
用电子式表示化合物 C2D 的形成过程 ;
(4)D、E的气态氢化物的稳定性 大于 (填化学式)。
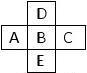
22、(8分)如图所示,前四周期元素中,已知A元素的
最低负化合价为-3价,它的最高价氧化物中含氧56.34%
(相对原子质量:A元素、31 氧元素:16)。
请回答:⑴写出A的名称_____,B的元素符号_____,
C的阴离子结构示意图_________,
D原子的电子式__________,E在周期表中的位置__________。
⑵A、B、C的原子半径由小到大的顺序为__________(填元素符号)。 ....
⑶D、B、E的氢化物的稳定性由高到低的顺序为_______________(填化学式)。 ....⑷A与D两种单质反应为_________反应(填“放热”或“吸热”)。
四、实验题(本题共1小题,13分)
23、实验探究:探究碳、硅元素的非金属性的相对强弱
根据要求完成下列各小题 ..
(1)实验装置:

2SiO3溶液
填写所示仪器名称A B
(2)实验步骤:
连接仪器、_____________、加药品后,打开a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是 ; 装置E中足量酸性KMnO4溶液的作用是 ; ②能说明碳元素的非金属性比硅元素非金属性强的实验现象是 ;
③依据试管D中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性___(填“能”或“否”),试管D中发生反应的离子方程式是 。
高一年级第一次月考化学试题答题卷 第I卷 (选择题 1-10每个2分,11-18每个3分,共44分) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 第Ⅱ卷(非选择题,共56分) 三.⑴ 、 ;⑵ 、 ⑶ ; (4) ; (5) ; 三. ; ; ; 四.⑴ ; ⑵ ⑶
五.⑴ ;
⑵ ;
⑶ ;
① ;
②
六. ⑴ 、 、 ;
⑵ ;
⑶ ;
⑷ ;
七、⑴ ⑵
⑶ 或 ;
八、A B C D E ⑴ ⑵ ⑶
参考答案
一、选择题(本题共计10小题,每小题只有一个正确答案,每小题2分,共计20分)
题号 答案
1 2 3 4 5 6 7 8 9
1
D B C A D D C B B D
二、选择题(本题共计8小题,每小题只有一个正确答案,每小题3分,共计24分)
题号 答案
11 A
12 D
13 A
14 D
15 B
16 D
17 C
18 B
三、填空题(本大题分5小题,共计56分)
19、(8分) (每空2分,错选漏选均不得分)
20、(14分)
(1)a、b、c、d、f、g、h、i、j、k、l;(错选漏选均不得分,2分)
b、c、d、e、f 、h;(错选漏选均不得分,2分) 第四周期VIII族(2分) (2)AC(2分)
(3))Al(OH)3 (2分), Al(OH)3+ OH=[ Al(OH)4](2分)(4)离子键和共价键(漏填、错填均不得分,2分)。
-
—
21、(13分)
(1)碳、钠、氯 (各1分,共计3分)
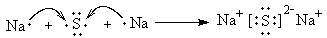
(2)CO2+2OH-=H2O+CO32- (2分) 2CO2+2Na2O2=2Na2CO3+O2↑(2分)
(3)
(各2分,共计4分)
(4)HCl H2S (各1分,共计2分) 22、 (13分)
(1)A:分液漏斗B:圆底烧瓶(每空1分) (2)检查装置的气密性(2分)
△
(3)①Cu+2H2SO4(浓)
CuSO4+ SO2↑+2H2O (2分) 除去SO2气体(2分)
-2---
②盛有Na2SiO3溶液的试管中出现白色沉淀(2分)
③否(1分)SO2+2HCO3=SO3+ H2O+CO2↑或SO2+HCO3=HSO3+CO2↑(2分)
23、
高一化学答题卷
1
2 3 4 5 6 8 9 10 11 12 13 15 16 17 18 19 20
19.⑴7 14
⑶ ;
(4) ;
20.⑴
⑵ ⑶
21.⑴;
⑵ ;
⑶ ;
(4) ;
(5)
22. ⑴;
⑵ ;
⑶ ;
4) ;
5)
-
高中化学必修1化学方程式总结
1、钠及其化合物的转化关系2②NaCl2①Na2O+2HCl=2NaCl+H2O②2Na+2HCl=2NaCl+H2↑++++Na…
- 高一化学必修1化学方程式及离子方程式汇总(背诵版)
-
高中化学必修一方程式大全
化学方程式一化学方程式总结1硫酸根离子的检验BaCl2Na2SO4BaSO42NaCl2碳酸根离子的检验CaCl2Na2CO3Ca…
-
高中化学必修1化学方程式总结
高中化学必修1化学方程式总结一钠及其化合物的转化关系1钠在空气中燃烧2NaO2点燃Na2O22钠在氧气中燃烧4NaO2点燃2Na2…
-
高一化学必修一化学方程式及离子方程式小结
必修一化学方程式及离子方程式小结1硫酸根离子的检验BaCl2Na2SO4BaSO42NaClSO4BaBaSO42碳酸根离子的检验…
-
高三化学月考总结
20xx-20xx学年度高三化学月考总结本次月考试题内容主要考查这一个月来学生的学习情况。总分为100+20分,其中有机化学约为4…
-
高一化学月考质量分析
一、对本次试卷的分析本次试卷总体上较全面的考查了本阶段所学内容,非选择题部分比较容易,,选择题部分难度不大,整个试题主要考查学生的…
-
高一化学教学工作总结
李红英本学期,我担任高一54、55、56、57四个班的化学教学工作,周课时为10课时。现就一学期以来的主要工作做以下的总结:开学初…
-
高一化学月考讲评变式练习 计算方法总结
高一化学月考试卷讲评一、阿伏伽德罗定律及推论试题重做17、在下列条件下,两种气体分子数一定相等的是:()A.同密度、同压强的N2和…
-
20xx——20xx学年度 高一化学备课组工作总结
20xx——20xx学年度高一化学备课组工作总结金台高级中学王伟平20xx-6-30本学期,在学校教导处、教研处、年级组的领导和指…