高一年化学必修1第二次月考试卷
20##至20##学年度第一学期礼县实验中学
高一年化学必修1第二次月考试卷
满分100分,答题时间1小时30分(温馨提示:所有答案全部写在答题卡上,写在试卷上无效)
本卷可能用到的相对原子质量:H~1 C~12 N~14 O~16 Cl~35.5 Na~23 Mg~24 Al~27 K~39 Fe~56 Ag~108 Mn~55
第Ⅰ卷 选择题(共54分)
一.选择题(每小题只有一个选项符合题意。每小题3分,共54分)
1.下列物质分类的正确组合是( )

2.铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等。下列与这些用途无关的性质是( )
A.不易生锈 B.导电性好 C.密度小 D.强度高
3.下列各组物质与其用途的关系不正确的是( )
A.过氧化钠:供氧剂 B.烧碱:治疗胃酸过多的一种药剂
C.小苏打:发酵粉主要成分 D.明矾:净水剂
4.下列说法正确的是( )
A. 一氧化碳的摩尔质量是28克
B. 氧原子的质量就是氧原子的相对原子质量。
C. C.1molN2的质量在以克为单位时,数值上等于它的相对分子质量。
D. D.1摩尔二氧化碳含有的分子的准确数目是6.02×1023个
5.钠与水反应时产生的各种现象如下( )
①钠浮在水面上;②钠沉在水底;③钠熔化成小球;④小球迅速游动逐渐减小,最后消失;⑤发出嘶嘶的声音;⑥滴入酚酞后溶液显红色。
A.①②③④⑤ B.①③④⑤⑥
C.①②③⑤⑥ D.全部
6.在空气中长时间放置少量金属钠,最终的产物是( )
A.Na2CO3 B.NaOH
C.Na2O D.Na2O2
7.将Na2O2投入FeCl3溶液中,观察到的实验现象是( )
A.有白色沉淀生成 B.有红褐色沉淀生成同时有无色气体生成
C.没有任何现象 D.有白色沉淀生成同时有无色气体生成
8.在强酸性溶液中能大量共存的无色透明离子组是( )
A. K+、Na++、CO32-、Cl- B. Mg2+、Na+、Cl-、SO42-
C. K++、Na+、Br-、Cu2+ D. Na+、Ba2+、OH-、SO42-
9.某盐的混合物中含有0.2mol Na+、0.4mol Mg2+、0.4mol Cl-,则SO42-为( )
A.0.1mol B.0.3mol
C.0.5mol D. 0.15mol
10.下列叙述正确的是( )
A.将三氯化铁饱和溶液滴入沸水中,再加热几分钟后可得到氢氧化铁胶体
B.氢氧化铁胶体分散质能透过滤纸,也能透过半透膜
C.溶液和胶体的本质区别是可否发生丁达尔效应
D.将氢氧化钠溶液滴入三氯化铁溶液中可得到氢氧化铁胶体
11.下列有关气体制取的反应中,其原理不属于氧化还原反应的是 ( )
A. 用稀硫酸与锌粒反应制取 H2
B. 用高锰酸钾加热分解制取 O2
C. 用浓盐酸与二氧化锰加热制取Cl2
D. 用稀盐酸与石灰石反应制取CO2
12.下列物质中既能与稀H2SO4反应, 又能与NaOH溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3
A.③④ B.①②③④ C.①③④ D.全部
13.下列有关钠的叙述正确的是 ( )
①钠在空气中燃烧生成氧化钠 ②金属钠可以保存在煤油中
③钠与硫酸铜溶液反应,可以置换出铜 ④金属钠有强还原性
⑤钠原子的最外层上只有一个电子,所以在化合物中钠的化合价显+1价
A.①②④ B.②③⑤ C.①④⑤ D.②④⑤
14.要证明某溶液中不含Fe3+而可能含有Fe2+。进行如下实验操作时最佳顺序为 ①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液( )
A.③① B.③② C.①③ D.①②③
15.下列各组中两个溶液间的反应,均可用同一离子方程式表示的是( )
A、CH3COOH和Na2CO3与CH3COOH和NaHCO3
B、AgNO3和HCl与AgNO3和NaCl
C、BaCl2和Na2SO4与Ba(OH)2与H2SO4
D、KOH和CH3COOH与NaOH与HCl
16.用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.标准状况下,22.4L H2O含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.常温常压下,1 NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol / L的MgCl2溶液中,含有Cl- 个数为1 NA
17.下列离子方程式书写正确的是( )
A.FeCl2溶液中通入Cl2 Fe2++Cl2 = Fe3++2Cl-
B.Ba(OH) 2溶液与盐酸的反应 OH-+H+ = H2O
C.Al(OH) 3沉淀中滴加盐酸 Al(OH)3 +3H+ = Al3++3H2O
D.AlCl3溶液中加入过量氨水 Al3++4OH-= AlO2--+2H2O
18.下列有关碳酸钠和碳酸氢钠的说法不正确的是( )
A. 在水中的溶解度:碳酸钠>碳酸氢钠
B. 热稳定性:碳酸钠>碳酸氢钠
C. 等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少
D. 足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生二氧化碳一样
第Ⅱ卷 (非选择题 共46分)
二、填空(共22分)
19.(每小题2分共10分)按要求完成有关化学方程式:(是离子反应的则写成离子方程式)
(1)钠在空气中燃烧 。
(2)氢氧化镁与盐酸反应 。
(3)除去Na2CO3固体中混有的少量NaHCO3固体 。
(4)氢氧化铝与氢氧化钠溶液反应 。
(5)铁与水蒸汽的反应 。
20.(6分)仅用一种试剂把Na2CO3 ,Ba(OH)2,Na2SO4三种无色溶液区别开,这种试剂是 ,(2分)写出有关反应的离子方程式 。(4分)
21.(6分)Na2O2可用作呼吸面具中的供氧剂,请写出有关反应的化学方程式,再指出反应中的氧化剂和还原剂,并用双线桥标出电子的转移① 氧化和还原剂分别是: ;② 氧化剂和还原剂分别是: 。
三、推断题、实验题(18分)
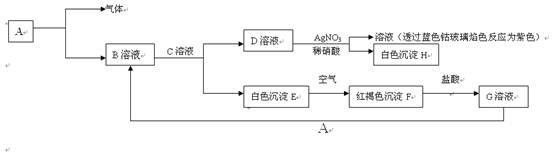 22. 已知有以下物质相互转化关系:
22. 已知有以下物质相互转化关系:
①写出B的化学式 ,D的化学式 。
②写出E转为F的化学方程式 。
③在G溶液中加入硫氰化钾的现象为 ,向G溶液中加入A的有关反应的离子方程式为 。
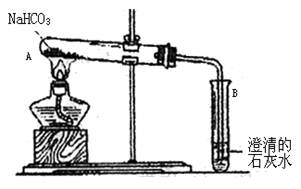
23.(8分)右图是加热分解碳酸氢钠的实验装置图。
(1)试管B中可观察到的现象是
有关反应的离子方程式 。
(2)试管B中不再出现气泡时,停止实验的正确操作是 。
(3)实验结束时发现试管B中又重新变成透明澄清的溶液,写出试管B中发生的反应的离子方程式 。
四、计算题(6分)
24.将3.9g Na2O2现投入到足量的水中充分反应。请回答:
①生成的气体在标准状态下的体积为多少L。
②该反应中所消耗的不的质量为多少g。
③将反应后的溶液配成1000mL溶液,所得溶液的物质的量浓度为多少?
20##至20##学年度第一学期礼县实验中学
高一年化学必修1第二次月考试卷
答题卡
一.选择题(每小题只有一个选项符合题意。每小题3分,共54分)

第Ⅱ卷 (非选择题 共46分)
二、填空(共22分)
19.(每小题2分,共10分)
(1) (2)
(3) (4)
(5 )
20.(6分)
这种试剂是 (2分) (4分)
21.(6分)① 氧化和还原剂分别是: ;
② 氧化剂和还原剂分别是: 。
三、推断题、实验题(18分)
22.(每小题2分)①写出B的化学式 ,D的化学式 。
②写出E转为F的化学方程式 。
③在G溶液中加入硫氰化钾的现象为 ,向G溶液中加入A的有关反应的离子方程式为 。
23.(每小题2分)
(1) ,
(2)
(3)
四、计算题(6分)
24.
第二篇:高一化学(必修1)第二次月考试题
高一化学(必修1)第二次月考试题
考试时间:90分钟 命题人:王俊
可能用到的相对原子质量:
H—1、N—14、O—16、S—32、Cl—35.5、K—39、Na—23、 Ag--108
第Ⅰ卷(共60分)
一、选择题(共12小题,每小题只有一个选项符合题意,每小题5分,共60分)
1、胶体区别于其他分散系的本质特征是:
A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B.产生丁达尔现象
C.分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在
2、等质量的下列物质中,所含分子数最少的是
A.Cl2 B.HCl
C.NH3 D.H2SO4
3.下列反应既属于化合反应,又属于氧化还原反应的是
A. Fe+2HCl=H2+FeCl2
B.2FeCl2+Cl2=2FeCl3
C.CaO+H2O=Ca(OH)2
D.2Fe(OH)3 =Fe 2O3 +3H2O
4、实验室有三瓶失去标签的试剂,分别是Na2CO3、NaCl、AgNO3。实
验员选择了一种试剂就把它们区别开来了,这种试剂是:
A.盐酸 B、氢氧化钠溶液 C、氯化钡溶液 D、硝酸
5.氧化还原反应的实质是 ( )
A.氧元素的得与失 B.化合价的升降
C.电子的得失或偏移 D.分子中原子重新组合
6.下列叙述正确的是( )
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
1
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4L
7、某实验小组只领取下列仪器或用品:铁架台、铁圈、铁架、三角架、石棉网、烧杯、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、蒸馏烧瓶、火柴、滤纸、漏斗。只应用上述仪器或用品,不能进行的实验操作是
A. 蒸发 B. 萃取 C. 过滤 D. 蒸馏
8、和22 g CO2所含分子数相等的水的质量为( )
A.44 g B.22 g C.18 g D.9 g
9、下列说法正确的是:
A.摩尔是物质的量的单位
B.熔融状态下或溶液中能导电的物质就是电解质
C.氧化还原反应的本质是化合价发生了变化
D. 得电子的物质被还原,是还原剂。
10、能在溶液中大量共存的一组离子是
A、Cu2+、SO42-、OH—、K+
B、Na、CO32-、H+、Cl-
C、H+、Cl-、NO3-、Ba2+
D、Ca2+、H+、CO32-、NO3-
11.农药波尔多液可用于水果灭虫,是由石灰水和硫酸铜溶液混合而成的悬浊液。它不能用铁制容器盛放,是因为铁与该农药中的硫酸铜起反应。在该反应中,对铁的叙述错误的是 ..
A.铁发生还原反应 C.铁是还原剂 B.铁发生氧化反应 D. 铁失去电子
12、在下列反应中, HCl 作氧化剂的是( )
A、NaOH+HCl=NaCl+H2O
B、Zn+2HCl=ZnCl2+H2↑
C、MnO2+4HCl(浓)MnCl2+2H2O+Cl2↑
D、CuO+2HCl=CuCl2+H2O
第Ⅱ卷(共40分)
二、填空题(共29分)
2
13.(4分)实验室制取氢氧化铁胶体的方法是,可用 (方法)证明胶体已经制成。
14.在Fe3O4 +4CO3Fe+4CO2的的中, 是氧化剂, 是
还原剂 元素被氧化, 元素被还原。
15.写出下列反应的离子方程式:(每小题2分,共4分) .....
(1)AgNO3溶液与KCl溶液混合: _________________________
(2)硫酸和氢氧化钡溶液混合:
________________________________________________________
16、用下列仪器的编号回答问题:
①容量瓶 ②蒸馏烧瓶 ③量筒④烧杯 ⑤托盘天平⑥分液漏斗
⑴加热时必须垫石棉网的有 ,
⑵使用时必须检查是否漏水的有 ,
⑶标有零刻度的有 。
四、计算题(11分)
17、实验室常用盐酸的质量分数为36.5%,密度为1.20g/㎝3。
(1) 此浓盐酸的物质的量浓度是多少?(列式计算)
(2) 配制100mL3.00mol/L的盐酸,需以上浓盐酸多少mL ?(列
式计算)
(3) 用浓盐酸配制该稀盐酸需要以下哪些步骤(按操作顺序填
写序号):①计算 ②装瓶③用50 mL量筒量取一定体积的浓盐酸④洗
涤⑤移液⑥稀释⑦定容⑧摇匀
3
高一级化学科期中考试题答题卡
第一题:选择题
第二题:填空题
13、、 14、、、 15、(1)(2)16、(1)2)3)、第三题:计算题 17(1): (2)
(3)
4
高一级化学科期中考试题答案
第一题:选择题(60分)
第二题:填空题
13、向沸腾的水中滴加少量氯化铁饱和溶液,并继续煮沸至液体呈褐色、丁达尔效应(6分) 14、Fe3O4、CO、C、Fe(8分) 15(1)Ag++Cl-=AgCl↓
2-+2+-(2) SO4+2H+Ba+2OH=BaSO4↓+2H2O
(6分)
16. ⑴ ②④ ;⑵ ①⑥; ⑶ ⑤(9分) 第三题:计算题 四、计算题(11分) 17、(1)(4分)
C=1000×1.20×36.5%÷36.5=12.0mol/L (2)(4分)设需浓盐酸XmL
100mL×3.00mol/L= 12.0mol/L·X X=25 mL
(3)(3分)
5
-
【强烈推荐】高一化学必修一第一章总结
第一章从实验学化学一、常见物质的分离、提纯和鉴别1.常用的物理方法——根据物质的物理性质上差异来分离。混合物的物理分离方法i、蒸发…
-
高一化学必修一知识点总结
新课标化学必修一1学习方法2研究一种物质的性质的程序3观察法4金属钠的物理性质5金属与水的反应第三章金属及其化合物1金属的化学性质…
-
高一化学必修一第一章知识总结
高一化学必修一第一章知识总结11化学实验基本方法111化学实验安全A常见危险化学品爆炸品KClO3KMnO4KNO3易燃气体H2C…
-
高一化学必修一第一章总结
平凡的人听从命运只有强者才是自己的主宰1平凡的人听从命运只有强者才是自己的主宰2平凡的人听从命运只有强者才是自己的主宰3平凡的人听…
-
高中化学鲁科版必修一第一章总结
化学第一章章末总结现象钠浮在水面上密度比水小熔化为银白色小球反应放热熔点低在水面上四处游动反应放出气体伴有嘶嘶响声气体与水摩擦滴有…
-
高三化学月考总结
20xx-20xx学年度高三化学月考总结本次月考试题内容主要考查这一个月来学生的学习情况。总分为100+20分,其中有机化学约为4…
-
高一化学月考质量分析
一、对本次试卷的分析本次试卷总体上较全面的考查了本阶段所学内容,非选择题部分比较容易,,选择题部分难度不大,整个试题主要考查学生的…
-
高一化学教学工作总结
李红英本学期,我担任高一54、55、56、57四个班的化学教学工作,周课时为10课时。现就一学期以来的主要工作做以下的总结:开学初…
-
高一化学月考讲评变式练习 计算方法总结
高一化学月考试卷讲评一、阿伏伽德罗定律及推论试题重做17、在下列条件下,两种气体分子数一定相等的是:()A.同密度、同压强的N2和…
-
20xx——20xx学年度 高一化学备课组工作总结
20xx——20xx学年度高一化学备课组工作总结金台高级中学王伟平20xx-6-30本学期,在学校教导处、教研处、年级组的领导和指…