分析化学设计性实验报告
阿司匹林中乙酰水杨酸含量的测定预习报告
本实验采用酸碱滴定法测定阿司匹林药片中乙酰水杨酸的含量
测定原理:
阿司匹林的主要成分是乙酰水杨酸。乙酰水杨酸是有机弱酸(Ka=1×10-3),
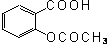
结构式为,
摩尔质量为180.16g/mol,微溶于水,易溶于乙醇。
由于它的Ka较大,可以作为一元酸用NaOH溶液直接滴定,以酚酞为指示剂。为了防止乙酰基水解,应在10℃以下的中性冷乙醇介质中进行滴定,滴定反应为:
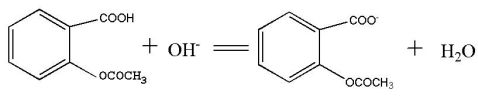
在强碱性溶液中溶解并分解为水杨酸(邻羟基苯甲酸)和乙酸盐,反应式如下:
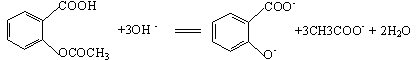
若采用直接滴定,操作较简单,但在反应过程中加入的碱可能使苯环支链上的脂水解,若采用反滴定法,反应过程中脂可能水解不完全。为更准确地测定乙酰水杨酸的含量,本实验先用纯乙酰水杨酸试剂进行两种方法的滴定,对比后选择较准确的操作方法再进行测定。
—采用直接滴定时,乙酰水杨酸上的羧基与OH进行1:1的中和反应。
采用反滴定时,乙酰水杨酸在强碱的条件反应分解为水杨酸盐和乙酸盐,在滴定终点时,体系的酸碱度为中性偏酸,此时苯环上的一个支链以酚羟基的形式存在,所以,在这一滴定反应中,1mol乙酰水杨酸消耗2mol NaOH。
实验仪器:
容量瓶100ml(3个)、200ml(1个)、50ml(2个)、烧杯100ml(4个)、表面皿(1个)、 酸式滴定管(1支)、碱式滴定管(1支)、量筒10ml(1个)试剂瓶500ml(2个)、
胶头滴管(2支)、移液管20ml(1支)、10ml(1支)、锥形瓶250ml(6个)、称量纸(5张)、 带胶头滴管的小试剂瓶(2套)、酒精灯(1个)、三脚架(1个)、电炉(一套)、 称量瓶(1个)、石棉网(1个)、研钵(1套)、电子天平(1台)、托盘天平(1台)、 电子台秤(1台)、温度计(100℃ 1支)、滤纸(擦烧杯)
实验试剂:
所有试剂,除注明者外,皆为分析纯,水均指蒸馏水或去离子水。
-11.1mol·LNaOH溶液 :用电子台秤称取氢氧化钠固体12.0g,配成300mL的溶液。
-12.0.1mol·LHCl溶液 :用量筒量取6ml浓HCl(12mol/L)用水稀释至700ml于试剂瓶中
3.酚酞指示剂:称取0.1克酚酞溶于50ml 95%无水乙醇
4.甲基红指示剂:称取0.1g甲基红溶于50ml 95%乙醇中
5.硼砂Na2B4O7·10H2O基准试剂 :4g(用电子天平称取1.9-2.3g用水稀释至100ml容量
瓶中)
6.阿司匹林药片 :20片
7.乙酰水杨酸:2.0g
实验步骤:
1.盐酸溶液的标定
以硼砂Na2B4O7·10H2O为基准物质标定
用差减法准确称取1.9-2.3g硼砂,置于小烧杯中加少量水溶解,转移至100ml容量瓶,用蒸馏水稀释至刻度线,定容后摇匀。用20ml移液管移取20.00ml硼砂溶液于250ml锥形
-1瓶中,滴加2滴甲基红指示剂,用0.1mol·LHCl溶液滴定溶液至黄色恰好变为浅红色,即
为终点。平行测定3次。计算HCl溶液的浓度CHCL。
CHCL=C(Na2B4O7?10H2O)?V(Na2B4O7?10H2O)?10?3
VHCl?10?3
2.氢氧化钠溶液的标定
称取12.0g氢氧化钠固体配成300ml溶液,用碱式滴定管取25.00ml上述溶液于100mL容量瓶中,用去离子水稀释至刻度,摇匀。在250mL锥形瓶中加入10.00mL上NaOH溶液,加
-1入去离子水20~30mL,加入2~3滴酚酞指示剂,用0.1 mol·LHCl溶液滴定,至红色刚刚
消失即为终点,平行测定3次。(本步骤所用的去离子水需经煮沸冷却)
CNaOHCHCl?VHCl?10?3??10 25ml?10-3
3.反应条件的探究
1)直接滴定:
①乙醇的预中和
量取约60ml乙醇置于100ml烧杯中,加入3滴酚酞指示剂,在搅拌下滴加0.1mol?Lˉ?的NaOH溶液至刚刚出现微红色,盖上表面皿,将烧杯泡在冰水中。
②滴定
准确称取乙酰水杨酸样品0.4-0.5g置于100ml干燥的锥形瓶中,加入20ml中性冷乙醇,置于冰水中,摇动使试样溶解后立即用NaOH标准溶液滴定至微红色为滴定终点,记录NaOH的体积。平行滴定3次。
2)返滴定
准确称取乙酰水杨酸样品0.4-0.5g于100ml 干燥烧杯中,用碱式滴定管取25ml 1mol/L的NaOH溶液于100ml烧杯中,加热至沸腾,盖上表面皿,用流水冷却后定量转移至盛放药品的烧杯中,用量筒加水30ml,盖上表面皿,轻摇几下,水浴加热15min,迅速用流水冷却,将烧杯中的溶液定量转移至100mL容量瓶中,用去离子水稀释至刻度线,摇匀。准确移取上述试液10.00mL于250mL锥形瓶中,加去离子水20~30ml,加入2~3滴酚酞指示剂,用0.1mol·L-1HCl标准溶液滴至红色刚刚消失即为终点。根据所消耗的HCl溶液的体积计算消耗的NaOH的物质的量。
3)选择反应条件
①若直接滴定法的结果中,氢氧化钠和乙酰水杨酸的反应系数比较接近1:1,则采用直接滴定法进行测量。
②若反滴定的结果中,氢氧化钠和乙酰水杨酸的反应系数比较接近1:2,则采用反滴定法进行测量。
4.药片中乙酰水杨酸含量的测定 1)直接滴定法
称量每片将阿司匹林药片的质量m g,取20片研成粉末后,准确称取m样品总质量=0.4-0.5g药粉三份,于干燥100mL锥形瓶,加入20ml中性冷乙醇,置于冰水中,摇动使试样溶解后立即用NaOH标准溶液滴定至微红色为滴定终点,记录NaOH的体积。平行滴定3次。
m乙酰水杨酸?CNaOH?VNaOH?10-3?M乙酰水杨酸
W乙酰水杨酸?
2)返滴定
称量每片将阿司匹林药片的质量m g,取20片研成粉末后,准确称取m样品总质量=(18m-19m)g药粉,于干燥100mL烧杯中,用碱式滴定管取25ml 1mol/L的NaOH溶液于100ml烧杯中,加热至沸腾,盖上表面皿,用流水冷却后定量转移至盛放药品的烧杯中,用量筒加水30ml,盖上表面皿,轻摇几下,水浴加热15min,迅速用流水冷却,将烧杯中的溶液定量转移至100mL容量瓶中,用去离子水稀释至刻度线,摇匀。
准确移取上述试液10.00mL于250mL锥形瓶中,加去离子水20~30ml,加入2~3滴酚酞指示剂,用0.1mol/L HCl标准溶液滴至红色刚刚消失即为终点。根据所消耗的HCl溶液的体积计算药片中乙酰水杨酸的质量分数及每片药剂中乙酰水杨酸的质量(g/片)。 (本步骤所用的去离子水需经煮沸冷却)
m乙酰水杨酸m样品总质量
m每片药剂乙酰水杨酸的
含量
?W乙酰水杨酸?m
m乙酰水杨酸
CNaOH?25ml?10?3?CHCl?VHCl?10?3??10?M乙酰水杨酸
2
m乙酰水杨酸m样品总质量
W乙酰水杨酸?
m每片药剂乙酰水杨酸的
含量
?W乙酰水杨酸?m
阿司匹林中乙酰水杨酸含量测定仪器试剂清单
20112401084杨晓纯&20112401080古梅莹
实验仪器:
容量瓶100ml(3个)、200ml(1个)、50ml(2个)、烧杯100ml(4个)、表面皿(1个)、 酸式滴定管(1支)、碱式滴定管(1支)、量筒10ml(1个)试剂瓶500ml(2个)、
胶头滴管(2支)、移液管20ml(1支)、10ml(1支)、锥形瓶250ml(6个)、100ml(1个)、称量纸(5张)、
带胶头滴管的小试剂瓶(2套)、酒精灯(1个)、三脚架(1个)、电炉(一套)、 称量瓶(1个)、石棉网(1个)、研钵(1套)、电子天平(1台)、托盘天平(1台)、 电子台秤(1台)、温度计(100℃ 1支)、滤纸(擦烧杯)
【老师准备】
1. 容量瓶50ml(2个)、
2. 锥形瓶100ml(1个)、
3. 电子台秤(1台)、
4. 托盘天平(1台)、
5. 研钵(1套)、
6. 带胶头滴管的小试剂瓶(2个)、
7. 电炉(1套,用于煮去离子水)、
8. 电子天平(1台)、
9. 称量纸(5张)、
10. 温度计(100℃ 1支)
11. 滤纸(擦烧杯)
实验试剂:
1.1mol·L-1NaOH溶液:用电子台秤称取氢氧化钠固体12.0g,置于烧杯中用少量水溶
解后配置成300mL溶液备用。
2.0.1mol·L-1HCl溶液:用量筒量取6ml浓HCl(12mol/L)用水稀释至700mL
于试剂瓶中
3.酚酞指示剂:称取0.1克酚酞溶于50ml 95%无水乙醇
4.甲基红指示剂:称取0.1g甲基红溶于50ml 95%乙醇中
5.硼砂Na2B4O7·10H2O基准试剂 :4g(用电子天平称取1.9-2.3g用水稀释至100ml容量
瓶中)
6.阿司匹林药片 :20片
7.乙酰水杨酸纯品:2g
8.无水乙醇:250mL
【老师准备】
1.
2.
3.
4.
5. NaOH固体(分析纯)12g、 浓盐酸(12mol/L)7ml、 酚酞0.1g、 甲基红0.1g、 95%无水乙醇250ml、
6.
7.
8.
9. Na2B4O7·10H2O(分析纯) 8g、 阿司匹林药片40片 乙酰水杨酸纯品(分析纯):2g 碎冰(适量、请老师实验开始前启用制冰机)
第二篇:设计性实验报告(一种液体洗涤剂的制备及分析)
应用化学综合实验报告
(设计性实验报告)
实验名称: 液体洗涤剂的制备和检测
实验报告人:*** 学生学号: 班级:
同组人:
实验日期: 2011 年 11 月 15 日
室温:大气压:
指导教师:
评 分:
1、前言
1.1液体洗涤剂的种类及用途
液体洗涤剂一般分为织物用洗涤剂、硬表面清洁剂和个人卫生清洁剂。硬表面清洁剂是一大类洗涤剂,包括餐具洗涤剂、日常硬表面清洁剂、金属表面清洁剂及交通工具清洁剂。个人卫生清洁剂在国外一般归类于化妆品种。
按液体洗涤剂的用途获功能进行分类可以分为织物液体洗涤剂、厨房液体洗涤剂、居室液体清洁剂、个人卫生清洁剂、金属清洁剂、交通工具清洁剂。
1.1.1 织物液体洗涤剂
织物液体洗涤剂用于洗涤各种衣料、衣物及其其他纺织品。
1.1.2 厨房液体洗涤剂
厨房液体洗涤剂用于厨房的各种硬表面清洗和消毒,其清洗范围涉及整个厨房的全面清洗,包括餐具、炉灶、地面、抽油烟机、饮具、及洗碗机等。
1.1.3 居室液体洗涤剂
居室液体洗涤剂系列产品用于居室或公共场所,家庭中的应用较为普遍,如清洁地毯、浴室、厕所、家具等
1.1.4 个人卫生清洁剂
个人卫生清洁剂用于个人卫生的清洁,包括头发、皮肤和口腔等。
1.1.5 金属清洁剂与交通工具清洁剂
金属洗涤剂主要是对加工金属件或机器本身进行清洗。清洁其中的油污、油漆及颗粒污垢,并保持金属表面不腐蚀、不损伤。
1.2液体洗涤剂的意义及发展
洗涤用品是指洗涤物体时,能改变谁的表面活性、提高去污效果的一类物质。洗涤剂是千家万户的日用必需品,长期以来对保护人体健康、洗洁环境起着十分重要的作用。
与固体洗涤剂相比,液体洗涤剂使用前无需溶解,具有使用方便、溶解(分散)速度快、低温洗涤性能好的优点。同时,还具有配方灵活,制造工艺简单、设备投资少、节省能源、加工成本低等优点,越来越受到消费者的欢迎。
在西欧,液体洗涤剂已得到广泛的应用。据统计,在发达国家,固体洗涤剂约占60%,液体洗涤剂约占40%。我国液体洗涤剂近年来发展很快,目前产量
已逾160万吨。今后,我国液体洗涤剂生产将持续高速发展。
2、实验部分
2.1配方的设计原理
洗涤剂的组成主要包括表面活性剂、助剂和辅助剂。在选择液体洗涤剂的主要组分时,可遵循以下一些通用原则:(1)有良好的表面活性和降低表面张力的能力,在水相中有良好的溶解能力;(2)表面活性剂在油/水界面能形成稳定的紧密排列的凝聚态膜;(3)表面活性剂能适当增大水相黏度,以减少液滴的碰撞和聚结速度;(4)要能用最小的浓度和最低的成本达到所要求的洗涤效果。
2.2仪器和药品
仪器:
烧杯,磁力搅拌恒温水浴锅,搅拌机,电子天平,玻璃棒,罗氏泡沫仪,pH计等。
药品:
烷基苯磺酸钠(LAS), 烷基酚聚氧乙烯醚(OP-10),三乙醇胺(85%),无水乙醇,荧光增白剂,去离子水,香精。
2.3配方
表-1 配方组分含量
配方成分
LAS
OP-10
三乙醇胺(85%)
无水乙醇
荧光增白剂
香精
去离子水
2.4实验步骤
在35℃的恒温水浴中,固定好烧杯和搅拌器,按配方中的顺序加料。边搅拌边将表面活性剂和助剂依次加入到去离子水中。每加入一个组分需搅拌15分质量分数 8.0% 40.0% 7.0% 5.0% 0.2% 适量 39.8% 主要功能和作用 表面活性剂,去污 表面活性剂,去污 有机助剂,助溶 有机助剂,助溶 辅助剂,调色 辅助剂,调香
钟左右再加下一组分。搅拌速度适中。全部加入完之后继续搅拌1小时左右。反应完之后测试原液的pH值,并将pH值调至8.5左右。
2.5产品的测试及应用
2.5.1 产品的pH值测试
液体洗涤剂的pH值按照GB/T 6368-2008表面活性剂的pH值测定来进行,以样品的1 %水溶液25 ℃时进行测定
2.5.2 产品的稳定性测试
将液体洗涤剂倒入洁净的100 mL无色透明玻璃磨口试剂瓶中,加塞。置于(-5±2)℃冰水浴中,24h取出,恢复到(15~25)℃,观察外观,记录是否分层、沉淀。
将液体洗涤剂倒入洁净的60 mL无色透明玻璃磨口试剂瓶中,加塞。置于(40±2)℃保温箱中,24 h取出,恢复到(15~25)℃,观察外观,记录是否分层、沉淀。
2.5.3 产品的发泡力测试
液体洗涤剂的发泡力测定按GB 7462-1994表面活性剂的发泡力测定来进行。用c=2.5 mmol/L 的Ca2+硬度的水配制样品的0.25 %溶液,用罗氏泡沫仪按表面活性剂发泡力的测定方法测定。
2.5.4 产品的去污力测试
取小片布料,称量其质量m0,将其浸取油污晾干,称量其质量m1。之后,用产品洗涤,晾干,称量洗涤之后的质量m2。
计算去污力=(m1-m2)/(m1-m0)*100%
3、备注
本实验方案尚未得以实践,故有所不完善之处将在实验中得到总结,并讨论完善之。认真观察实验现象,并做好实验记录。若35℃不满足实验要求,可适当升高温度,但不超过40℃(高于40℃时OP-10的稳定性差)。
所涉及的国标见附表补充材料。
4、参考文献
1. 蓝建京、蓝丽红. 高效衣料液体洗涤剂的研究(N). 大众科技. 2008(2).
2. 廖文胜. 液体洗涤剂——新原料·新配方(M). 第二版. 北京:化学工业出版社,2004. 10.
3. 徐宝财. 洗涤剂概论(M). 第二版. 北京:化学工业出版社,2007. 10.
4. 宋小平,韩长日. 洗涤剂实用配方与生产工艺(M). 北京:中国纺织出版社,2010. 9.
-
分析化学实验报告
分析化学实验报告20xx0218200858分类理工类标签字号大中小订阅盐酸和氢氧化钠标准溶液的配制和标定时间12月15号指导老师…
-
分析化学实验报告(武汉大学第五版)
分析化学实验报告陈峻贵州大学矿业学院贵州花溪550025摘要熟悉电子天平的原理和使用规则同时可以学习电子天平的基本操作和常用称量方…
-
分析化学实验报告
级名分析化学实验报吉林农业大学告班姓同组人实验酸碱标准溶液的配制和比较滴定实验目的实验原理实验步骤1酸碱标准溶液的配制101mol…
-
分析化学实验报告样本
实验名称游标卡尺的使用实验目的1掌握游标卡尺的使用方法2了解游标卡尺的结构原理3学习数据处理的相关内容4养成良好的写实验报告的习惯…
-
分析化学实验报告本模版
分析化学实验报告实验一电子分析天平的操作及称量练习学院专业班级姓名学号实验日期年月日教师评定实验目的掌握电子分析天平的基本操作和粉…
-
分析化学实验报告七
硫酸铜中铜含量的测定摘要:利用间接碘量法测定铜离子的含量。旨在掌握硫代硫酸钠溶液的配制和保存,并掌标定握硫代硫酸钠溶液浓度的原理和…
-
分析化学实验报告
四川农业大学实验报告课程名称:分析化学实验实验名称:班级学号学生姓名指导教师硫酸铜中铜含量的测定作者:李豪杨蕊摘要:利用间接碘量法…
-
分析化学实验报告3. CAT-20xx-0924-ST
血红蛋白过氧化物酶特性的测定一.目的了解血红蛋白的特殊性质,学习利用时间扫描法测定酶活力的方法,并加深理解过氧化物酶的催化作用。二…
-
《分析化学实验》总结
定量分析是一门实验性课程,通过分析化学实验可以是我们对分析学化学基本理论进一步加深理解,并能够熟练地掌握定量分析的基本操作技能,为…
-
分析化学实验心得
分析化学实验心得体会分析化学是人们获得物质化学组成和结构信息的科学,它所要解决的问题是物质中含有哪些组分,各个组分的含量多少,以及…