实验性毕业论文范例
学号: 4109014048
泰山医学院毕业设计(论文)

题目:2212 凋亡机制的研究
院(部)系
所 学 专 业
年级、班级 完成人姓名 指导教师姓名
专业技术职称 药学院 药学
20xx年 6 月 18 日
论文原创性保证书
我保证所提交的论文都是自己独立完成,如有抄袭、剽窃、雷同等现象,愿承担相应后果,接受学校的处理。
专业:
班级:
签名:
20 年 月 日
泰山医学院本科毕业设计(论文)
摘 要
目的 观察蜂胶黄酮对过氧化氢(H2O2)诱导大鼠肾上腺嗜铬细胞瘤细胞(PC12)凋亡的影响及机制。
方法 培养PC12细胞,取对数生长期细胞分为五组,空白对照组、模型组、蜂胶黄酮高、中、低剂量组,剂量分别为200mg/L、100 mg/L、50 mg/L.药物预处理2h后,孵育H2O2(140μmol/L)24h诱导过氧化损伤。TUNEL试剂盒检测原位细胞凋亡,流式细胞仪检测细胞内活性氧水平以及细胞周期,ELISA检测细胞内Caspase-3蛋白含量。
结果 TUNEL细胞凋亡染色显示, H2O2组与空白对照组比较染色明显加深,而蜂胶黄酮
组染色明显变浅,说明蜂胶黄酮能对抗H2O2诱导细胞凋亡;周期结果显示H2O2组处于G0/G1
细胞明显增多,而处于G2/M、S期细胞明显减少,细胞增殖降低,而蜂胶黄酮增加S期细胞促进细胞增殖;与空白对照组相比H2O2组活性氧水平、细胞内Caspase-3含量明显增高,
而蜂胶黄酮各剂量组活性氧水平降低,Caspase-3含量减少。
结论 蜂胶黄酮对H2O2诱发PC12神经细胞凋亡有显著的抑制作用,其机制可能其影响细胞周期、清除氧自由基、降低凋亡因子Caspase-3有关。
关键词 蜂胶黄酮;PC12细胞;H2O2;Caspase-3;细胞凋亡
泰山医学院本科毕业设计(论文)
Abstract Objective: To observe the protection of propolis flavonoids on rat with injuried pheochromocytomacells(PC12) induced by hydrogen peroxide(H2O2) and to explore its possible mechanism.
Methods: Culture PC12 cells,the cells in the logarithmic growth phase were divided into five groups,blank control group,model group,propolis flavone of high,medium and low dose group,the dose of 200mg/L,100 mg/L,50 mg/L. After 2h 0f Pharmacological preconditioning,the cells were incubated with H2O2(140 μ mol/L) for 24h to induce oxidative damage. TUNEL Kit is used for determining Cell apoptosis,Flow cytometry was used to detect the intracellular ROS level and cell cycle,ELISA is used for determining the concentration of protein Caspase-3 in cells. Results: Apoptosis of TUNEL cells staining, H2O2 group compared with the control group, staining was deepened, and the propolis flavone group was significantly lighter, that propolis flavonoids can antagonize the apoptosis induced by H2O2 Cycle showed that H2O2 group in G0/G1 cells were increased, and in the G2/M,S phase cells decreased significantly, reduced cell proliferation, and propolis flavonoids increased S phase cells promoting cell proliferation; compared with the blank control group, caspase-3 in H2O2group, the levels of reactive oxygen species in cells increased significantly, while the propolis flavone in all dose groups decrease the levels of reactive oxygen species, reduced caspase-3 content.
Conclusion: Propolis flavonoids on H2O2-induced PC12 cells damage a significant protective effect,The mechanism may be its effect on cell cycle, scavenging oxygen free radicals, decrease the apoptosis related factor caspase-3.
Key words: Propolis; flavonoids; PC12 cells; H2O2; apoptosis
泰山医学院本科毕业设计(论文)
目 录
正文????????????????????????????????????01 1前言??????????????????????????????????01 2仪器与试剂???????????????????????????????01 3实验方法????????????????????????????????02
3.1 蜂胶总黄酮的提取与含量测定?????????????????????02
3.2 PC12细胞的培养及分组给药??????????????????????02
3.3 TUNEL细胞凋亡原位检测????????????????????????02
3.4流式细胞仪检测细胞周期???????????????????????02
3.5流式细胞仪检测细胞内活性氧水平???????????????????03
3.6 ELISA试剂盒检测细胞内Caspase-3蛋白含量??????????????03 4实验结果????????????????????????????????03
4.1 TUNEL细胞凋亡原位检测???????????????????????03
4.2流式细胞仪检测细胞周期???????????????????????04
4.3流式细胞仪检测细胞活性氧水平????????????????????05
4.4 ELISA检测细胞内Caspase-3蛋白含量?????????????????06 5讨论?????????????????????????????????07 6结论?????????????????????????????????08 参考文献?????????????????????????????????09 文献综述?????????????????????????????????10 致谢???????????????????????????????????15
泰山医学院本科毕业设计(论文)
蜂胶黄酮抗H2O2诱导PC12细胞凋亡机制的研究
学生:*** 指导教师:***
(泰山医学院药学院,泰安 271016)
1 前言
老年性痴呆 (Alzheimer?s disease, AD) 是一种以进行性认知功能障碍和记忆能力受损为主的中枢神经系统退行性疾病。该病严重威胁中老年人的健康,对社会和经济造成巨大压力。因此,研究AD发病机制及寻求有效药物防治已成为目前世界医药界的热点和难点。氧化应激损伤神经元在神经退行性病变中具有重要的病因学意义。研究表明老年性痴呆与氧化应激损伤密切相关。H2O2是和氧化应激反应密切相关的活性氧之一,它参与了许多
神经系统疾病的发病,与多种疾病如自身免疫病,肿瘤,炎症以及细胞凋亡的发生有关,长期用作神经细胞氧化损伤的诱导剂。
蜂胶(Propolis) 被誉为“紫色黄金”,是蜜蜂从植物新生枝嫩芽或花蕾处采集的树脂类物质,掺入其舌腺及蜡腺分泌物,经蜜蜂反复混合而成的胶状物质。蜂胶富含多种具有药用价值的活性成分,其中主要是黄酮类化合物。本课题组前期研究发现蜂胶醇提物对东莨菪碱、亚硝酸钠、三氯化铝诱导的小鼠学习记忆障碍模型具有明显保护作用,对D-半乳糖诱导衰老模型小鼠学习记忆功能也有保护作用,其作用机制可能与其对抗小鼠体内过氧化反应有关[1-2]。通过MTT、流式细胞术等前期研究也发现蜂胶黄酮能有效的保护H2O2诱导的PC12细胞损伤,提高细胞存活率,抑制细胞凋亡,为进一步研究其抗痴呆作用奠定了基础。
PC12细胞为大鼠肾上腺嗜铬细胞瘤细胞,在细胞形态,结构,功能上与多巴胺神经元有许多相似特征,能够表达多巴胺转运体,是体外神经细胞损伤及保护作用研究使用最为广泛的细胞系。
本实验拟培养大鼠肾上腺髓质嗜铬细胞瘤细胞PC12细胞株,以H2O2诱导神经细胞损伤,
蜂胶黄酮干预, TUNEL 染色观察蜂胶黄酮的抗凋亡作用,并通过检测细胞周期、活性氧及Caspase-3对蜂胶黄酮的抗凋亡机制进行研究。
2 仪器与试剂
2.1 材料和试剂
蜂胶原胶,购自山东省实验种蜂场;PC12 细胞(大鼠肾上腺嗜铬细胞瘤细胞株),购自南京凯基生物技术有限公司;二甲基亚砜(DMSO)、胰蛋白酶、PBS,购自于索莱宝;完全
1
泰山医学院本科毕业设计(论文)
DMEM 培养基、新生牛血清(NBS),购自于南京凯基生物技术有限公司;TUNEL细胞原位凋亡测定试剂盒、活性氧试剂盒及细胞周期检测试剂盒(购自于南京凯基生物技术有限公司)、ELISA试剂盒(蓝基生物技术有限公司)。其它试剂均为分析纯。
2.2 仪器
二氧化碳孵箱(Thermo);单人双面超净工作台(SW-CJ);倒置式生物显微镜(XDS-1B);酶标仪(Infinite f200);流式细胞仪(FACSCalibur);高速离心机(TGL-16G);数控超声波清洗器(KQ-600DB);旋转蒸发仪(RE-52A 上海亚荣生化仪器厂)、恒温干燥箱(施都宝Bao-80A)、恒温水浴锅(HW.SY21-K)、超低温冰箱(Thermo)。
3.实验方法
3.1蜂胶黄酮的提取与含量测定
取蜂胶50g粉碎,用85%乙醇浸泡4天,配料比蜂胶(g):85%乙醇(ml)为1:30,在30℃条件下超声50min后,旋转蒸发仪蒸发成浸膏状,冰箱4℃内保存备用。以芦丁为标准品,得标准曲线y=13.656x+0.0404, R=0.9969,计算蜂胶中黄酮含量为:4.86mg/g。 2
3.2 PC12细胞的培养及分组给药
在37℃,恒湿的5%CO2细胞培养箱内培养PC12细胞,完全培养基为高糖DMEM培养基中含10%新生小牛血清,加入100 μg/ml链霉素和100 μg/ml氨苄青霉素。细胞为上皮样贴壁生长,每2~3 d传代1次,取对数生长期细胞用于实验。将细胞分为五组:空白对照组、模型组、蜂胶黄酮高、中、低剂量组。加药前先将蜂胶黄酮溶于DMSO中,再用完全培养基稀释,使药物终浓度为200 mg/L、100 mg/L、50mg/L,DMSO终体积为1?,空白对照组及模型组加入含1?DMSO完全培养基。药物预处理2h后,再加入H2O2培养24h,24h后检测
各项指标。
3.3 TUNEL细胞凋亡原位试剂盒检测
细胞以2×10个/孔接种量接种于24孔带爬片的培养板上,药物分组处理后,取出爬片,自然晒干后用4%多聚甲醛室温固定20-30min,PBS漂洗三次,每次5min,1%TritionX-100通透5min,PBS漂洗,3% H2O2封闭10min,PBS漂洗吸干,每个样本滴加50μlTdT酶反应液,加盖玻片放入温盒,37℃避光反应60min,PBS漂洗吸干,加5oμlStreptavidin-hrp工作液,加盖玻片放入温盒,37℃避光反应30min,PBS漂洗吸干,加50μlDAB工作液,反应5min,显微镜下观察,拍照。 5
3.4 流式细胞仪检测细胞周期
细胞以1×10个/孔的接种量接种于6孔培养板上。药物分组处理后,加入不含EDTA的胰酶消化,加培养基终止消化,PBS冲洗2次,加入2ml-20℃预处理12h的70%乙醇固定24
2 6
泰山医学院本科毕业设计(论文)
小时后,离心5min(小于1000r/min),弃去乙醇,每管加入PBS洗两遍,将细胞混悬后离心5min(小于1000r/min),按照1:50的RNaseA和PBS,37℃恒温水浴锅水解30min,过20目细胞筛于流式管内,加入5μl PI染色10-15min,流式细胞仪测细胞周期。通常用细胞增殖指数PI( pro liferation index)作为衡量细胞增殖的指标,PI即指处于DNA 合成期及有丝分裂期的细胞在全部细胞中所占比例,公式表示为: PI= [ ( S+ G2 /M ) / ( G0 /G1 + S+G2 /M) ]*100%
3.5 流式细胞仪检测细胞内活性氧
细胞以1×10个/孔接种量接种于6孔培养板上,药物分组处理后,加入不含EDTA的胰酶消化,加培养基终止消化,提取细胞,PBS离心冲洗2次,收集于流式管中,离心5min(1000r/min),按照1:1000有用无血清的培养基稀释DCFH-DA,去PBS加入稀释好的DCFH-DA,37℃孵育20min,3-5min摇匀一次使充分安装探针,PBS洗三次,流式仪测细胞内氧自由基含量。 6
3.6 Elisa检测Caspase-3
细胞以1×106/孔的接种量接种于6孔培养板上。药物分组处理后,加入不含EDTA的胰酶消化,加培养基终止消化,提取细胞,PBS洗三次,加微量PBS反复冻融三次,每次半小时,使细胞离解,细胞液检测Caspase-3含量,取试剂盒至于室温平衡30min,再取酶标板按照标准品的次序加50μl于空白孔,空白孔加50μl样品,空白50μlPBS,在每个空加100μl酶标记溶液(不含空白孔),封口37℃培养箱孵育1h(时间可适当延长),反复充分洗5次,拍干,各加50μlA.B显色剂,避光37℃孵育15min,加50μl终止液,450nm检测OD值。
4 实验结果
4.1 蜂胶黄酮对细胞凋亡的影响
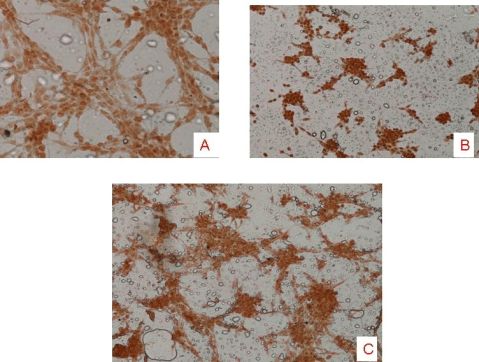
蜂胶黄酮作用2h后加入终浓度为140μmol/L H2O2作用24h后做TUNEL原位细胞凋亡染
色,结果图1所示,蜂胶黄酮组颜色明显低于H2O2损伤组,说明蜂胶黄酮的凋亡率比模型
组明显降低。
3
泰山医学院本科毕业设计(论文)
图1 TUNEL染色观察蜂胶黄酮对H2O2损伤保护作用
(A空白对照组×200 B H2O2损伤组×100 C蜂胶黄酮保护组×100)
4.2 流式细胞仪法检测细胞周期
与空白组比较,给予H2O2后,G0/G1期细胞明显增多,G2/M、S期细胞明显减少(P<0.01),细胞增殖降低,而蜂胶黄酮组G0/G1期细胞明显减少,G2/M、S期细胞明显增多,说明蜂胶黄酮具有促进细胞增殖(P<0.05)。其中蜂胶黄酮组S期细胞增加较多,说明蜂胶黄酮可能会促进细胞有丝分裂。结果见表1、图2。
表1蜂胶黄酮对细胞周期的影响
分组
空白对照组 模型组
G0/G1 47.62±3.2** 63.34±2.5 54.61±1.62** 57.85±1.23* 61.83±1.00
G2/M 17.31±1.71** 10.75±0.98 8.97±0.84 9.92±1.11 8.89±1.79
S 35.07±2.51** 23.42±3.55 34.48±1.54** 32.17±1.40* 29.29±1.04
增殖指数(PI) 52.38±3.22** 34.17±3.81 45.39±1.61** 41.15±1.23* 38.18±2.42
(H2O2140μmol/L)
蜂胶高剂量组
( 200 mg/L)
蜂胶中剂量组
( 100 mg/L)
蜂胶低剂量组
( 50 mg/L)
4
泰山医学院本科毕业设计(论文)
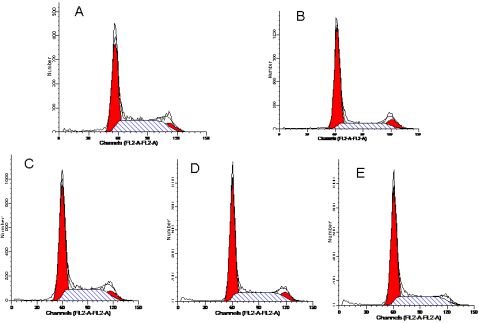
图2蜂胶黄酮对细胞周期的影响
(A空白组B模型组C蜂胶黄酮高剂量组D蜂胶黄酮中剂量组E蜂胶黄酮低剂量组)
4.3蜂胶黄酮对细胞内活性氧水平的影响
与空白组比较,给予H2O2后,细胞内活性氧水平明显提高(P<0.05),而蜂胶黄酮各剂量组能明显降低细胞内活性氧水平(P<0.01),且具有剂量依赖性,结果见表2、图3。
表2 蜂胶黄酮对细胞内活性氧水平的影响(?x±s, n=3)
组别 空白组 模型组 ( H2O2140μmol/L) 蜂胶黄酮高剂量组 ( 200 mg/L) 蜂胶黄酮中剂量组 ( 100 mg/L) 蜂胶黄酮低剂量组 ( 50 mg/L ) 活性氧( mg/ml ) 76.36±1.83** 171.79±24.01 82.75±14.73** 103.27±15.20** 151.96±26.70*
注:与模型组比较*P<0.05,**P<0.01。
5
泰山医学院本科毕业设计(论文)
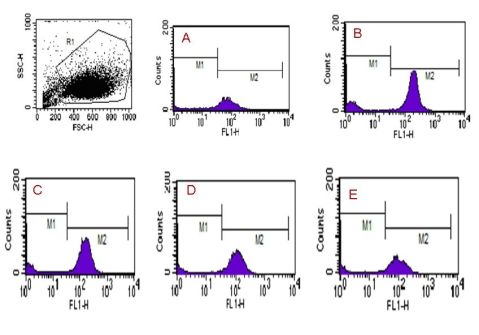
图3 蜂胶黄酮对细胞内活性氧水平的影响
(A空白组B模型组C蜂胶黄酮高剂量组D蜂胶黄酮中剂量组E蜂胶黄酮低剂量组)
4.4蜂胶黄酮对细胞内Caspase-3蛋白含量的影响
与空白组比较,给予H2O2后,细胞内Caspase-3蛋白含量明显提高(P<0.05),而蜂胶黄酮各剂量组能明显降低细胞内Caspase-3蛋白含量(P<0.01),说明蜂胶黄酮可抑制凋亡因子的产生。结果见表3。
表3蜂胶黄酮对细胞内Caspase-3蛋白含量的影响(?x±s, n=3)
组别 空白组
模型组
( H2O2140μmol/L)
蜂胶黄酮高剂量组
( 200 mg/L)
蜂胶黄酮中剂量组
( 100 mg/L)
蜂胶黄酮低剂量组
( 50 mg/L )
注:与模型组比较*P<0.05,**P<0.01。
6
Caspase-3( ng/ml ) 7.74±3.09** 34.63±1.19 13.98±4.13** 25.56±3.19** 29.79±2.46*
泰山医学院本科毕业设计(论文)
5 讨论
PC12细胞在细胞生物学特征上和某些神经元在发生上都源自神经嵴细胞,因此在国内外广为用作研究神经细胞的模型[3]。H2O2对细胞的损伤是通过在代谢过程中产生活性氧
[4](ROS),ROS再引发一些氧化毒性产物的细胞毒作用损伤细胞。本实验通过H2O2损伤PC12
细胞,蜂胶黄酮作用细胞,TUNEL细胞凋亡原位检测染色,流式细胞仪检测细胞活性氧水平和细胞周期,ELISA检测细胞内Caspase-3蛋白含量,结果显示,TUNEL细胞凋亡原位检测染色,蜂胶黄酮组颜色明显低于模型组且接近空白组,说明蜂胶黄酮各剂量组明显降低3-OH断裂诱导的细胞凋亡作用[5、6]。细胞周期检测中,与空白组比较,给予H2O2后,G0/G1
期细胞明显增多,G2/M、S期细胞明显减少,细胞增殖降低,而蜂胶黄酮组G0/G1期细胞明显减少,G2/M、S期细胞增加,说明蜂胶黄酮具有促进细胞增殖的潜势。通过流式细胞仪检测细胞活性氧水平,蜂胶黄酮组明显低于模型组且接近空白组,说明有清除细胞内氧自由基,抗氧化作用;ELISA检测细胞内Caspase-3蛋白含量,蜂胶黄酮组明显低于模型组且接近空白组,说明抑制细胞凋亡因子产生,减少细胞凋亡,并且随蜂胶黄酮浓度增大效果更加明显,所以还具有一定的剂量依赖性。以上实验结果均显示蜂胶黄酮对PC12具有明显的抗凋亡作用。
TUNEL细胞凋亡检测试剂盒是用来检测细胞在凋亡过程中细胞核DNA的断裂情况,其原理是生物素标记dUTP在脱氧核苷酸末端转移酶的作用下,可以连接到凋亡细胞中断裂DNA的3-OH末端,并可与连接辣根过氧化酶的链酶亲和素特异结合,在辣根过氧化酶底物二氨基联苯胺的存在下,产生很强的颜色反应(深棕色),特异准确的定位正在凋亡的细胞,因而在普通显微镜下即可观察和计数凋亡细胞;由于正常的或者正在增殖的细胞几乎没有DNA的断裂,没有3-OH的形成,很少能够被染色。
流式细胞仪检测细胞内活性氧水平,是一种利用荧光探针DCPH-DA进行的活性氧检测的试剂盒,DCFH-DA本身没有荧光,可以自由穿过细胞膜,进入细胞后,可以被细胞内的酶水解生成DCFH,而DCFH不能通过细胞膜,从而使探针很容易被装载到细胞内,细胞内的活性氧使无荧光的DCFH生成有荧光的DCF,检测DCF的荧光就可以知道细胞内的活性氧水平,实验结果显示,模型组细胞活性氧水平明显高于正常组与蜂胶黄酮组,说明H2O2可使细胞过氧化,而蜂胶黄酮的三个剂量组细胞活性氧水平率稍高于正常组,明显低于模型组,说明蜂胶黄酮对细胞有保护作用,可清除细胞内氧自由基水平。
7 [9][8][7]
泰山医学院本科毕业设计(论文)
Caspase-3是调控凋亡最直接的基因,被称为凋亡的执行者,在许多凋亡过程中,Caspase-3被凋亡信号激活后由其前体形式转变为成熟的酶,介导下游的凋亡效应,在正常细胞中以酶原形式存在,氧自由基等刺激因子使线粒体通透性增加,线粒体跨膜电位下降,释放细胞色素C,细胞色素C主要激活Caspase-9,进而激活下游的Caspase-3,引起细胞形态的变化如出现皱缩、DNA裂解、染色体浓缩和凋亡,小体的形成,最终导致细胞凋亡[10]。
本文结果表明,蜂胶黄酮在抗H2O2对PC12细胞的凋亡发挥抑制作用的机制可归结为减少G0/G1细胞,增加 G2/M、S期细胞,而促进细胞增殖;抗氧化、清除氧自由基作用,与自由基直接结合,阻止Caspase-3蛋白活化。
本研究结果表明蜂胶黄酮具有抗PC12神经细胞凋亡作用,为蜂胶黄酮的临床应用和AD病的临床治疗提供了极有意义的药理和药物学依据[11、12]。
6 结论
蜂胶黄酮对H2O2诱发PC12神经细胞凋亡有显著的抑制作用,其机制可能其影响细胞周期、清除氧自由基、降低凋亡因子Caspase-3有关。
8
泰山医学院本科毕业设计(论文)
参考文献
[1]王浩,张庆乐,许利军等.蜂胶醇提物对小鼠学习记忆的促进作用[J].中国蜂业,2008,59(8):5-6,9.
[2] 王浩,张庆乐,徐晓燕等.蜂胶总黄酮对衰老小鼠学习记忆影响的实验研究[J].中国老年学杂志,已接收.
[3]ISH ISAWA R, UTSUMI K, UTSUM I T . Involvement of lysosomal cysteine proteasis in hydrogen peroxideinduced apoptosis in HL- 60 cells [J]. Biosci B iotechnol B iochem,2002, 66 ( 9 ) :1865-1872.
[4] 徐颖.方金凤,顾岚,蜂胶黄酮清除自由基作用的研究_20xx年《 食品工业 》第一期
[5] 杨明,朱姝,隋殿军等. 蜂胶总黄酮对大鼠心肌缺血 -再灌注损伤诱导细胞凋亡的影响
[J].中国药理学通报,2005,21(5)551-554
[6] 宋明旭, 杨吉成, 王蔚平. 谷氨酸诱导的PC12细胞损伤的研究. 苏州科技学院学报. 2006,23(1): 62-65.
[7] 费洪荣, 王李梅, 王凤泽-泰山白首乌醇提物对HepG2肝癌细胞增殖与凋亡的调节作用.
[8] 谢大兴_..细胞周期检测点的流式细胞术分析2009,31(1): 1-3
[9] 曹炜,尉亚辉 等.蜂胶对氧自由基和四氧嘧啶致小鼠肝脏损伤的保护作用[J].中草药,
[10] 闻春生,应斌武,张永刚,槲皮素对肺腺癌细胞株A549细胞 caspase-3表达的影响 2000,15(1):67-71.
[11]Shafer TJ, Atchison WD. Transmitter, ion channel and receptor properties of pheochromocytoma (PC12) cells: a model for neurotoxicological studies.
-492. [12]
of mechanisms and potential avenues for therapy. Curr Opin Pediatr. 1999, 11(3): 223-228.
9
泰山医学院本科毕业设计(论文)
文献综述
蜂胶主要成分及药理作用
摘要: 蜂胶中的活性物质主要为类黄酮,研究证明其具有抗氧化、抗炎及保护心脑血管;提高免疫力的作用; 抑菌、抗病毒、抗炎作用从而促进伤口愈合和组织修复。此外蜂胶中的类黄酮物质还有预防肿瘤等药理作用。
关键词:蜂胶;类黄酮;抗氧化;抗菌;抗病毒;增强免疫;抗肿瘤
1 蜂胶的来源及其化学成分
蜂胶是工蜂从植物的新生支条、叶、芽或树皮等组织上采集到树脂状分泌物后混入其上颚腺等腺体的分泌物和蜂蜡等加工而成的芳香性胶状物,含有与胶原植物相类似的大量有效成分。蜂胶的化学成分很复杂,我国蜂胶成分主要含有三类,酚酸及醛类、黄酮类、酚酸酯类;含有大量的黄酮类、萜烯类化合物是蜂胶的重要特征,现已从蜂胶中分离鉴定的黄酮化合物有30余种,包括白杨素、柚柏杨素、芹菜素,金合欢素、槲皮素、高良姜素、芦丁、山萘酸、山萘甲黄素、鼠李素、松属素等,其5,7-二羟基-3,4-二甲黄酮和5-羟基4,7-二甲氧基双氢黄酮是蜂胶的特有成分,蜂胶大部分的生理及药理功能都与此类化合物有密切关系。蜂胶所含有的丰富的黄酮类、萜烯类物质是蜂胶的最大特点。它赋予蜂胶许多奇妙而独特的生物学作用。蜂胶成分复杂、作用广泛,让科学家感到惊奇,人工无法合成类似的产品。
2 蜂胶的药理作用
蜂胶具有抗氧化、抗炎、预防动脉粥样硬化、降血糖、抗肿瘤、免疫调节抑菌等多种生物学活性,体内外实验验证蜂胶及其主要活性成分生物学活性作用的分子机制是近年来研究的热点。
2.1 抗氧化作用
已知有许多常见的疾病,如癌症、动脉硬化、糖尿病、白内障、心血管病、老年痴呆、关节炎等,都被认为与自由基相关。蜂胶中含有大量的抗氧化活性成分,关于蜂胶抗氧化的研究从未间断过。蜂胶能抑制2,2’-偶氮(2-脒基丙烷)二盐酸盐诱导的人红细胞氧化溶血现象和脂质过氧化,有效保护溶血红细胞膜,使红细胞中脂质过氧化的分解产物丙二醛水平降低,且呈现时间和剂量依赖性。蜂胶能有效抑制低密度脂蛋白的脂质过氧化和酪氨酸硝基化,减少内皮型一氧化氮合酶的表达,抑制内皮细胞还原型辅酶Ⅱ(NADPH)氧化酶的活性,说明蜂胶是通过增加血管内皮细胞中一氧化氮的生物利用度而发挥潜在的心血管保护作用的。
10 [2][1]
泰山医学院本科毕业设计(论文)
2.2 抗炎作用
蜂胶对血管内皮细胞的影响具有剂量依赖性,低浓度的蜂胶能保护血管内皮细胞,而高浓度蜂胶却会诱导血管内皮细胞凋亡,具有细胞毒性。在去除血清和生长因子的条件下,高剂量的蜂胶能破坏线粒体膜电位,是潜在的凋亡诱导剂,而低剂量的蜂胶能显著降低膜整连蛋白β4、PC-PLC、P53和ROS水平,保护血管内皮细胞。在脂多糖(LPS)诱导的血管内皮细胞中,蜂胶能降低TLR4的表达和PCPLC的活性,进而抑制下游信号分子NF-Kb p65、p53、ROS和NO的水平,抑制LPS诱导的血管内皮细胞损伤。在ox-LDL诱导的血管内皮细胞损伤条件下,蜂胶均能降PC-PLC的活性和ROS的水平,抑制ox-LDL诱导的血管内皮细胞损伤。有研究发现,蜂胶水提取物对海绵植入小鼠的血管生成、炎症细胞聚集和内源性细胞因子能产生影响,表明蜂胶的抗炎症和抗血管生成作用与细胞因子调控有关。
2.3 预防动脉粥样硬化
蜂胶乙醇提取物可有效增加高密度脂蛋白胆固醇,减少动脉粥样硬化的风险。将3H-胆固醇载货巨噬细胞经腹膜内注入到灌服蜂胶乙醇提取物的小鼠体内,可导致血浆、肝脏和粪便中的高密度脂蛋白胆固醇和腹膜巨噬细胞3H-胆固醇显著增加,肝脏蛋白质三磷酸腺苷结合盒转运体A1和三磷酸腺苷结合盒转运体G1表达增加。细胞株HepG2和RAW264.7的体外实验也证实了上述结果。这些研究表明,蜂胶乙醇提取物增强胆固醇的逆向转运可能是由于蜂胶乙醇提取物刺激血浆高密度脂蛋白水平和肝三磷酸腺苷结合盒转运体A1和三磷酸腺苷结合盒转运体G1表达所致。
2.4 降血糖作用
利用链脲霉素构建1型糖尿病大鼠模型,链脲霉素+高脂饲料构建2型糖尿病大鼠模型,研究蜂胶改善糖尿病肾病可能的作用机理。结果发现,蜂胶能有效改善1型糖尿病和2型糖尿病对大鼠造成的损伤。蜂胶均能抑制糖尿病大鼠体重下降,改善大鼠血液糖代谢、脂质代谢、蛋白代谢以及血液、肝、肾氧化应激。通过测定肝肾功能相关指标及组织切片观察,结果表明蜂胶能改善糖尿病大鼠肝肾功能。蜂胶的效果发现,蜂胶对血糖的控制效果和肝脏的保护效果、改善氧化应激的效果都很强。对维持糖尿病大鼠血糖稳定和防止骨骼发生变化具有显著作用。
2.5抗肿瘤作用
蜂胶中含有丰富的抗癌物质。研究证明,癌症患者在服用蜂胶后,可缩小癌细胞且能减轻化疗、 放疗引起的副作用。目前,蜂胶中抑制癌细胞的成分已被鉴定出来,主要是caffeic acid类的衍生物,在19xx年Grunberger等人便发现caffeic acid phenethyl ester(CAPE)对细胞具有选择性的毒杀作用。CAPE可以抑制致癌基因的表现,可以诱导这些不正常细胞
11 [5][4][3]
泰山医学院本科毕业设计(论文)
进行细胞凋亡作用(apoptosis),对正常的细胞则否。对於受到致癌物质诱导转型的不正常细胞,CAPE同样也可以使它们产生细胞凋亡作用。
2.6 免疫调节活性
蜂胶能明显抑制同种异体CD4 T细胞的增殖,激活和抑制这些同种异体CD4 T细胞中IL-2、IFN-γ和IL-17的表达。蜂胶能选择性地诱导增殖T细胞的凋亡,抗增殖作用是可逆的,也适用于活化的T细胞。蜂胶可用于移植物抗宿主病的免疫抑制剂。
2.7抑菌作用 [7][6]
蜂胶乙醇提取物对外阴阴道念珠菌具有抗真菌活性,为外阴阴道念珠菌病的治疗和预防提供了重要信息。蜂胶对Trichophyton violaseum、Triehophyton tonsorans和
Epidermophyton flucosum 3种皮肤癣菌有很好的抗真菌作用。巴西绿蜂胶提取物能抑制头癣和花斑癣,其作用效果堪比达克宁,可作为替代药用于治疗癣菌病。抑菌活性的研究拓展了蜂胶的应用范围。
另外吕泽田等报道了蜂胶中黄酮类化合物抑制肿瘤作用的试验与应用,结果表明高剂量治疗组小鼠瘤的抑制率为30%;中剂量组小鼠腹腔巨噬细胞吞噬率及各剂量吞噬指数显著高于对照组;高、中剂量组小鼠的脾脏(NK)自然杀伤细胞活性(%)亦显著高于对照组。韩连堂等报道蜂胶对移植的小鼠S180肉瘤、肝癌具有明显的抑制作用,其可能的抗癌机制包括:(1)抗氧化作用;(2)减少致癌物的合成、吸收和活化;(3)对细胞的分化、增殖、基因表达的影响;(4)对DNA损伤与修复的作用;(5)促进癌细胞凋亡;(6)对细胞的连接通讯的作用;(7)对机体免疫功能的作用。张建等对蜂胶提取物进行体外抗肿瘤实验,结果表明:山东蜂胶乙醇提取物和乙醚提取物在体外对肿瘤细胞均具有较强的抑制作用。蜂胶乙醇提取物诱导肿瘤细胞凋亡的研究表明,肿瘤细胞经蜂胶处理后,细胞形态呈现固缩,核染色质固缩致密,DNA 电泳分析显示特征的梯度形图谱;流式细胞仪检测细胞周期,凋亡峰增高,且G0-G1与C2-M期百分比增高,凋亡控制基因bel-2 基因表达的同时,激活了凋亡相关基因,启动了细胞凋亡过程,表明蜂胶抗肿瘤作用是通过诱发细胞凋亡实现的。韩连堂等应用Ames试验分别检测蜂胶对环磷酰胺、叠氮钠、正定霉素、2-氨基芴诱发突变的抑制作用,结果显示:蜂胶对4种诱变剂的不同类型的基因突变均产生抑制作用,证明蜂胶具有广谱的抗诱变作用,其抑制基因突变的作用机制可能是对基因突变过程中的多个环节产生作用而显示其抗诱发活性。
蜂胶除了具有上述的保健作用外,还有抗病毒、护肝、抗疲劳、调节血脂、改善代谢等作用。
12 [9][8]
泰山医学院本科毕业设计(论文)
3 蜂胶的临床应用
蜂胶具有抗菌、抗病毒、抗溃疡、抗炎、降血压、增强免疫力等作用。在很多国家蜂胶被作为民间药物使用。
3.1 对糖尿病的治疗作用
糖尿病是最常见的慢性病之一, 在中国的发病率达到2%, 发病机理为胰岛素绝对或相对分泌不足以及靶组织细胞对胰岛素敏感性降低, 引起蛋白质、脂肪、水和电解质等一系列代谢紊乱综合症。目前, 世界上还没有一种药物可以根治糖尿病。蜂胶中含有胰蛋白酶等多种活性酶和其他抗病毒物质, 对恢复胰脏机能有明显的作用, 同时, 蜂胶中含有的B 族维生素, 又可能成为胰脏制造胰岛素的料。如果蜂胶与蜂王浆合用, 对糖尿病会有更好的疗效。
3.2 增强免疫力
在影响人体健康的诸多因素中, 自身免疫功能失调, 是最核心、最本质的因素。蜂胶通过调节人体生理功能, 激发免疫细胞活力和自然杀伤细胞活性, 促使丙种球蛋白增长, 增加抗体产量, 显著增强免疫能力, 在人体内培育抗病力与自愈力。蜂胶增强免疫功能体现在免疫防御、免疫自稳、免疫监视三方面, 即机体对病菌、病毒的抗感染能力, 识别和清除自身衰老的组织细胞的能力, 杀伤和清除异常突变细胞、抑制恶性肿瘤生长的能力。
3.3 促进皮肤健康
临床实验表明: 蜂胶对皮肤瘙痒症、神经性皮炎、射线皮炎、日光性皮炎、毛囊炎、汗腺炎、脂溢性脱发、斑秃、青年痤疮等有效; 对物理性皮肤病, 如烧伤、烫伤、冻疮、手足皲裂有效,有促进伤口愈合与黏附伤口的作用。同时, 蜂胶抗菌消炎作用强, 局部止血止痛快, 能促使上皮组织增生和肉芽生长, 改善皮下组织血液循环, 限制疤痕形成。同时蜂胶对皮肤过敏、皮肤搔痒、头皮屑、头皮疹、湿疹、药症均有效果。
3.4 抑制癌症的作用
蜂胶具有抗癌广谱性, 能抑制致癌物质代谢活性, 增强正常细胞膜活性, 分解癌细胞周围的纤维蛋白, 防止正常细胞癌变或癌细胞转移。同时蜂胶中含有多种对肿瘤细胞生长有抑制作用的物质, 其中以栎精(槲皮素、五羟黄酮)、咖啡酸苯乙酯、clerda 二萜烯、金雀异黄酮和菲瑟酮等化合物的作用最强, 这些成分除了对人类的肝癌细胞有抑制作用, 对人类的宫颈癌细胞和淋巴癌细胞也有作用。亚硝酸胺和黄曲霉素是目前所了解的具有高致癌力的物质, 蜂胶中的酚类和酸类化合物可以阻断机体内亚硝酸胺的合成, 蜂胶中的黄酮类化合物可以诱导机体分泌苯芘羟化酶, 以解除黄曲霉素类等致癌物对机体的毒害。
3.5 对胃肠道疾病的作用
13
泰山医学院本科毕业设计(论文)
对于慢性胃肠炎患者, 常给服抗生素类药物, 以抑制炎症发展。但是, 经常服用化学合成的抗生素, 容易导致人体消化道寄生菌群比例失调。实验表明: 食用蜂胶, 对慢性胃肠炎, 效果显著, 而且不会造成人体消化道寄生菌群比例失调。同时蜂胶具有良好的成膜性, 能够在粘膜上形成一层酸不能渗透的薄膜。利用蜂胶这一特性, 人们应用它治疗胃及十二指肠溃疡, 可获得较好的疗效。除了上述临床作用, 蜂胶对更年期障碍也具有调节作用。因蜂胶具有镇静、麻醉及其他神经系统作用, 使它具备了治疗失眠、止痛及各种神经系统疾病的功效。此外, 蜂胶在预防和治疗龋齿和口腔炎方面效果也很显著。
蜂胶具有广泛的生理及药理功能,开发前景极为广阔, 拟被列为世界卫生组织营养与保健计划内的一种保健品。随着人们对其认识和研究的深入, 经过足够时间的考查, 蜂胶以其资源丰富、效果显著、提取方便等优点, 将会成为很有前途的新药和天然保健品。
14
泰山医学院本科毕业设计(论文)
参考文献
[1]王玉芬;蜂胶的研究进展[J];河北医药;20xx年03期:227-229
[2] Valente MJ, Baltazar AF, Henrique R, Estevinho L, Carvalho M.Biological activities of Portuguese propolis: Protection against freeradical-induced
erythrocyte damage and inhibition of human renalcancer cell growth in vitro[J].Food Chem Toxicol, 2011, 49: 86-92.
[3] Silva V, Genta G, Moller MN, Masner M, Thomson L, Romero N, RadiR, Fernandes DC, Laurindo FRM. Antioxidant activity of Uruguayanpropolis. In vitro and cellular assays[J].J Agr Food Chem, 2011, 59:6430-6437.
[4] De Moura SAL, Ferreira MAND, Andrade SP, Reis MLC, Noviello ML,Cara DC. Brazilian green propolis inhibits inflammatory angiogenesisin a murine sponge model[J].Ecam, 2011, 182703, 7. T, Polak T, Gasperlin,2010, 29:130-137.
[5] 吴粹文 张复兴.真理蜂胶营养液调节血脂作用的研究[J].中国养蜂,20xx年01期:
121-124
[6] 华启云,李英华,胡福良;蜂胶血糖作用的研究进展[J];蜜蜂杂志;20xx年02期:42-46
[7]王泽剑,聂宝明,殷明等.人参炔醇对氧应激诱导大鼠海马神经细胞凋亡的影响[J].中国药学杂志2007,42(13)987-990.
[8]李淑华,于晓红,于英君,杨宝华,张德山;蜂胶对免疫功能低下模型鼠细胞免疫功能的影响[J];中医药学报;20xx年03期:66-71
[9] 唐传核 孟岳成.蜂胶的生理功能以及开发研究[J].食品工业科技, 20xx年04期:11-13
15
泰山医学院本科毕业设计(论文)
致 谢
16 学生:*** 20xx年6月18日
-
药学院20xx年本科毕业实验类论文格式要求
20xx本科毕业实验类毕业汇报材料格式要求20xx修订本科毕业论文设计是学生所学知识的实际运用它集中表明了作者在专业学习中获得的新…
-
工程类专业毕业设计(论文)格式规范
工程类专业毕业设计论文格式规范一基本规范要求的内容1毕业设计论文文本结构规范中外文摘要扼要叙述本设计的主要内容特点文字要精练中文摘…
-
毕业论文类型
一毕业论文的类型分为专题型论辩型综述型和综合型四大类二毕业论文的规格学年论文毕业论文硕士论文博士论文三毕业论文是大学生在大学的最后…
-
实验类毕业论文模板
XX学院毕业论文题目的研制学生姓名学号系院专业班级指导教师姓名及职称教授实验师起止时间20xx年4月20xx年12月教务处制表的研…
-
毕业论文格式模版(实验类)
说明1全文A4纸双面打印上下左右页边距均为25cm行间距15倍2除规定外其余内容均为宋体小四3每段首行缩进2字符3从论题页开始插入…
-
1-1实验型毕业论文格式及内容撰写方式模版(定稿用)
武汉生物工程学院本科论文设计目录学位论文作者声明II摘要III关键词IIIAbstractIIIKeywordsIII1前言一级标…