国家自然科学基金酸菜版标书范文
20##年国家自然科学基金面上项目
示例版
题目:真核起始因子X-Y轴调控糖基转移酶对肠癌肝转移的作用机制
摘要:
大肠癌术后复发转移中,肝、肺转移是最常见的转移模式,对其机制一直未能阐明。申请者在前期工作中建立了大肠癌远处转移的特征分子谱式,在肝转移相关分子标志中,发现真核起始因子Z家族的成员:X和Y具有关键调节作用。X-Y轴能够介导大肠癌肝转移的发生,X可促进细胞获得运动能力,并且在转移灶中通过Y的相互作用促进细胞异常增殖。进一步实验证实,X能调节下游糖基转移酶,可能存在激活肠癌细胞膜表面半乳糖残基,从而通过与肝细胞膜上特异性受体相互作用而使肠癌细胞“定居”于肝脏的机制,可见X-Y调节轴对于大肠癌肝转移至关重要。本项目拟在此基础上,从大样本回顾性分析中总结X-Y对于结肠癌肝转移的临床相关性和预后判断价值。同时,在细胞和动物模型中进一步深入探讨其在结肠癌肝转移调控中的作用方式和调控分子机制,解析下游效应途径及靶点。
(一)立项依据与研究内容(4000-8000 字):
一、立项依据
大肠癌是一种发生在结肠或者直肠中的癌症,是最常见的恶性肿瘤之一,全球每年新发病人约八百万,占所有恶性肿瘤的10%-15%,其发病率和死亡率居恶性肿瘤的第三位[1]。随着手术、化疗、放疗水平的提高,大肠癌患者的生存率有了较大的提高,但远处转移是影响其预后的最主要因素。在美国大肠癌中有90%的死亡由肿瘤的远处转移所致[2]。所以,通过对大肠癌转移机制的研究,正确认识大肠癌术后转移模式,对于制定合理的术后随访方案,采取有针对性的干预措施,提高生存率至关重要。
大肠癌最常见的远处转移部位是肝脏和肺。对于肝转移,人们更多的把原因归结为解剖因素,结肠是通过门静脉系统回流进入肝脏,所以认为大肠癌的首发转移部位往往在肝脏。但是很多临床研究发现大肠癌患者术后转移可以绕开肝脏而首先出现在肺部甚至是甲状腺转移[3-6],有报道出现首发肺转移的大肠癌患者最高可达患者总数的6%,已经相当可观[7],这就对我们的随访策略提出挑战,对于大肠癌患者即使术后没有肝转移,也不能放松对肺部的检查。而申请者在前期临床研究中,通过对本院486例行根治手术的大肠癌患者资料研究后发现:主要通过门静脉系统回流的高位直肠癌和通过体循环回流的直肠中、低位直肠癌的术后肺转移率和肝转移率都没有显著性差异。由此可见,决定大肠癌的术后转移模式的因素并非仅仅解剖可以阐释。近年来研究发现包括原发肿瘤的分期,术前放化疗,转移靶器官的微环境等因素都会影响大肠癌的转移模式[8-10],但其确切机制仍然没有探明。
为搜寻大肠癌远端转移相关分子靶标并评估其作为预测远端转移发生的潜在分子标志物的可能性,我们前期在临床上收集了6例珍贵的同时性肝、肺转移分别切除的患者,将其原发灶、肝、肺转移的组织样本通过高通量的基因芯片技术,从全基因表达谱的角度对这两种转移组织的基因表达情况进行了全方位的检测分析(来源于同一患者的组织样本可以排除个体遗传背景的干扰)。我们发现:有41个基因在两种大肠癌远处转移组织中存在显著性差异(肝转移分子群有27个,肺转移分子群有14个),这些分子可能构成了驱动大肠癌不同转移模式的分子因素。为进一步确认芯片的结果,我们在47例大肠癌肝转移和22例肺转移组织病理样本中,通过qPCR的方式进行了回顾性验证,确认了13个在大肠癌肝转移过程中明显高表达的基因(5倍以上),区别于肺转移,这是一种特异性的表达改变(见前期工作)。
这些肝转移特异的分子标志中,有两个属于真核起始因子Z家族的成员:X和Y,引起了我们的研究关注。Z真核起始因子在真核生物翻译起始过程中起着重要作用,参与了真核生物翻译起始过程中的多个反应[11],但其在肿瘤中的角色功能还尚不十分清楚。我们首先鉴定了Y基因在大肠癌细胞中高表达,并确认Y表达被干扰后,细胞增殖能力被显著抑制,处于G1期的细胞数量显减少,处于S期和G2期的细胞数量显著增加,细胞凋亡比例显著提高,细胞的存活能力显著下降,克隆形成能力受到显著抑制。这一结果已发表于《XXX》[12]。考虑到有报道X与Y之间存在相互结合[13-14],我们又进一步观察了两者之间的交互作用。有意思的是,X对于Y的促恶性增殖功能是必需的,表现在沉默X表达之后,过表达Y对大肠癌细胞的增殖调控失活。而X本身具有调节细胞迁移的能力,抑制X可显著降低细胞运动性(见前期工作)。由此,我们提出科学假设:真核起始因子X-Y轴能够调控大肠癌肝转移的发生,X可介导细胞获得运动能力,并且在转移灶中调节Y发挥促进肿瘤细胞继发性增殖的作用,具体作用机制有待阐明。
在哺乳动物中,Z因子的亚基有8种,按分子量从大到小排列而命名[15]。Z因子参与真核细胞翻译过程,而调节蛋白合成在维持细胞生长控制中起重要作用[16]。据报道,Z因子不仅能通过促进mRNA与40s亚基结合,而且还可以独自与游离的40s亚基结合,影响40s亚基与60s亚基及其他亚基蛋白的结合或解离等[17]。Z家族成员一般含有PCI和MPN结构域,这两类结构域都参与蛋白-蛋白相互作用,部分还具有RNA识别(RNA recognition motif,RRM)结构域,可能参与RNA的结合[15]。除此之外,Z因子还被发现具有调控细胞周期的作用[16,18]。通过调节不同类型的mRNA的翻译起始,Z因子就可以选择性地调控蛋白的合成,从而对肿瘤细胞的生长的转移等生物学行为进行调控[16,19]。
Z家族中部分成员已证实在肿瘤的发生、发展中扮演重要角色,已报道的包括:A、B、C、D等[18-22]。Y的致癌作用由申请人首先报道,随后其在胶质瘤和呼吸系统肿瘤中的作用也被其他研究者发现 [12,23-25]。而关于X与恶性肿瘤的关系目前还未见文献报道,可见在针对X、Y两个分子尤其是交互作用方面,申请人尚居于领先的研究地位。
更早前,权威杂志J Biol Chem上的报道提示了X在包含Y蛋白的复合物与40S核糖体亚基结合的过程中扮演着关键的链接作用,缺失X时两者的结合很不稳定,对翻译起始系统的调节能力也会降低[26]。20##年9月,J Biol Chem上又报道了W可与X竞争性结合Y[27],从而形成不同的Z复合物。Z复合物负责招募tRNA或mRNA,可调节下游基因表达,继而影响肿瘤细胞的生长、迁移等生物学过程。不同的Z因子蛋白结合可能存在不同的翻译调节机制从而执行不同功能作用。
在近期的研究工作中,申请人对X的调控机制进行了进一步深入。敲减X后,基因芯片检测显示肠癌细胞中多个关键调控节点发生了改变。其中,有3个半乳糖基转移酶(β1,3-GalT; β1,4-GalT-1; β1,4-GalT-7)的表达降低了,这引起了我们的兴趣。糖基化作为常见的蛋白翻译后修饰,参与细胞增殖、分化、转移、侵袭、免疫应答等多种生命活动,糖基化紊乱能够导致多种肿瘤的发生与恶性转化,糖基转移酶的表达和活性与包括大肠癌在内的多种肿瘤的恶性化程度相关[28-29]。Tang等发现β1,4-半乳糖基转移酶1通过调节EGFR影响肝癌细胞的生长和凋亡[30]。β1,4-半乳糖基转移酶3通过调节整联蛋白信号通路影响神经细胞瘤的侵袭能力[31]。此外,半乳糖基转移酶的激活,可以使细胞膜上蛋白糖基化程度增加[32]。
经过进一步肠癌细胞株的体外实验验证,X与半乳糖基转移酶β1,4-GT-1和β1,4-GT1-7的表达正相关(见前期工作),我们推测X对半乳糖基转移酶的调节作用很可能是它在肠癌中介导肿瘤细胞肝转移的关键。原因在于,肝细胞表面存在一种特异性表达的抗原:去唾液酸糖蛋白受体(asialoglycoprotein receptor, ASGPR),又称半乳糖受体。ASGPR是一种跨膜蛋白,主要表达于哺乳动物肝窦状隙的肝实质细胞表面,密度很高,每个细胞表面可多达500,000个受体,其胞外结构域含有糖识别结构域,能识别和结合半乳糖残基和N-乙酰半乳糖胺残基[33]。Misawa等[34]曾经用神经氨酸酶处理骨髓细胞(Bone marrow cell,BMCs),使细胞膜表面的糖蛋白脱去唾液酸而暴露出半乳糖残基,利用半乳糖残基与ASGPR的相互作用使BMCs直接聚集到肝脏。我们相信,真核起始因子X在肠癌肝转移的过程中,可能调节下游糖基转移酶,存在一种通过激活肠癌细胞膜表面半乳糖残基,从而与肝细胞膜上特异性受体ASGPR相互作用而使肠癌细胞“定居”于肝脏的机制,此后,它又可介导Y的促进肿瘤细胞克隆化增殖的能力,最终形成肝组织肿瘤转移灶。X-Y调节轴对于大肠癌肝转移的内在调节机理是令人期待的。
在前期工作基础上,本项目拟从大样本回顾性分析中总结X-Y对于结肠癌肝转移的临床相关性和预后判断价值。同时,在细胞和动物模型中进一步深入探讨其在结肠癌肝转移调控中的作用方式和调控分子机制:解析X调节半乳糖苷转移酶表达的方式和作用靶点,明确其介导的信号通路,并确认X在Y复合物发挥功能的效应分子途径中的作用。以上研究在组织、细胞、动物三个层次展开,并通过分子机制研究进行纵向的突破,以期获得高水平的研究成果。
本项目是对结肠癌肝转移发生机制的研究深入,所获得的研究成果可帮助我们更好判断肠癌预后,通过肝转移特征性的分子标志,提示风险,并为相关靶点应用于临床转化医学奠定理论基础。
主要参考文献
因涉敏感基因信息,略
二、项目的研究内容、研究目标,以及拟解决的关键科学问题
1、研究内容
1) 回顾性检测500例肠癌患者手术标本中X和Y蛋白的表达水平,根据临床病理数据和随访数据多因素分析X、Y表达与肠癌肝转移发生的相关性,尝试建立基于X、Y表达的分子预测模型,评价这一预后指标的临床适用价值。
2) 在肠癌细胞株中过表达和沉默X、Y基因,观察细胞功能变化。在细胞实验基础上,应用裸鼠成瘤和肝转移动物模型进行验证,观察X、Y对于肠癌恶性增殖和转移发生的影响。结合细胞、动物和组织水平的研究数据阐明X、Y在肠癌发生、进展中的功能作用。
3) 根据前期工作的下游通路和靶分子分析结果,重点阐明:①X与糖基转移酶之间的调控关系和作用靶点;②X与细胞运动性信号通路靶分子的调节关系;③Y复合物调节的信号通路与效应分子;④X与Y相互结合的序列位点和精细调控。
2.研究目标及考核的技术指标
基于Y在肠癌细胞高表达能促进细胞恶性增殖和周期改变,X与Y之间存在相互结合,而X具有调节细胞迁移的能力,申请者的研究目标在于证实X-Y轴能够调控大肠癌肝转移的发生,X可介导细胞获得运动能力并在转移灶中调节Y发挥促进肿瘤细胞继发性增殖的作用。而在体内、体外明确其促肝转移功能作用基础上,X调控结肠癌细胞迁移的分子机制通过以下两个目标进行深入探讨:
1) 阐明Y复合物调节的信号通路与效应分子;
2) 确认X与Y相互结合的序列位点和精细调控;
3)探讨X调节大肠癌肝转移模式的具体作用机制。
3.拟解决的关键科学问题及其解决方法
本课题所需解决的第一个关键科学问题为X和Y在大肠癌肝转移中的临床意义,通过大样本组织中检测这两个分子的表达,并利用病理和随访数据进行统计分析,我们可以获得多因素条件下这两个靶标的临床价值。这其中,规范化的组织样本库,随访数据的积累以及统计方法的运用都是重要的影响因素,但申请者所在课题组在这方面从事过多个课题的研究,具有丰富经验。另一方面,这两个靶标的检测有成熟的商业化抗体,方法学上也不存在困难。
本课题第二个关键问题也是本课题研究的重点,即X-Y轴在大肠癌肝转移中的调控分子机制,我们需要阐明Y所介导的迁移功能及糖基转移酶信号途径的效应分子和作用方式,并且确认Y与X结合的精细调控及促进肿瘤细胞增殖的分子机制。这方面的工作依赖于扎实的前期工作,首先,我们已经得到Y和X沉默后功能表型的结果,即Y可调控细胞增殖,而X能够调节细胞迁移,并影响Y对肿瘤的促增殖作用,在此基础上做机制研究有的放矢。其次,我们已筛查和验证到X可通过调节两个糖基转移酶对肠癌细胞肝脏种植起到调节作用,在本课题中,我们需要深入做的工作是揭示X如何调节细胞迁移功能,其下游调节糖基转移酶是否与肝脏特异性的转移相关,以及它们具体的作用机制是怎样的。在逻辑清晰的机制通路假设中,我们只需逐条验证,即可真正揭开X作用通路的神秘面纱。最后,Y和X之间的cross-talk有创新性且立足于前期研究的数据支持,只需将X-Y复合物调节的位点和下游与细胞增殖功能相关的机制阐释清楚,即可形成完成的研究故事。考虑到肿瘤细胞增殖机制方面报道众多,可参考模式丰富,这方面的研究也不会有太大的科学风险。
三、拟采取的研究方法、技术路线、实验方案及可行性分析
1. 技术路线
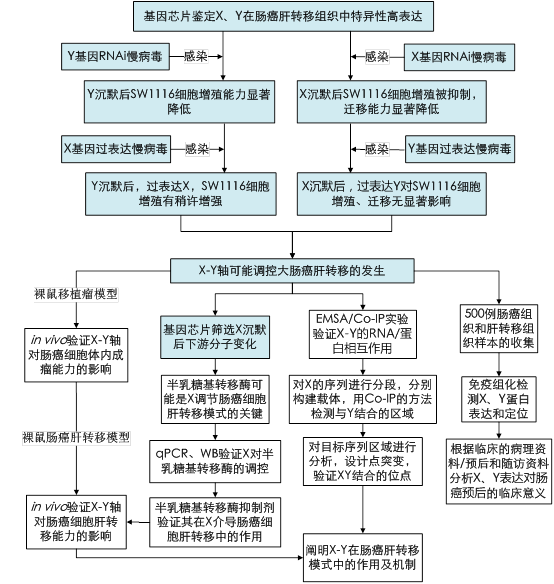 备注:蓝色背景填充部分为前期已完成工作。
备注:蓝色背景填充部分为前期已完成工作。
2. 研究方法
2.1 X、Y在结肠癌发生、发展中的作用和预后相关性
1) 回顾性收集肠癌临床标本500例,取手术切除的肠癌组织、匹配的肝脏转移灶手术和穿刺标本,新鲜组织液氮保存标本200例,石蜡块300例,全部病例均通过临床、影像学、病理诊断,术前未进行辅助治疗,来自某某医院20##-20##年临床收治病例,随访资料齐全。
2) 免疫组化检测组织切片中X、Y蛋白的表达及定位,分别设立阴性对照、肿瘤对照、肝转移对照。
3) SPSS16.0统计软件对X、Y表达及定位与临床标本进行病理关联性分析和预后统计分析,了解X、Y表达情况与相关临床资料之间的关系,单因素生存分析对临床各项指标与结肠癌生存期进行相关性分析,建立Cox比例风险回归模型,综合探讨临床各因素和X、Y表达与结肠癌肝转移、转移灶形成及预后的相关性。
2.2 体外、体内水平研究X、Y基因在肠癌肝转移中的调节功能
1) 制备X-shRNA慢病毒,建立X稳定沉默的细胞株,以无义序列作为阴性对照,利用MTT实验观察X沉默后细胞的生长曲线;克隆形成实验检测X沉默后细胞的克隆形成能力;流式细胞术结合PI单染、Annexin-V双染检测细胞周期和凋亡情况;细胞划痕实验、Transwell实验观察细胞运动能力的变化。与此同时,制备过表达X的慢病毒载体。
2) 在稳定沉默X的结肠癌细胞中,导入过表达Y的慢病毒载体,利用细胞生长曲线观察X沉默且Y过表达后细胞的增殖能力变化;细胞划痕实验、Transwell实验观察细胞运动能力的变化。同样地,在稳定沉默Y的结肠癌细胞中,导入过表达X的慢病毒载体,利用细胞生长曲线观察Y沉默&X过表达后细胞的增殖能力变化;细胞划痕实验、Transwell实验观察细胞运动能力的变化。
3) 制备结肠裸鼠皮下移植瘤模型,观察肿瘤生长情况,建立生长曲线,统计分析Y和X对结肠癌细胞体内成瘤能力的影响,明确Y和X在结肠癌恶性增殖的作用。实验分组:空白对照、Y沉默组、X沉默组、X沉默组+Y过表达组、Y沉默组+X过表达组。
4) 建立结肠癌肝转移动物模型,观察肝脏中的转移灶,统计分析Y和X对结肠癌肝转移能力的影响,明确Y和X在结肠癌肝转移过程中的作用。实验分组:空白对照、Y沉默组、X沉默组、X沉默组+Y过表达组、Y沉默组+X过表达组。
5) 处死裸鼠取得的肿瘤组织,利用qRT-PCR和免疫组化方法检测Y/X以及下游半乳糖苷酶的mRNA和蛋白的表达;部分肿瘤组织制备成冰冻切片,利用FITC和TRITC双标记免疫荧光染色,使用激光共聚焦显微镜观察X与Y的共定位情况。
2.3. X-Y轴调节结肠癌肝转移的分子机制研究
1) 通过基因芯片Microarray分析X过表达/沉默后基因表达谱变化情况,对原始数据进行归一化、标准化,差异表达分析,明确X消减后表达发生改变的下游调控分子,芯片结果中有显著差异的潜在作用分子,设计引物,通过qRT-PCR进行二次表达验证。
2) X基因过表达/沉默后发生显著表达差异的基因,利用Bayesian Network、Genes2Networks、Go-anaslysis软件进行signaling network 重建。解析X调控结肠癌细胞运动能力的信号通路网络,构建X为核心的信号分子网络。
3) 根据X基因沉默后影响的信号通路结果(半乳糖基转移酶及其上游调节信号通路),利用信号通路抑制剂处理X稳定过表达/沉默后结肠癌细胞和对照细胞,检测不同分子信号对X表达及功能的作用,验证阻断这些信号通路后对X在结肠癌中的功能表型的影响。
4) 采用信号通路高通量检测蛋白芯片,根据以上实验分析的通路情况,订购相应通路的Pathway Array试剂盒,按试剂盒操作,依据封闭、加入细胞裂解液、洗脱、加入抗体混合液、再次洗脱,加入辣根过氧化物酶HRP并洗脱、信号检测的步骤,检测X基因表达变化后的特定通路关键蛋白的变化。
5) 分别构建X、Y的真核表达载体,共转293T,通过免疫共沉淀(Co-IP)验证XY的相互结合作用。
6) 应用生物信息学技术模拟X与Y的结合位点。在结合位点制备不同氨基酸的突变体。采用RNAi方法敲减互作蛋白表达,接着转入互作蛋白的突变体,检测细胞功能表型变化。通过免疫共沉淀(Co-IP)验证X与Y之间的结合位点特异性。
7) EMSA实验验证X与Y之间的相互作用关系,参考蛋白相互作用实验,设计突变载体,再验证其结合特异性,由此揭示X作为Y调节蛋白其对下游RNA进行调控的精细机制。
3. 可行性分析
1) 研究目标切实可行:我们前期的工作已明确证实:Y可以调节结肠癌的恶性增殖,并且进行了大量的预实验,可支持本课题主要科学假设。本项目是对前期研究工作的进一步补充和完善,具有较好的可行性。
2) 技术平台与硬件设施完善:课题组成员长期从事结直肠癌的诊治和发生发展机制研究,在免疫组化、免疫印迹、实时荧光定量PCR、RNA 干扰、慢病毒包装、表达谱芯片研究等各个方面积累了大量的经验,本项目中所用到的实验技术以前均有所涉及,为本项目的实施提供了技术保障。本项目所需的主要仪器设备目前均已经具备。
3) 研究基础扎实:本课题组成员长期从事结直肠癌的基础和临床研究,具有良好的科研素质。在国内外杂志上发表了多篇结直肠癌基础研究和临床研究相关的论文。
4) 临床标本充足:仁济医院普外科长期从事结直肠癌的诊治,已经建立一套规范化的结直肠癌诊疗体系,拥有大量结直肠癌手术标本(每年1000余例),能够保证课题所需大量的结直肠癌标本的要求。
5) 团队年轻优秀、成员配备合理:课题组成员大部分为中青年业务骨干,热爱科学研究,有较强的创新能力,能为实验投入大量的时间,每个人均有自己的研究专长,能保障本实验的顺利完成。
4. 本项目的特色与创新之处
1) 思路上创新:X和Y是Z家族中具有相互作用的一对分子,他们在结肠癌肝转移的过程中发挥差异性的功能。针对X-Y轴进行组合策略研究,能够解决更多维度的科学问题,对临床具有指导意义;
2) 内容上创新:X-Y轴在结肠癌癌中的功能作用和与癌变的关系还是未知领域,我们首先鉴定了Y,随后对Y和X的交互作用进行研究,能够进一步形成创新的研究成果。
5. 研究工作的进度安排
本项目预计在4年内完成,具体进展计划如下:
u 2015.01-2015.12:定量PCR检测结肠癌及结肠癌肝转移新鲜组织标本中X和Y表达,分析临床病理及预后的相关性;X和Y基因过表达和shRNA慢病毒构建、包装和纯化,细胞功能检测;
u 2016.01-2016.12:免疫组化检测结肠癌及结肠癌肝转移标本中Y和X表达,分析临床病理及预后的相关性;X和Y影响结肠癌肝脏转移和恶性增殖的动物实验。
u 2017.01-2017.12:Pathway array分析X和Y调控结直肠癌细胞转移的信号通路网络;生物信息学分析与分子验证,通路抑制剂验证。
u 2018.01-2018.12:Co-IP实验验证X与Y之间的相互作用关系。蛋白结合位点突变载体制备及其结合特异性验证。
6. 预期研究结果
1)阐明X和Y表达在肠癌中的临床意义;
2)解析X-Y调节轴在结肠癌肝转移中的功能及相互作用机制;
3)在国际学术刊物上发表SCI收录学术论文3篇,至少1篇IF>5;
4)申请专利1项;
5)培养博士研究生1名,硕士研究生2名。
三、工作基础
因涉敏感基因信息,略
-
成功申请国家自然科学基金申请书范例
国家自然科学基金申请书申报日期:20xx年月日国家自然科学基金委员会国家自然科学基金申请书项目组主要成员(注:项目组成员不包括项目…
-
国家自然科学基金(NSFC)申请书样本
申请代码受理部门收件日期受理编号E050802解除保护国家自然科学基金申请书20xx版资助类别面上项目亚类说明附注说明项目名称金属…
-
国家自然科学基金标书写作全攻略+成功范例1份
国家自然科学基金标书写作全攻略成功范例1份指导思想篇1追求卓越在知识上要绝对专业坚决反对侥幸心理2相信NSFC申请是公平的大家靠实…
-
20xx年度国家自然科学基金申请书撰写格式参考
国家自然科学基金申请书国家自然科学基金申请书撰写指南申报日期20xx年月日20xx版国家自然科学基金委员会国家自然科学基金申请书纸…
-
国家自然科学基金申请书范例
国家自然科学基金申请书现代机电控制工程姓名学号学院班级20xx国家自然科学基金申请书空国家自然科学基金申请书申报日期20xx年月日…
-
医学生20xx年寒假见习报告书范文
精品医学生20xx年寒假见习报告书范文见习时间20xx020720xx0220见习地点省市第二医院见习人作为医学生的第一个寒假学校…
-
医学标书范文3
河南省科技攻关计划项目申请书姓名:xx项目名称:FGFR4表达对结直肠癌细胞株生物学行为的影响及作用机制的研究单位:郑州大学联系电…
-
大学生职业生涯规划书范文(临床医学)
要做好职业生涯规划就必须按照职业生涯设计的流程认真做好每个环节职业生涯设计的具体步骤概括起来主要有以下几个方面前言正确说明社会发展…
-
大学生职业生涯规划书范文(临床医学)
要做好职业生涯规划就必须按照职业生涯设计的流程认真做好每个环节职业生涯设计的具体步骤概括起来主要有以下几个方面前言正确说明社会发展…
-
大学生职业生涯规划书范文(临床医学)
大学生职业生涯规划书范文临床医学txt如果我穷得还剩下一碗饭我也会让你先吃饱全天下最好的东西都应该归我所有包括你先说喜欢我能死啊别…
-
国家社科基金成功中标申请书范本
国家社会科学基金项目申请书项目类别一般项目学科分类应用经济课题名称房地产税收制度研究基于市场价值体系下个人住房税收制度的安排项目负…