20xx届高三化学二轮复习计划9
20##—20##学高三化学二轮复习计划及进度
高三化学备课组
经过一轮的复习,学生已将零碎的化学知识进行归类、整理、加工,使之规律化、网络化,对知识点、考点、热点进行了初步的思考、总结、处理,在一轮的训练中已体会到近来几年高考常考点、易错点。二轮复习更加艰巨,因为二轮复习资料更重要的是提高学生的实际应用的本领,分析问题和解决问题的能力,同时将学生获得的知识转化成能力,提升学生的解题能力和规范答题,从而使学生该得的分不丢,能得的分尽可能多得,难得的分想办法多得点。
为了使第二轮复习能扎实有效地顺利进行,确保今年高考取得优异成绩,结合学校的要求,总结专家的经验,通过高三备课组认真学习,深入思考,特制订如下的复习计划:
一、吃透教材,落实考纲
首先集中组织全组的老师钻研《考试大纲》,按《考试大纲》的要求复习备考。做到每位教师都能把握要求,明确方向。
其次,把《考试大纲》与高考试题、教材、平时的练习相结合。
再次,从平时的练习中发现我们的学生离近几年高考的差距,把握命题的难度和区分度,命出好题,精讲练后结果,提高练习的价值。
二、确立好专题 负责人
第一专题 实验设计与评价题型应对策略
第二专题 物质组成及化学计量
第三专题 氧化还原反应 离子反应
第四专题 物质结构 元素周期表周期律
第五专题 化学反应及能量变化
第六专题 化学反应速率 化学平衡
第七专题 水溶液中的离子平衡
第八专题 电化学
第九专题 无机推断题型应对策略
第十专题 有机推断、有机合成题型应对策略
第十一专题 高考规范答题例析
三、强调好老师在二轮中的作用
1、老师重点在备课,做到一课一备,每周二次备课组活动,备理论知识,更备学生信息。
2、命好题。所谓的好题就是紧扣高考考纲,根据老师对近几高考题研究的体会,结合我们的学生特征,命出步步提升学生对知识的处理能力的题目。
3、学生所做的题目,老师必须从批阅中发现自己学生的问题,精心讲评。AB层每套题目老师讲评最好不超过四道,舍得花时间让学生自主消化,小组合作提升,教师负责释疑。
4、强调答题的技巧和答题的规范。从多次统一阅卷的错误统计中,发现学生的弱点、失分点,在讲评练习和大考之前再三强调规范,通过反复提示,让学生养成良好的答题方法和习惯。
四、实施措施
为更好地完成任务,主要有以下措施
1.组织教师加强对教纲、考纲及考试说明的学习,把考点分解到每节课,复习中重视知识的横向与纵向深入,把握高考复习的正确方向。
2.在备课组中加强全体教师对关键问题、内容的沟通与研究,引导全体同学探究化学复习方法,狠抓听课效率和训练质量两个关键点。
3.组织教师精心研究近几年的高考试题,每位教师在备课组活动对自己研究的相关部分内容主发言,提出问题一起解决,并就相应部分模拟高考命出多道题,供其他老师审阅后定稿。
4.对例题、练习、试题,加强针对性的筛选,特别关注重点知识、热点知识的落实情况。
5.认真分析测试结果,及时调整复习计划、训练内容和辅导的方式。
6.重视对学生的学法指导和情感交流,帮助学生树立信心克服困难。
7.每周的备课组活动时间及周练时间为集体备课时间,讨论下周应讲授知识的重点与难点、研究学情与教法。
五、临界生的培养
1、重视第次的考试,做到对临界生面批。
2、对易失分的知识点和题型,反复练,可以另外“加餐”。
3、不定期抽查临界生的学习计划本。
4、每周一次让临界生听写化学方程式。
5、从生活到学习,全方位关注临界的发展。
七、二轮进度及备课安排

第二篇:20xx届高三化学二轮复习练习三十(循环练习9)(第四稿)定稿
2014届高三化学二轮复习练习三十(循环练习9) 命题人:田益民 审核人:李 洁
班级姓名
1.常温下,下列各组离子在指定溶液中一定能大量共存的是 ( )
A.0.1 mol·L
B.0.1 mol·L
C.0.1 mol·L-1的NaI溶液:K、H、SO24、NO3 ++---1-1
-1的NaHCO3溶液:K、Na、NO3、Cl FeCl3溶液:K、Na、CO32、Cl ++--++--D.0.1 mol·L 的氨水:Cu2+、Na+、SO24、NO3--
2.设NA表示阿伏加德罗常数的值。下列说法正确的是 ( )
A.1.5 g CH3含有的电子数为NA B.电解精炼铜转移NA个电子时,阴极析出32 g铜
C.1 L 0.1 mol·L1 氨水溶液中所含的离子和分子总数为0.1NA -+
D.标准状况下,22.4 L CHCl3含有C—Cl 键的数目为3NA
3.对下列物质用途的解释不正确的是 ( )
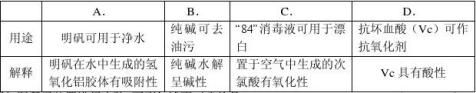
...
4...
A.K与N连接时,铁被腐蚀
B.K与N连接时,石墨电极产生气泡
C.K与M连接时,一段时间后溶液的pH增大
D.K与M连接时,石墨电极反应:4OH——4e—=2H2O+O2↑
5.W、X、Y、Z是4种短周期元素,其原子序数依次增大,其中
W、X是形成化合物种类最多的两种元素,Y、Z同主族,Z的核
电荷数是Y的2倍。下列说法错误的是 ( )
A.最高价氧化物对应水化物的酸性:X>Z
B.W、X、Z都能与Y形成两种共价化合物
C.X、Y、Z分别与W形成的所有化合物中,Y与W形成的化合物沸点最高
D.X、Y、Z均能分别与W形成18电子化合物
6.下列说法中用离子方程式表达正确的是 ( )
A.盛放石灰水的试剂瓶出现白色固体:Ca(OH)2+CO2===CaCO3↓+H2O
B.向NaAlO2溶液中通入过量CO2:2AlO2+CO2+3H2O=2Al(OH)3 ↓+CO23 --C.Fe(NO3)2 溶液中滴加少量稀盐酸:Fe2++NO3+4H+===Fe3++NO↑+2H2O -
D.

Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2+HCO3+OH===CaCO3↓+H2O +--
1
7.下列装置能达到实验目的的是 ( )
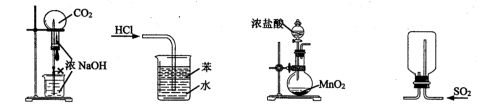
图1 图2 图3 图4
A.利用图1装置进行喷泉实验 B.利用图2装置吸收HCl气体
C.利用图3装置制备Cl2 D.利用图4装置收集SO2
8.下列物质的转化在给定条件下能实现的是 (
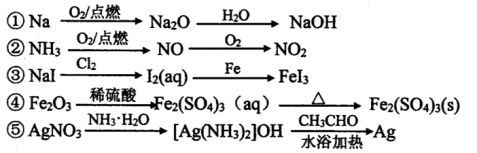
)
A.①③ B.②⑤ C.②④ D.④⑤
9.香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下图所示。下列说法
错误的是 ( )
A.理论上反应1→2中原子利用率为100%
B.化合物2在一定条件下可发生缩聚反应
C.检验制得的香草醛中是否混有化合物3,可用氯化铁溶液
D.等物质的量四种化合物分别与足量NaOH反应,消耗NaOH物质的量之比为1:2:2:1
10.下列有关实验原理、操作方法和说法都正确的是 ( )
A.某溶液中加入BaCl2溶液,有白色沉淀,再加入稀盐酸沉淀不溶,说明该溶液中一
-定含SO24
B.将含有SO2杂质的CO2气体,缓慢通过足量的高锰酸钾溶液,再通过浓硫酸干燥,可获得较纯净的CO2气体
C.将某试样 (含NaHCO3、Na2CO3中的一种或两种)进行灼烧,冷却,并用托盘天平称量残留固体的质量,根据质量是否变化,可确定样品的组成
D.某蛋白质溶液中加入饱和硫酸铵溶液,将得到的沉淀分离出来溶于水,多次重复上述操作,可提纯蛋白质
2
11.下列图示与对应的叙述相符的是 ( )
图1 图2 图3 图4
A.图1曲线a和b是盐酸与氢氧化钠溶液的相互滴定的滴定曲线,P点时二者恰好反应完全且溶液呈中性
B.图2表示H2(g)与O2(g)反应生成H2O(l)或H2O(g)时的能量变化的关系 C.图3表示向Ba(HCO3)2溶液中滴入NaOH溶液时所得沉淀质量的变化 D.由图4表示的反应速率随温度变化的关系可知该反应的ΔH>0
12.下列有关溶液中微粒浓度关系的叙述错误的是 ( )
-
A.25℃时,pH=8的CH3COONa稀溶液中,c(CH3COOH)=9.9×107mol/L B.溶有等物质的量NaClO、NaHCO3的溶液中:
---
c(HClO)+c(ClO)=c(HCO3)+c(H2CO3)+c(CO32) C.向CH3COONa溶液中滴加稀HCl至中性,所得溶液中:
-+
c(Cl)>c(Na)>c(CH3COOH)
D.等物质的量浓度的Na2CO3溶液和NaHCO3溶液等体积混合,所得溶液中: c(CO32)+2c(OH)=2c(H)+c(HCO3)+3c(H2CO3)
-
-
+
-
13.工业上利用含镍废料(镍、铁、钙、镁合金为主)制取Ni2O3的工艺流程如下:

镍废料
3
已知:①草酸的钙、镁、镍盐均难溶于水。
②有关氢氧化物开始沉淀和沉淀完全的pH如下表:
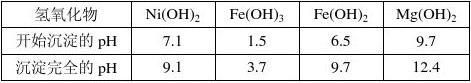
请问答下列问题:
(1)加入H2O2的目的是将溶液中Fe2氧化,写出该反应的离子方程式 。
+
(2)步骤A应调节溶液pH的范围是 。步骤B中加入NH4F的目的是 (3)如果在酸溶过程中HNO3完全反应,则从溶液A中可以回收的物质是 。 (4)干燥脱水后得到NiC2O4,将其煅烧3h,制得Ni2O3,同时生成CO和CO2。写出NiC2O4受热分解的化学方程式 。煅烧时温度过高会导致固体中镍元素的质量分数明显增大,解释可能的原因是 。
3
-
高三二轮复习计划的运作说明
高三二轮复习计划的运作说明高三物理第二轮复习计划目前,物理总复习普遍进入二轮,即专题复习阶段,时间一般延伸到四月底。这是一个承上启…
-
20xx届高三二轮复习计划
红安一中20xx届高三二轮复习计划高三一轮复习即将结束二轮复习迫在眉睫复习备考工作即将进入攻坚阶段为了使我们的复习备考行之有序为了…
-
高三二轮复习计划与策略
高三二轮复习计划与策略我们都有清晰的认识对于一个学校来说得数学者得天下对理科生来说得数学者得高分得名牌大学的通知书因此二轮复习对于…
-
20xx届高三物理第二轮复习计划
岑巩县中学20xx届高三物理第二轮复习计划高三物理备课组高三物理通过第一轮的复习学生大都能掌握物理学中的基本概念规律及其一般应用但…
-
20xx届高三语文第二轮复习计划
20xx届高三语文第二轮复习计划高三语文备课组一、指导思想注重策略,狠抓落实,重点突出,全面提高。二、具体要求巩固语基,加强阅读,…
-
高三化学二轮复习计划
高三化学二轮复习计划高三化学的第一轮复习按照原计划,将要在三月底结束,从四月开始的第二轮复习是高考复习备考非常重要的时期,也是巩固…
-
20xx年高三化学备考总复习计划
20xx年高三化学备考总复习计划高三化学备课组徐老师通过对几年高中化学教学和近几年全国各地高考化学试题的研究在认真分析考试大纲基础…
-
高三化学第二轮复习计划
高三化学第二轮复习计划来源高分网为了使第二轮复习能扎实有效地顺利进行确保今年高考取得优异成绩经过高三备课组认真学习深入思考特制订如…
-
20xx年中考化学复习计划
20xx年中考化学复习计划20xx年中考即将来临为了更好的迎接中考让同学们尽可能的考出一个理想的成绩因此我们必须做好中考前的复习工…
-
20xx年九年级化学总复习计划
九年级化学复习计划张丽根据20xx年中考化学考试特点结合我校教学实际情况为了把握好中考方向提高教学效率我们制定如下化学复习计划一指…
-
安徽省中考化学复习计划
20xx年中考化学复习计划张磊20xx年中考即将来临,为了迎接中考,让同学们尽可能的考出一个理想的成绩,我们必须做好中考前的复习工…