粗盐的提纯实验教学设计
粗盐的提纯
教学目标
一、知识和技能
1、学习蒸发的操作;
2、练习溶解、过滤等操作。
二、过程与方法
通过粗盐提纯的实验操作了解提取氯化钠的方法;
三、情感、态度价值观
通过实验进一步加深化学与生活的联系。
教学重点
粗盐提纯的步骤,溶解、过滤、蒸发等操作中玻璃棒的作用
教学难点
过滤的操作和蒸发操作的技巧
教学方法
贯彻“教为主导、学为主体、注重过程“的原则,采用问题探究和实验探究为教学情境,配以讨论、实验等方法的综合运用,激发学生的学习兴趣,从而培养学生分析、解释问题的能力,以达到化学与实践的有机结合和学以致用的目的。
课时安排
1课时
教学过程
一、导入新课
1、混合物的分离和提纯:教师演示铁屑和沙子的分离实验。
2、有 “粗食盐和食盐”、“粗盐溶液和食盐溶液” 各一瓶(展示)请你分析:
(1)各组的外观有何差异?
(2)你了解的粗盐中有哪些杂质?如何将粗盐转化为精盐?怎样除去粗盐中的不溶性杂质?(引入本节的探究任务:活动与探究——粗盐的初步提纯)
3、粗盐提纯的基本步骤有哪些?
二、分组实验探究
1、分组实验
各组分工合作,分步操作;(教师巡回指导,发现问题,适时强调;发现典型,及时评价。)
2、粗盐提纯的每个步骤中,应注意哪些问题?
(1)简要说明过滤操作的注意事项。
(2)教师强调蒸发时的操作注意问题。
3、交流试验结果
(1)各小组代表汇报实验结果,交流实验的得与失。
(2)教师点评。(告诉粗盐产率的理论值)
4、学生评议,提出质疑
(1)我们小组所得食盐产率大于理论值,为什么?
(2)我们小组所得食盐产率小于理论值,为什么?
5、组内讨论
(1)造成实验误差的原因可能有哪些?
四、总结交流
1、这节课你学到了什么?提高了哪些方面的能力?(自我评价)
2、对粗盐提纯的基本步骤及注意事项进行归纳总结。(学生示范)
3、玻璃棒在实验中有哪些作用?
五、作业布置
1.收交实验报告。
2、课后延伸
如何除去粗盐中含有的氯化钙、氯化镁、碳酸钠等可溶性杂质?原理是什么?怎样操作?
第二篇:粗盐的提纯实验教学设计
粗盐的提纯探究实验学案设计
【实验目的】
1. 知识与技能目标
(1)通过粗盐提纯实验,进一步掌握溶解、过滤、蒸发等基本操作。
(2)通过实验中杂质离子的检验与除杂质方法的讨论,加深对物质分离及提纯操作原理和方法的理解。
(3)初步认识实验方案设计、实验条件控制、实验现象分析等方法在化学学习和科学研究中的应用。能够记录实验现象,对现象进行分析得出结论,完成实验报告。
2. 过程与方法目标
(1)通过思考与交流、实验设计、实验探究,学会如何设计实验,学会在设计实验时如何把握实验的难点、注意点和可能产生的问题。
(2)体验科学探究的过程,学习运用以实验为基础的实证研究方法。
3. 情感态度与价值观目标
(1)通过探究实验、亲自实验,让学生感受化学学习的趣味,感受化学学习的快乐,从而乐意学习化学。
(2)鼓励引导学生将化学知识带进生活、生产,感受化学学习的意义,把化学与生活联系起来,从生活中获取化学知识,用化学知识服务于生活。
【提示与准备】
1、除去粗盐固体中的不溶性杂质,必须要进行的实验操作依次是:
① ② ③
2、过滤器的制作方法是将一张滤纸对折两次,打开成圆锥形,把其尖端朝下放入漏斗。过滤操作时应做到“一贴二低三靠”,
①一贴:即滤纸应紧贴 ;
②二低:滤纸边缘应低于 ,滤液液面应低于 ;
③三靠:滤液应靠 引流,玻璃棒应靠在 层滤纸的一边,漏斗下端的管口应紧靠 。
【实验用品】
药品:粗盐,水,氢氧化钠溶液,碳酸钠溶液,稀盐酸
仪器:量筒,烧杯,玻璃棒,药匙,漏斗,铁架台(带铁圈),蒸发皿,酒精灯,坩埚钳,胶头滴管,滤纸,剪刀,火柴
【实验内容】
粗盐中常含有泥沙等不溶性杂质以及一些可溶性杂质,现有一份粗盐样品中含有少量MgCl2 、CaCl2以及一些不溶性杂质,请设计实验方案并小组合作完成粗盐的提纯
【方案设计】
讨论交流如何除掉MgCl2 、CaCl2呢?设计写出方案(注意不要带入杂质离子)
 【实验步骤】
【实验步骤】
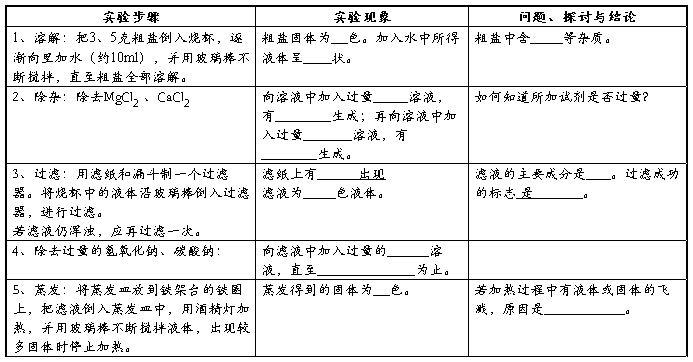
1、 溶解:
把3、5克粗盐倒入烧杯,逐渐向里加水(约10ml),
并用玻璃棒不断搅拌,直至粗盐全部溶解。
讨论:为什么溶解这部分粗盐要选择约10 ml水呢?
2、 除杂:
除去MgCl2 、CaCl2
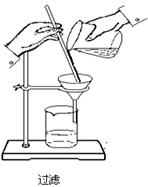
3、 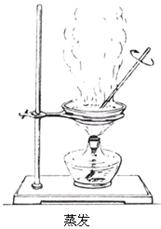 过滤:
过滤:
用滤纸和漏斗制一个过滤器。将烧杯中的液体
沿玻璃棒倒入过滤器,进行过滤。
若滤液仍浑浊,应再过滤一次。
4、除去过量的氢氧化钠、碳酸钠:
5、蒸发:
将蒸发皿放到铁架台的铁圈上,把滤液倒入蒸发皿中,
用酒精灯加热,并用玻璃棒不断搅拌液体,
出现较多固体时停止加热。
【提升练习】
一、本实验中玻璃棒的作用:
1、溶解
.
2、过滤
3、蒸发
二、一份粗盐溶液中含有钙离子、镁离子、硫酸根离子
等可溶性杂质,要想除掉杂质离子获得精盐,通过本节实验回答下列问题。
(1)为了保证除去SO42-离子,所用的除杂药品是 用量上怎么要求?
(2)在上述溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问该操作的目的是为了除去 离子。
(3)理论上经过提纯得到的氯化钠比样品中含有的氯化钠 。(填多还是少了或者不变)。
粗盐的提纯实验报告
实验目的
1)通过粗盐提纯实验,进一步掌握溶解、过滤、蒸发等基本操作。
2)通过实验中杂质离子的检验与除杂质方法的讨论,加深对物质分离及提纯操作原理和方法的理解。
3)体验科学探究的过程,学习运用以实验为基础的实证研究方法。
实验用品
药品:粗盐,水,氢氧化钠溶液,碳酸钠溶液,稀盐酸
仪器:量筒,烧杯,玻璃棒,药匙,漏斗,铁架台(带铁圈),蒸发皿,酒精灯,坩埚钳,
胶头滴管,滤纸,剪刀,火柴
注意事项: 蒸发实验中什么时候停止撤去酒精灯?
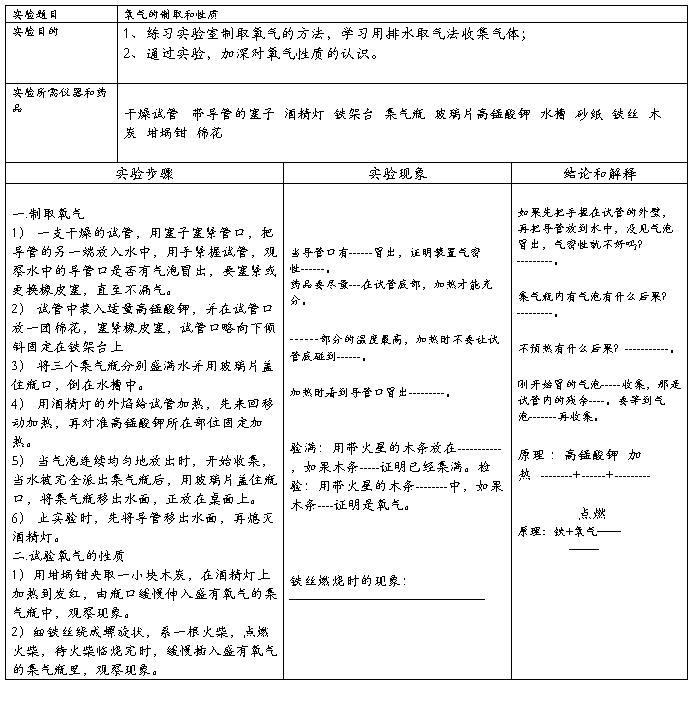
氧气的制取和性质实验报告
学校 班级 姓名
-
粗盐的提纯实验报告
粗盐提纯实验报告一、实验目的:1.掌握溶解、过滤、蒸发等实验的操作技能.2.理解过滤法分离混合物的化学原理.3.体会过滤的原理在生…
-
粗盐提纯实验报告
一实验目的1掌握溶解过滤蒸发等实验的操作技能2理解过滤法分离混合物的化学原理二实验原理粗盐中含有泥沙等不溶性杂质不溶性杂质可以用溶…
-
粗盐提纯实验报告
粗盐提纯实验报告实验时间一实验目的实验人去除粗盐中一些不容于水的一些颗粒蒸发后的到比较纯净的盐类物质二实验原理粗盐中含有泥沙等不溶…
-
粗盐提纯实验报告
一实验目的1掌握溶解过滤蒸发等实验的操作技能2理解过滤法分离混合物的化学原理3体会过滤的原理在生活生产等社会实际中的应用二实验原理…
-
粗盐提纯实验报告
化学实验报告姓名班级日期实验名称粗盐中难溶性杂质的去除实验目的1学会除去粗盐中的少量难溶性杂质的方法2初步学会使用过滤蒸发的方法对…
-
粗盐的提纯实验报告
粗盐提纯实验报告一、实验目的:1.掌握溶解、过滤、蒸发等实验的操作技能.2.理解过滤法分离混合物的化学原理.3.体会过滤的原理在生…
-
粗盐提纯实验报告
一实验目的1掌握溶解过滤蒸发等实验的操作技能2理解过滤法分离混合物的化学原理二实验原理粗盐中含有泥沙等不溶性杂质不溶性杂质可以用溶…
-
粗盐提纯实验报告单
化学实验报告班级姓名桌号日期年月日实验名称粗盐中难溶性杂质的去除一实验目的1体验固体混合物初步提纯的实验过程2学习蒸发操作技能巩固…
-
实验1 粗盐提纯实验报告
实验1粗盐提纯实验目的1了解如何除去粗盐中的不溶性杂质和可溶性杂质硫酸盐镁离子钙离子2通过实验进一步巩固溶解过滤蒸发等基本操作实验…
-
粗盐提纯实验报告
初中化学实验粗盐提纯练习过滤和蒸发操作班级姓名组员日期一实验目的1掌握溶解过滤蒸发等实验的操作技能2理解过滤法分离混合物的化学原理…
-
粗盐提纯实验报告
化学实验报告姓名班级日期实验名称粗盐中难溶性杂质的去除实验目的1学会除去粗盐中的少量难溶性杂质的方法2初步学会使用过滤蒸发的方法对…