岛津DTG-60H热分析实验报告--TG,DTA曲线联用分析
岛津DTG-60H热分析实验
一. 实验原理
热分析(thermal analysis)是在程序控制温度下,测量物质的物理性质与温度关系的一类技术,在加热和冷却的过程中,随着物质的结构、相态和化学性质的变化,通常伴有相应的物理性质的变化,包括质量、温度、热量以及机械、声学、电学、光学、磁学等性质,依此构成了相应的各种热分析测试技术。表1列出了几种主要的热分析法及其测定的物理化学参数和有关仪器。其中最具代表性的三种方法:热重法(TG),差热分析(DTA),差示扫描量热法(DSC)。
表1 热分析中的主要测定方法

本实验使用的岛津DTG-60H是一类差热(DTA)—热重(TG)同步测定装置。
热重法(Thermalgravimetry, TG)是在程序控制温度下,测量物质的质量和温度关系的一种技术。热重法记录的是热重曲线(TG曲线),它是以质量作纵坐标,从上向下表示质量减少;以温度(T)或时间(t)作横坐标,自左向右表示增加。用于热重法的仪器是热天平,它连续记录质量和温度的函数关系。热天平一般是根据天平梁的倾斜与质量变化的关系进行测定的,通常测定质量变化的方法有变位法和零位法两种。变位法利用质量变化与天平梁的倾斜成正比关系,用直接差动变压器检测。零位法根据质量变化引起天平梁的倾斜,靠电磁作用力使天平梁恢复到原来的平衡位置,所施加的力与质量变化成正比。DTG-60H采用的为变位法。只要物质受热时发生质量的变化,就可用热重法来研究其变化过程。其应用可大致归纳成如下几个方面:(1)了解试样的热(分解)反应过程,例如测定结晶水、脱水量及热分解反应的具体过程等;(2)研究在生成挥发性物质的同时所进行热分解反应,固相反应等;(3)用于研究固体和气体之间的反应;(4)测定熔点、沸点;(5)利用热分解或蒸发、升华等,分析固体混合物。图1为在相同实验条件下测得的聚氯乙烯(PVC),聚甲基丙烯酸甲酯(PMMA),高压聚乙烯(HPPE),聚四氟乙烯(PTPE)和芳香聚四酰亚胺(PI)的热重曲线。它们不仅提供了高聚物分解温度的信息,也很简便地比较了高聚物的热稳定性。

差热分析(Differential thermal analysis, DTA)是在程序控制温度下,测量试样与参比物(一种在测量温度范围内不发生任何热效应的物质)之间的温度差与温度关系的一种技术。在实验过程中,可将试样与参比物的温差作为温度或时间的函数连续记录下来:
⊿T = ? (T或t)
由于试样和参比物的测温热电偶是反向串联(见图2),所以当试样不发生反应,即试样温度(Ts)和参比温度(Tr)相同时,⊿T = Ts — Tr = 0,相应的温差电势为0。当试样发生物理或化学变化而伴有热的吸收或释放时,则⊿T≠ 0,相应的温差热电势讯号经放大后送入记录仪,得到以⊿T为纵坐标,温度为横坐标的差热曲线(DTA曲线),如图3所示其中

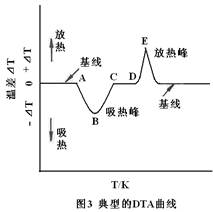
基线相当于⊿T = 0,试样无热效应产生;向上和向下的峰反映了试样的放热、吸热过程。图4为吸热反应中试样的真实温度和试样与参比物温差⊿T的比较,从试样温度曲线可见,

吸热过程开始于A点。此时由于试样吸收热量,体系温度偏离直线而落后于炉温。达到B点时,反应基本完成。随后体系温度逐渐上升,至C点再回到炉温。至于温差曲线,显然更为清晰明显。由图可见,⊿T开始于A点,其最大值(峰点)则在B点,至C点又回到基线。 采用⊿T作检测量,比单纯用实验温度更为理想,因为这样能更好地确定峰点位置。如果是放热反应,将得到类似的差热峰形,只是差热峰处于与吸热峰相反的方向。
将不同体系的吸热和放热的原因归纳于表2,供判断差热峰的产生机理时参考。
表2 差热分析中的放热峰和吸热峰产生的原因

图5为高聚物的DTA模式曲线,它反映了高聚物随温度升高所产生的玻璃化转变、结晶、熔融、氧化和分解等过程。DTA曲线的峰形,出锋位置,峰面积等受试样的质量,热传导率,比热,粒度,填充的程度,周围气氛和升温速度等因素的影响。以升温速度为例,升温速度太慢,转变不明显,甚至观察不到;升温速度快,转变明显,但达到峰值的温度向高温方向偏移,峰形尖锐,但峰的分辨率降低,一般采用10℃/分比较合适。一般情况下,在实验时采用薄膜或细粉状样品,并使试样铺满盛器底部,加盖压紧,试样底部尽可能平整;保证和托架之间的良好接触。气氛应该是静态的,也可以是动态的,就气体性质而言,可以是惰性的,也可以是参加反应的,视实验要求而定。一般采用N2,流量在30毫升/分左右。

差热分析主要应用于以下方面:研究结晶转变,二级转变;追踪熔融,蒸发等相变过程;用于分解、氧化还原、固相反应等的研究。
在热分析中,参比物应选择那些在实验温度范围内不发生热效应的物质,如α-氧化铝、石英、硅油、瓷、玻璃珠等。
二、实验仪器
岛津DTG-60H,是一类差热(DTA)—热重(TG)同步测定装置,如图6所示。图7为操作键和显示屏的图示。图8为参比物和试样架示意图。图9为DTG-60H的热失重部分结构图。本实验中采用的参比物为α-氧化铝,试样进样重量视试样性质而定,有机物进样量约为参比物的两倍质量,无机物进样与参比物质量相等即可。




三、实验步骤
1、开启电脑和DTG-60H,并预热10分钟。
2、称取聚丙烯(PP)材料5mg,放入铝坩埚中,将铝坩埚放入DTG-60H样品架上(右侧)。
3、通入保护气(N2),流量为40ml/min(指示球位于中间位置)。设定测试程序,升温速度为10℃/min,最高温设置为200℃;降温速度设置为10℃/min。将重量输入重量栏,或者直接仪器读取(在zero的前提下)。为数据设置到目标文件夹内。
4、启动DTG-60H测试程序,对PP样品进行DTA和TG测试。
5、根据数据处理方法介绍处理数据,分析样品的Tg,Tm以及Td等。
四、结果与分析
1.图1是聚丙烯的热分析数据处理结果,相关信息标于图中,可以看出,在温度从20℃升高到300℃的过程中,TG曲线是一条几乎水平的直线,说明未发生失重;DTA在170.5℃出现吸热峰,是由于熔化吸收热量所致,说明PP的熔点是170.5℃,与标准数据作比较,判断此PP应是全同立构聚合物。

图1 聚丙烯的DTG曲线
2. 图2是丁二酸的热分析图谱,相关信息标于图中。由热失重曲线可知,温度升高到186℃,发生失重,说明有分解反应发生,此过程是丁二酸熔化,并逐渐脱去小分子水,生成酸酐。再由DTA曲线,知丁二酸的熔点是191℃,沸点是235℃。

图2 丁二酸的DTG曲线
3. 图3是三苯基磷的热分析图谱,综合TG和DTA曲线知,83℃是其熔点,固态三苯基磷熔融吸热;179.7℃以后,发生了热分解反应,导致失重和吸热峰的产生。
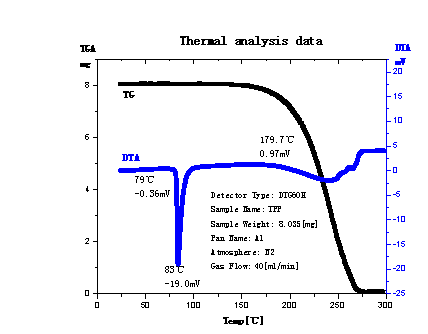
图3 三苯基磷的DTG曲线
第二篇:DSC TG综合热分析实验
华南师范大学实验报告
专 业: 材料化学 年 级:2008级
课程名字: 近代材料分析测试技术 实验项目:综合热分析实验 实验类型: 验证 实验时间:20xx年5月6日
指导老师: 石光老师 实验评分:
实验六:综合热分析实验
一、 实验目的
1.了解综合热分析仪的原理及仪器装置、操作方法。
2.通过实验掌握热重分析的实验技术。
3.使用综合分析仪分析高聚物的热效应和热稳定性。
二、 实验原理
在程序温度(等速升降温、恒温和循环)控制下,测量物质的质量和热量随温度变化的分析仪器。刚开始加热时,试样和参比物以相同温度升温,试样没有热效应,DSC曲线上为平直的基线。当温度上升到试样产玻璃化转时,大分子的链段开始运动。试样的热容发生明显的变化,由于热容增大需要吸收更多的热量,于是DSC曲线上方出现一个转折,该转折对应的温度,即玻璃化转变温度(Tg)。若试样是能结晶的并处于过冷的无定形状态,则在玻璃温度以上的适当温度进行结晶,同时放出大量的热量,此时DSC曲线上表现为放热峰。再进一步加热,晶体开始熔融而需要吸收热量,其DSC曲线在相反方向出现吸热峰。当熔融完成后,加于试样的热能再使试样温度升高,直到等于参比物的温度,回复到基线位置,将熔融峰顶点对应的温度记作熔点(Tm);继续加热试样可能发生其他变化,如氧化、分解(氧化是放热反应,分解是吸热反应)。因此,根据DSC曲线可以确定高聚物的转变和特征温度。
三. 仪器和试剂
交联壳聚糖微球、吸附了重金属的交联壳聚糖微球,聚丙烯,高密度聚乙烯, a-Al2O3、STA409PC综合热分析仪。
四、实验步骤
(一)操作条件
1、实验室门应轻开轻关,尽量避免或减少人员走动。
2、计算机在仪器测试时,不能上网或运行系统资源占用较大的程序。
3、充入保护气体。
4、吹扫气体。
5、恒温水浴保证测量天平工作在一个恒定的温度下。
(二)试样准备
1、检查并保证测试试样及其分解物。
2、坩埚(包括参比坩埚)预先进行热处理到等于或高于其最高测量温度。
3、保证与测量坩埚底部接触良好,样品应适量,确保测量精度。
4、对于热反应剧烈或在反应过程中易产生气泡的样品,应适当减少样品量。
5、炉子内部温度必须保持恒定(室温),天平稳定后的读数才有效。
6、测试必须保证样品温度(达到室温)及天平均稳定后才能开始。
7、先将试样制成细粉状并通过80~100目的筛孔,称取聚丙烯和低压聚乙烯的混合物(重
量比3:1混合)10mg装入试样坩埚、隋性参比物a-Al2O3填充于另一坩埚中,样品量一般不超过坩埚容积的2/3,把装样的坩埚在清洁的石台上轻墩数次,使样品松紧适中。
(三)开机
(1)开机过程无先后顺序。恒温水浴及其他仪器应至少提前1h打开。
(2)开机后,首先调整保护气体及吹扫气体输出压力及流速并待其稳定。
(四)样品测试程序
以使用TG-DSC样品支架进行测试为例,升温速度除特殊要求外,一般为10~30K/min。
(五) 测试结果分析
1) 仪器测试结束后打开Tools菜单,从下拉菜单中选择Run analysis program 选
项,进入软件界面。
2) 在分析软件界面中点击工具栏中的Segments按钮,打开Segments对话框,去
掉Segments对话框中的“1”、“2”复选项,点击OK按钮关闭对话框。
3) 点击工具栏上的“X-time/X-temperature”转换开关,使横坐标由时间转换成
温度。
4) 点击待分析曲线使之选中,然后点击工具栏上的“1st Derivative”一次微分
按钮,屏幕上出现一条待分析曲线的一次微分曲线。
5) 完成全部分析内容后,即可打印输出,测试分析操作结束。
五、影响综合热分析的因素
1、 升温速率
2、 样品
3、 气氛
4、 坩埚材质
六、注意事项
1.由于本仪器面板许多参数是出厂设定值,不能任意更改,以免影响仪器正常运行;
2.试样装填和取出动作要轻稳,一般情况由试验老师操作;
3.不得随意更改计算机中的预设参数和端口设置等。
七、实验报告要求
由实验获得TG曲线如下:
TG /%
100DSC /(mW/mg) 放热??
[1]
80
-2
60质量变化: -90.49 %-440-6
-8
20
质量变化: -6.27 %-10
100200300400500温度 /℃600700800
1、分析TG曲线,给出该物质的起始分解温度、终止分解温度、各阶段的失重情况
聚苯乙烯和二氯苯的共混物,第一失重阶段是二氯苯分解 起始温度49.9,终止温度270,实中15.29,第二失重聚苯乙烯分解,383.8 450.77.65
2、分析材料在热处理过程中的热焓变化情况。
第一阶段 170附近的小吸收峰和在370附近的放热峰是二氯化苯发生分解,小吸收峰是因为小分子脱离吸收热量,大放热峰是分解产物的氧化或其他化学反应放出的热量,第二阶段是聚苯乙烯分解长碳链,吸收峰明显,在450的小放热峰是碳的氧化放热。
八、思考题
1.示差扫描量热分析(DSC)的基本原理是什么?
DSC是测量输入到试样和参比物热流量差或功率差与温度或时间的关系. DSC在试样在热反应时发生的热量变化,由于及时输入电功率而得到补偿,所以实际记录的是试样和
参比物下面两只电热补偿的热功率之差随时间t的变化关系。如果升温速率恒定,记录的也就是热功率之差随温度T的变化关系
-
热重分析实验报告
南昌大学实验报告学生姓名学号专业班级实验类型演示验证综合设计创新实验日期20xx0409实验成绩热重分析一实验目的1了解热重分析法…
-
差热分析 实验报告
差热分析【实验目的】1.用差热仪绘制CuSO45H2O等样品的差热图。2.了解差热分析仪的工作原理及使用方法。3.了解热电偶的测温…
-
热分析实验报告
功能材料的动态机械热分析实验报告实验名称粘弹性材料的动态机械热分析实验姓名陈玉立学号SX1101304指导老师沈星一实验目的和要求…
-
材料热分析实验报告
材料的热分析研究林海MG13220xx南京大学物理学院一实验目的1熟悉热分析仪的基本原理2了解热分析仪的构造原理及性能3学习热分析…
- 实验报告 差热分析
-
差热分析 实验报告
差热分析【实验目的】1.用差热仪绘制CuSO45H2O等样品的差热图。2.了解差热分析仪的工作原理及使用方法。3.了解热电偶的测温…
- 实验报告 差热分析
-
差热分析实验报告
深圳大学实验报告课程名称学院化学与化工学院班级实验时间实验报告提交时间教务处制实验目的与要求1用差热分析仪对苏州土进行差热分析并定…
-
差热分析实验报告
差热分析摘要本文阐述了差热分析的基本原理实验及数据处理方法分别测量了锡样品和五水硫酸铜样品的差热曲线并对其进行了分析最后对本实验进…
-
差热分析实验报告
差热分析实验报告一、实验目的1、掌握差热分析的基本原理及测量方法2、学会差热分析仪的操作,并绘制CuSO45H2O等样品的差热图。…
-
差热分析实验报告
错误未找到引用源差热分析摘要本文阐述了差热分析的基本原理实验及数据处理方法分别测量了锡样品和五水硫酸铜样品的差热曲线并对其进行了分…