浙江大学实验报告-电子版

实验报告
课程名称:_______________________________指导老师:________________成绩:__________________
实验名称:_______________________________实验类型:________________同组学生姓名:__________
一、实验目的和要求(必填) 二、实验内容和原理(必填)
三、主要仪器设备(必填) 四、操作方法和实验步骤
五、实验数据记录和处理 六、实验结果与分析(必填)
七、讨论、心得
实验名称:_______________________________姓名:________________学号:__________________
第二篇:浙江大学化工原理(过程工程与控制乙)实验报告 吸收实验
实验报告
课程名称:过程工程原理实验(乙) 指导老师: 成绩:__________________
实验名称:吸收实验 实验类型:工程实验 同组学生姓名:XX
一、实验目的和要求(必填) 二、实验内容和原理(必填)
三、主要仪器设备(必填) 四、操作方法和实验步骤
五、实验数据记录和处理 六、实验结果与分析(必填)
七、讨论、心得
填料塔吸收操作及体积吸收系数测定
1 实验目的:
1.1 了解填料吸收塔的构造并熟悉吸收塔的操作;
1.2 观察填料塔的液泛现象,测定泛点空气塔气速;
1.3 测定填料层压降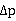 与空塔气速u的关系曲线;
与空塔气速u的关系曲线;
1.4 测定含氨空气—水系统的体积吸收系数 。
。
2 实验装置:
2.1 本实验的装置流程图如图1:




图1.装置图
2.2物系:水—空气—氨气。惰性气体由漩涡气泵提供,氨气由液氮钢瓶提供,吸收剂水采用自来水,他们的流量分别通过转子流量计。水从塔顶喷淋至调料层与自下而上的含氮空气进行吸收过程,溶液由塔底经过液封管流出塔外,塔底有液相取样口,经吸收后的尾气由塔顶排至室外,自塔顶引出适量尾气,用化学分析法对其进行组成分析。
3 基本原理:
3.1 实验中气体流量由转子流量计测量。但由于实验测量条件与转子流量计标定条件不一定相同,故转子流量计的读数值必须进行校正。校正方法如下:
Q= (2)
(2)
式中: —标定状况下空气的密度,1.205kg/m3;
—标定状况下空气的密度,1.205kg/m3;
ρ—被测气体在标定状况下下的密度,kg/m3;
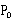 、
、 —标定的空气状况,
—标定的空气状况,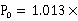 105Pa,
105Pa, =293K;
=293K;
P、T—实际测量时候被测气体的绝对压强、绝对温度,Pa,K。
3.2 体积吸收系数 的测定
的测定
3.2.1相平衡常数m
对相平衡关系遵循亨利定律的物系(一般指低浓度气体),气液平衡关系为:
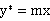 (3)
(3)
相平衡常数m与系统总压P和亨利系数E的关系如下:
 (4)
(4)
式中:E—亨利系数,Pa
P—系统总压(实验中取塔内平均压力),Pa
亨利系数E与温度T的关系为:
lg E= 11.468-1922 / T (5)
式中:T—液相温度(实验中取塔底液相温度),K。
根据实验中所测的塔顶表压及塔顶塔底压差△p,即可求得塔内平均压力P。根据实验中所测的塔底液相温度T,利用式(4)、(5)便可求得相平衡常数m。
3.2.2 体积吸收常数
体积吸收常数 是反映填料塔性能的主要参数之一,其值也是设计填料塔的重要依据。本实验属于低浓气体吸收,近似取Y≈y、X≈x。
是反映填料塔性能的主要参数之一,其值也是设计填料塔的重要依据。本实验属于低浓气体吸收,近似取Y≈y、X≈x。
吸收速率方程为:

则  (6)
(6)
式中: —气相体积吸收系数,kmol/m3·h;
—气相体积吸收系数,kmol/m3·h;
a—单位体积填料层所提供的有效接触面积,m2/m3;
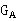 —单位时间内氨气的吸收量,kmol/h;
—单位时间内氨气的吸收量,kmol/h;
Ω—塔截面积,m2;
h—填料层高度,m;
 —吸收推动力,气相对数平均浓度差。
—吸收推动力,气相对数平均浓度差。
为求得 ,需求取
,需求取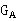 及
及 。
。
3.2.3被吸收的氨气量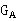 ,可由物料衡算
,可由物料衡算
 (X1-X2) (7)
(X1-X2) (7)
式中:V—惰性气体空气的流量,kmol/h;
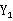 —进塔气相的组成,比摩尔分率,kmol(A)/ kmol(B);
—进塔气相的组成,比摩尔分率,kmol(A)/ kmol(B);
 —出塔气相(尾气)的组成,比摩尔分率,kmol(A)/ kmol(B);
—出塔气相(尾气)的组成,比摩尔分率,kmol(A)/ kmol(B);
X1—出塔液相组成,比摩尔分率,kmol(A)/ kmol(B);
X2=0;
L—吸收剂水的流量,kmol/h。
3.2.3.1 进塔气相浓度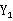 的确定
的确定
 (8)
(8)
式中: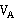 —氨气的流量,kmol/h。
—氨气的流量,kmol/h。
根据转子流量计测取得空气和氨气的体积流量和实际测量状态(压力、温度)。应对其刻度流量进行校正而得到实际体积流量,再由气体状态方程得到空气和氨气的摩尔流量,并由式(8)即可求取进塔气相浓度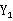 。
。
3.2.3.2 出塔气相(尾气)的组成 的确定
的确定
用移液管移取体积为Va ml、浓度为Ma mol/l的标准硫酸溶液置于吸收瓶中,加入适量的水及2-3滴百里酚兰(指示剂),将吸收瓶连接在抽样尾气管线上(如装置图)。当吸收塔操作稳定时,尾气通过吸收瓶后尾气中的氨气被硫酸吸收,其余空气通过湿式流量计计量。为使所取尾气能反映塔内实际情况,在取样分析前应使取样管尾气保持畅通,然后改变三通旋塞流动方向,使尾气通过吸收瓶。
 (9)
(9)
式中: —氨气的摩尔数,mol;
—氨气的摩尔数,mol;
 —空气的摩尔数,mol。
—空气的摩尔数,mol。
尾气样品中氨的摩尔数 可用下列方式之一测得:
可用下列方式之一测得:
(i)若尾气通入吸收瓶吸收至终点(瓶内溶液颜色由黄棕色变至黄绿色),则
 10-3 mol (10)
10-3 mol (10)
(ii)若通入吸收瓶中的尾气已过量(瓶中溶液颜色呈蓝色),可用同样标准硫酸溶液滴定至终点(瓶中溶液呈黄绿色)。若耗去酸量为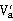 ml,则
ml,则
 10-3 mol (11)
10-3 mol (11)
尾气样品中空气摩尔数 的求取
的求取
尾气样品中的空气量由湿式流量计读取,并测定温度
 mol (12)
mol (12)
式中: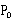 —尾气通过湿式流量计时的压力(由室内大气压代替),Pa;
—尾气通过湿式流量计时的压力(由室内大气压代替),Pa;
 —通过湿式流量计的空气量,l;
—通过湿式流量计的空气量,l;
 —通过湿式流量计的空气温度, K;
—通过湿式流量计的空气温度, K;
R—气体常数,R=8314N·m/(mol·K)。
由式(10)(11)可求得 和
和 ,代人(9)即可得到
,代人(9)即可得到 ,根据得到的
,根据得到的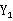 和
和 ,由(7)即可得到
,由(7)即可得到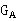 。
。
3.2.4对数平均浓度差 
 (13)
(13)
其中: ;
; 

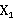 —出塔液相的组成,比摩尔分率,kmol(A)/ kmol(B);
—出塔液相的组成,比摩尔分率,kmol(A)/ kmol(B);
出塔液相浓度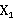 可取塔底液相样品进行化学分析得到,也可用物料衡算式(7)得到。求得
可取塔底液相样品进行化学分析得到,也可用物料衡算式(7)得到。求得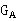 、
、 ,即可由式(6)得到
,即可由式(6)得到 。
。
4 实验步骤:
4.1先开启吸收剂(水)调节阀,当填料充分润湿后,调节阀门使水流量控制在适当的数值,维持恒定;
4.2启动风机,调节风量由小到大,观察填料塔内的流体力学状况,并测取数据,根据液泛时空气转子流量计的读数,来选择合适的空气流量,本实验要求在两至三个不同气体流量下测定 ;
;
4.3为使进塔气相浓度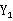 约为5%,须根据空气的流量来估算氨气的流量,然后打开氨气钢瓶,调节阀门,使氨气流量满足要求;
约为5%,须根据空气的流量来估算氨气的流量,然后打开氨气钢瓶,调节阀门,使氨气流量满足要求;
4.4水吸收氨,在很短时间内操作过程便达到稳定,故应在通氨气之前将一切准备工作做好,在操作稳定之后,开启三通阀,使尾气通入吸收瓶进行尾气组成分析。在实验过程中,尤其是测量时,要确保空气、氨气和水流量的稳定;
4.5 改变气体流量或吸收剂(水)流量重复实验:本次实验,控制空气流量分别为8-8-9.6 m3/h,水流量则相对应为30-36-30 l/h;
4.6 实验完毕,关闭氨气钢瓶阀门、水调节阀,切断风机电源,洗净分析仪器等。
5 实验数据处理:
5.1 大气压:776.30mmHg;填料层高度:41cm;填料塔内径:70mm;标准酸浓度:0.025M
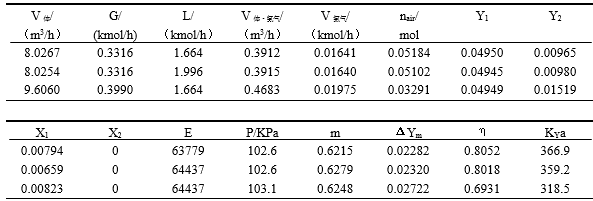
5.2 原始数据记录:
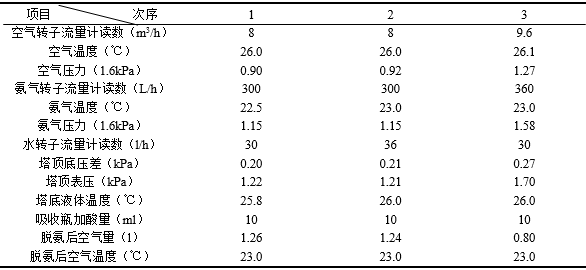
5.3数据处理:
塔截面积Ω=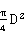 =0.00385m2 P=P0+P表
=0.00385m2 P=P0+P表
计算示例(以第一组为例):
V体= =8*
=8* =8.0267 m3/h;
=8.0267 m3/h;
G=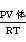 =(1.6*0.90+101.3)*8.0267/8.314/(273.15+26.0)=0.3316 kmol/h;
=(1.6*0.90+101.3)*8.0267/8.314/(273.15+26.0)=0.3316 kmol/h;
L=ρL0/M=998.2*30/18/1000=1.664 kmol/h;
V体·氨气= =300*0.001*
=300*0.001* =0.3912 m3/h;
=0.3912 m3/h;
V氨气=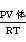 =(1.6*1.15+101.3)*0.3912/8.314/(273.15+22.5)=0.01641 kmol/h;
=(1.6*1.15+101.3)*0.3912/8.314/(273.15+22.5)=0.01641 kmol/h;
nair= =101.3*1.26/8.314/(273.15+23)=0.05184mol;
=101.3*1.26/8.314/(273.15+23)=0.05184mol;
Y1= =0.01641/0.3316=0.04950;
=0.01641/0.3316=0.04950;
Y2= =0.025*0.01*2/0.05184=0.00965;
=0.025*0.01*2/0.05184=0.00965;
X1= (Y1-Y2)=0.3316*(0.04950-0.00965)/1.664=0.00794;
(Y1-Y2)=0.3316*(0.04950-0.00965)/1.664=0.00794;
E=1011.468-1992/()273.15+25.8=63779;
P=(2*1.22+0.20)/2+101.3=102.6kPa,P为塔内平均压力;
m=E/P=63779/102.6/1000=0.6315;
 =
=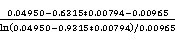 =0.02282;
=0.02282;
η=1-Y2/Y1=1-0.00965/0.04950=0.8052;
 =
=  =366.9。
=366.9。
6 结果分析、讨论:
6.1 本次实验分别通过改变吸收剂流量和空气流量来讨论对吸收的影响。从实验数据处理的结果可以看出,第一组和第二组之间,空气流量不变,增大水的流量,出口气体浓度变大,体积吸收系数也变小,且两者相差不多;而第一组和第三组之间,水流量保持不变,增大空气流量,出口气体流量也变大,体积吸收系数也跟着变小,且小得多。
6.2 根据氨气易容于水的性质,理论上氨气应该属于气模控制,而根据化工原理理论知识,气模控制的时候,增大吸收剂流量时,出口气体浓度减小,吸收率增大,Kya 增大;当增大气体流速时,出口气体浓度增大, 吸收率减小,Kya 也增大,且比前者要大得多。
即本实验所得结果于理论上应有的结果有极大的偏差,分析原因,我认为很有可能是第三组实验数据中脱氨后空气量读数结果存在较大偏差,导致氨气浓度出现较大误差,导致实验结果不理想。按照吸收理论,第三组数据中的脱氨后空气量应与第一组差不多,因为吸收剂水的流量没有改变,氨气与空气的比例也没有改变。之所以会有这样的偏差产生,原因是多样的。
首先,过程控制原理实验是工程实验,其实验结果于理论值出现偏差并不足为奇。其次,在实验过程中,各个数据的读数也一定存在误差,由于操作者操作水平的限制等原因,也会使得实验数据出现较大的偏离。
6.3 从实验基本数据可以看出,不论是改变吸收剂流量或是空气流量,实验中测得的塔底液体温度和脱氨后空气温度都没有发生变化或者波动很小,可以认为不变化,而理论上认为,随着气体或者吸收剂流量的改变,脱氨后空气温度也会发生变化,其原因可能是因为实验当天室温比较高所致。
6.4 从实验数据处理结果可以看出,当保持空气流量不变而增大水流量时,吸收效率下降很少,而相反地,保持水流量不变,增大空气流量时,吸收效率大幅度下降。而吸收剂流量小到一定程度则达不到吸收要求,所以应适当合理选取吸收剂用量。
7思考题:
7.1 要测定体积吸收系数 ,需要测定哪些数据?使用哪些仪表?
根据实验知道,要测定体积吸收系数,需要测定的数据有空气体积流量、空气温度和压力、氨气体积流量、氨气温度和压力、塔顶底压差、塔顶表压、水温、塔底液温、脱氨后空气量、尾气温度、氨气摩尔质量等。
使用的仪表有转子流量计、温度计、压差计等。
7.2 实验时,如何确定水、空气和氨气的流量?
水的体积流量可直接从转子流量计上读取,再转化为摩尔流量;空气和氨气的体积流量则先从转子流量计上读取,利用校正公式进行校正,然后再转化为摩尔流量。
7.3 怎么样判断实验过程处于稳定状态?
全塔压力基本保持不变时即可判断实验过程处于稳定状态,此时可以读取实验所需数据。
7.4 为什么吸收时氨气从气相转移到液相?空气量改变对KYa有何影响?
吸收的基本原理就是利用气体在吸收剂中溶解度不同来分离气体,在本实验中,氨气易溶于水,在气相和液相之间存在浓度差,这是发生传质过程的根本动力和原因。
按照吸收理论,当增大气体流速时,出口气体浓度增大,吸收率减小,KYa增大。
参考文献:《过程工程原理实验(乙)》 . 杭州:浙江大学化学工程实验室 . 2009.8.
《化工原理上、下册》 . 何潮洪等 . 北京:科学出版社 . 2008.5.
-
浙大标准实验报告纸
实验报告装订线课程名称指导老师成绩实验名称实验类型同组学生姓名一实验目的和要求必填二实验内容和原理必填三主要仪器设备必填四操作方法…
-
浙江大学实验报告模板
实验报告课程名称指导老师成绩实验名称实验类型同组学生姓名一实验目的和要求必填二实验内容和原理必填三主要仪器设备必填四操作方法和实验…
-
浙江大学实验报告用纸(标准格式)
实验报告课程名称生理学及实验乙指导老师成绩实验名称蟾蜍坐骨神经干复合动作电位特性实验类型同组学生姓名陈琳黄丽聪一实验目的二实验原理…
-
浙江大学城市学院实验报告封面
编号学年第学期实验报告实验课程名称专业班级学生学号学生姓名实验指导教师浙江大学城市学院实验报告纸实验名称指导老师成绩专业班级姓名学…
-
浙江大学实验报告用纸(标准格式)
实验报告课程名称:_______________________________指导老师:________________成绩:_…
-
浙大电工电子实验报告 实验十五 集成定时器及其应用
实验报告课程名称:电工电子学实验指导老师:实验名称:集成定时器及其应用一、实验目的1.了解集成定时器的功能和外引线排列。2.掌握用…
-
浙大Word操作实验报告
实验指导书第四章word操作P74五实验报告第12题1写出操作题的步骤并附上课程表题目一新建Word文档在文本编辑区输入Word实…
-
浙大版电工电子学实验报告02单向交流电路
实验报告课程名称电工电子学实验指导老师实验名称单向交流电路一实验目的1学会使用交流仪表电压表电流表功率表2掌握用交流仪表测量交流电…
-
浙大版电工电子学实验报告15集成定时器及其应用
实验报告课程名称电工电子学实验指导老师实验名称集成定时器及其应用一实验目的1了解集成定时器的功能和外引线排列2掌握用集成定时器构成…
-
浙江大学化学实验报告模板
实验报告课程名称指导老师成绩实验名称实验类型同组学生姓名一实验目的和要求必填三主要仪器设备必填五实验数据记录和处理七讨论心得一实验…
-
20xx-20xx-1大学计算机基础实验报告样式(新)
大学计算机基础实验报告格式要求本课程要求完成3个实验报告,即应用WindowsXP管理计算机、Word文档的编辑与排版、计算机网络…