原电池电动势的测定与应用物化实验报告
原电池电动势的测定及热力学函数的测定
一、实验目的
1) 掌握电位差计的测量原理和测量电池电动势的方法;
2) 掌握电动势法测定化学反应热力学函数变化值的有关原理和方法;
3) 加深对可逆电池,可逆电极、盐桥等概念的理解;
4) 了解可逆电池电动势测定的应用;
5) 根据可逆热力学体系的要求设计可逆电池,测定其在不同温度下的电动势值,计算电池反应的热力学函数△G、△S、△H。
二、实验原理
1.用对消法测定原电池电动势:
原电池电动势不能能用伏特计直接测量,因为电池与伏特计连接后有电流通过,就会在电极上发生生极化,结果使电极偏离平衡状态。另外,电池本身有内阻,所以伏特计测得的只是不可逆电池的端电压。而测量可逆电池的电动势,只能在无电流通过电池的情况下进行,因此,采用对消法。对消法是在待测电池上并联一个大小相等、方向相反的外加电源,这样待测电池中没有电流通过,外加电源的大小即等于待测电池的电动势。
2.电池电动势测定原理:
Hg | Hg2Cl2(s) | KCl( 饱和 ) | | AgNO3 (0.02 mol/L) | Ag
根据电极电位的能斯特公式,正极银电极的电极电位:
其中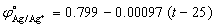 ;而
;而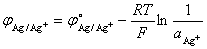
负极饱和甘汞电极电位因其氯离子浓度在一定温度下是个定值,故其电极电位只与温度有关,其关系式: φ饱和甘汞 = 0.2415 - 0.00065(t – 25)
而电池电动势  ;可以算出该电池电动势的理论值。与测定值比较即可。
;可以算出该电池电动势的理论值。与测定值比较即可。
3.电动势法测定化学反应的△G、△H和△S:
如果原电池内进行的化学反应是可逆的,且电池在可逆条件下工作,则此电池反应在定温定压下的吉布斯函数变化△G和电池的电动势E有以下关系式:
△rGm =-nFE
从热力学可知: 
△H=-nFE+△S
4.注意事项:
①盐桥的制备不使用:重复测量中须注意盐桥的两端不能对调;
②电极不要接反;
三、.实验仪器及用品
1.实验仪器
SDC数字电位差计、饱和甘汞电极、光亮铂电极、银电极、250mL烧杯、20mL烧杯、U形管
2.实验试剂
0.02mol/L的硝酸银溶液、饱和氯化钾溶液、硝酸钾、琼脂
四、实验步骤
1.制备盐桥
3%琼脂-饱和硝酸钾盐桥的制备方法:在250mL烧杯中,加入100mL蒸馏水和3g琼脂,盖上表面皿,放在石棉网上用小火加热至近沸,继续加热至琼脂完全溶解。然后加入40g硝酸钾,充分搅拌使硝酸钾完全溶解后,趁热用滴管将它灌入干净的U形管中,两端要装满,中间不能有气泡,静置待琼脂凝固后便可使用。制备好的盐桥丌使用时应浸入饱和硝酸钾溶液中,防止盐桥干涸。
2.组合电池
将饱和甘汞电极插入装有饱和硝酸钾溶液的广口瓶中。将一个20mL小烧杯洗净后,用数毫升0.02mol/L的硝酸银溶液连同银电极一起淌洗,然后装此溶液至烧杯的2/3处,插入银电极,用硝酸钾盐桥不饱和甘汞电极连接构成电池。
3.测定电池的电动势
①根据Nernst公式计算实验温度下电池(I)的电动势理论值。
②正确接好测量电池(I)的线路。电池与电位差计连接时应注意极性。盐桥的两支管应标号,让标负号的一端始终不含氯离子的溶液接触。仪器要注意摆布合理并便于操作。
③用SDC数字电位差计测量电池(I)的电动势。每隔2min测一次,共测三次。
④接通恒温槽电源进行恒温,使其分别达到25.2℃、35.2℃,温度波动范围要求控制在正负0.2℃之内。把被测电池放入恒温槽中恒温15min,同时将原电池引出线连接到SDC型数字式电位差计的待测接线柱上(注意正负极的连接),测定其电动势,每5分钟测1次,直至电位差计读书稳定为止。
⑤测量完毕后,倒去两个小烧0.55杯的溶液,洗净烧杯的溶液。
五、实验数据记录与处理
1、电动势的测定
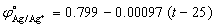 ;
;
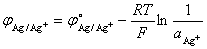 ;
;
φ饱和甘汞 = 0.2415 - 0.00065(t – 25);
通过以上三式可求得电池电动势  的理论值。
的理论值。
气压:101.6KPa

2、热力学函数的测定—--测定△G、△S和△H。
作E-T图(见下图),求得斜率 为-6.4×10∧-4,
为-6.4×10∧-4,

E-T图的直线方程为:Y =0.64812-6.4×10∧-4 X ,故 =--6.4×10∧-4
=--6.4×10∧-4
所以当T=298K时,
△rGm=-nFE=-1×96500×0.45740 = -44139.1 J/mol = -44.14 kJ/mol
因为 所以△S=1×96500×(-6.4×10∧-4 ) =-61.6 J/(mol·K)
所以△S=1×96500×(-6.4×10∧-4 ) =-61.6 J/(mol·K)
因为△H=△rGm +T△S, 所以△H= -44139.1-61.6×298=-62.5kJ/mol
热力学函数

3、将实验所得的电池反应的热力学函数变化值和理论值进行比较
电池总反应
查参考文献得Ag+(aq)、Cl-(aq)、AgCl(c) 在298K时各自的的标准生成焓变ΔfHºm、标准生成自由能变ΔfGºm及标准熵Sºm,由此计算出电池反应的ΔfHºm、ΔfGºm、ΔfSºm如下所示.
Ag+(aq)、Cl-(aq)、AgCl(c) 的ΔfHºm、ΔfGºm、ΔfSºm

而热力学函数(298K)的理论值:
ΔrGºm=-44.1 kJ/mol  ;ΔrSºm= -61.6 J/(mol·K) ;ΔrHºm= -62.5 kJ/mol
;ΔrSºm= -61.6 J/(mol·K) ;ΔrHºm= -62.5 kJ/mol
则对比文献值可得:
ΔrGºm 相对误差:(-44.1-(-51.31))/-51.31 = -14.1 %
ΔrSºm 相对误差:(-61.6-(-69.35))/-69.35 =-11.1 %
ΔrHºm 相对误差:(-62.5 -(-71.07))/-71.07=-12.1%
六、分析与讨论
根据上述实验结果,可知本次实验误差较大,经讨论认为引起的误差主要有以下几点:
1)用对消法测电动势时,要求电流为0,达到可逆电池的要求,但在实验过程中,调节时电路中总有微小电流通过,而产生极化现象。但当外加电压大于电动势时,原电池相当于电解池,使反应电势增加;相反,当外电压小于电动势时,原电池放电极化,使反应电势降低,这会影响实验结果的测定。而且有少量电流也会使内阻分走部分电压,导致测量电压并不等于电动势而等于外电路电压。
2)在本次实验中,我们只进行了两组不同温度的数据测量,使用的热力学计算方法均为粗略计算,作E-T图也只是2个数据点,因数据处理方法粗略,所以计算结果相对误差也较大。因此应该进行更多组在不同温度下的测定,绘出δE/δT的关系图,拟合线性,求出斜率,这样误差才小。
3)本实验测定的并不是可逆电池,但在溶液间插入了盐桥,近似地当作可逆电池来处理。通常,常用的盐桥是氯化钾盐桥,离子相对迁移速率较为一致。但对于硝酸银溶液,不能使用氯化钾盐桥,而是采用了硝酸钾盐桥。虽然硝酸钾盐桥的正负离子迁移数较接近,但是它们与通电极无共同离子,因而在使用时会改变参考电极的浓度和引入外来离子,从而可能改变参考电极电位,造成实验误差。
4)这次实验中有很多的近似处理,比如液接电势、接触电势和扩散电势的忽略,电池近似处理为可逆电池等等。因而,实验结果与实际值有一定的偏差。
5)调节电桥平衡的操作时间应尽可能的短,否则电极上较长时间的有电流通过,会发生电池反应使得溶液浓度下降、电极表面极化,这样可逆电极变成不可逆的,会给实验带来较大误差。而实验中所用仪器不稳定,需要较长的时间才能大致调节到平衡,即使是同一个电动势值,在很短的时间内测得的数据都有较大波动,所以不能很快调节到平衡也会造成实验的误差;
6)实验过程中,恒温槽温度存在波动,会造成不稳定,温度会0.2℃左右波动。④恒温槽温度存在波动,所以在实验测定过程中,电池反应并不完全是在同一温度下进行,进行数据处理时也会带来一定的误差。在此外实验中采用盐桥来消除液接电位,但实际实验中不能保证盐桥能够完全消除液接电位。
7)本实验的理论参考数据是在标准状况下的数值,而实验过程中的温度和大气压都有变化,所以也存在一定的误差。
七、思考题
1、为何测电动势要用对消法,对消法的原理是什么?
答:原电池电动势不能直接用伏特计来测量,因为电池与伏特计接通后会有电流通过,在电池两级上会存在极化现象,使电极偏离平衡状态,另外,电池本身有内阻,伏特计测量得到的仅是不可逆电池的端电压。采用对消法(又叫补偿法)可在无电流或很小电流通过电池的情况下准确测定电池的电动势。
对消法的原理是:在待测电池上并联一个大小相等、方向相反的外加电势差,这样待测电池中没有电流通过,外加电势差的大小即等于待测电池的电动势。
2、测电动势为何要用盐桥,如何选用盐桥以适应各种不同的体系?
答:盐桥可将液接电势降低到最小的作用。选择盐桥的原则是:盐桥中的盐浓度尽量大(一般用饱和溶液),正负离子迁移数接近,与电池中的电解质不发生反应。所选取的KNO3的在水中的溶解度很大,正负负离子迁移数接近,与大多数电解质不发生反应,故可以作为大多数体系的盐桥。
3、用测电动势的方法求热力学函数有何优越性?
答:电动势测定法比其它方法(例如量热法)更精确,误差更小。因为电池电动势可以测得很准,其数据较化学方法准确可靠。
参考文献:
[1] 何广平,南俊民,孙艳辉.物理化学实验.化学工业出版社, 2008, 92-99
[2] 傅献彩, 沈文霞, 姚天扬. 物理化学. 高等教育出版社, 2008:64-65
[3] 栾翀. 电动势的测定及其应注意的问题[J]. 科技信息. 2008(35)
[4] 凌勋利,王晔,韩民乐,王跃. 电化学方法测定化学反应热力学函数的变化值[J]. 洛阳师范学院学报. 2010(02)
第二篇:原电池电动势的测定实验报告
实验九 原电池电动势的测定及应用

一、实验目的
1.测定Cu-Zn电池的电动势和Cu、Zn电极的电极电势。
2.学会几种电极的制备和处理方法。
3.掌握数字电位差计的测量原理和正确的使用方法。
二、实验原理
电池由正、负两极组成。电池在放电过程中,正极起还原反应,负极起氧化反应,电池内部还可以发生其它反应,电池反应是电池中所有反应的总和。
电池除可用来提供电能外,还可用它来研究构成此电池的化学反应的热力学性质。从化学热力学知道,在恒温、恒压、可逆条件下,电池反应有以下关系:
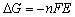 (9-1)
(9-1)
式中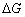 是电池反应的吉布斯自由能增量;n为电极反应中得失电子的数目;F为法拉第常数(其数值为96500
是电池反应的吉布斯自由能增量;n为电极反应中得失电子的数目;F为法拉第常数(其数值为96500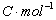 );E为电池的电动势。所以测出该电池的电动势E后,进而又可求出其它热力学函数。但必须注意,测定电池电动势时,首先要求电池反应本身是可逆的,可逆电池应满足如下条件:
);E为电池的电动势。所以测出该电池的电动势E后,进而又可求出其它热力学函数。但必须注意,测定电池电动势时,首先要求电池反应本身是可逆的,可逆电池应满足如下条件:
(1)电池反应可逆,亦即电池电极反应可逆;
(2)电池中不允许存在任何不可逆的液接界;
(3)电池必须在可逆的情况下工作,即充放电过程必须在平衡态下进行,亦即允许通过电池的电流为无限小。
因此在制备可逆电池、测定可逆电池的电动势时应符合上述条件,在精确度不高的测量中,常用正负离子迁移数比较接近的盐类构成“盐桥”来消除液接电位。
在进行电池电动势测量时,为了使电池反应在接近热力学可逆条件下进行,采用电位计测量。原电池电动势主要是两个电极的电极电势的代数和,如能测定出两个电极的电势,就可计算得到由它们组成的电池的电动势。由(9-1)式可推导出电池的电动势以及电极电势的表达式。下面以铜-锌电池为例进行分析。电池表示式为:
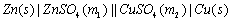
符号“|”代表固相(Zn或Cu)和液相(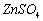 或
或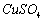 )两相界面;“‖”代表连通两个液相的“盐桥”;
)两相界面;“‖”代表连通两个液相的“盐桥”;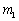 和
和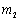 分别为
分别为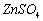 和
和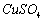 的质量摩尔浓度。
的质量摩尔浓度。
当电池放电时,
负极起氧化反应: 
正极起还原反应: 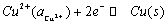
电池总反应为: 
电池反应的吉布斯自由能变化值为:
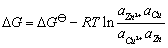 (9-2)
(9-2)
上述式中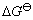 为标准态时自由能的变化值;
为标准态时自由能的变化值;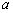 为物质的活度,纯固体物质的活度等于1,即
为物质的活度,纯固体物质的活度等于1,即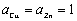 。而在标态时,
。而在标态时,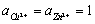 ,则有:
,则有:
 (9-3)
(9-3)
式中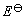 为电池的标准电动势。由(9-1)至(9-1)式可得:
为电池的标准电动势。由(9-1)至(9-1)式可得:
 (9-4)
(9-4)
对于任一电池,其电动势等于两个电极电势之差值,其计算式为:
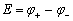 (9-5)
(9-5)
对铜-锌电池而言 
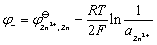
式中 和
和 是当
是当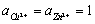 时,铜电极和锌电极的标准电极电势。
时,铜电极和锌电极的标准电极电势。
对于单个离子,其活度是无法测定的,但强电解质的活度与物质的平均质量摩尔浓度和平均活度系数之间有以下关系: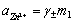
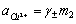
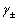 是离子的平均离子活度系数,其数值大小与物质浓度、离子的种类、实验温度等因数有关。
是离子的平均离子活度系数,其数值大小与物质浓度、离子的种类、实验温度等因数有关。
在电化学中,电极电势的绝对值至今无法测定,在实际测量中是以某一电极的电极电势作为零标准,然后将其它的电极(被研究电极)与它组成电池,测量其间的电动势,则该电动势即为该被测电极的电极电势。被测电极在电池中的正、负极性,可由它与零标准电极两者的还原电势比较而确定。通常将氢电极在氢气压力为101325Pa,溶液中氢离子活度为1时的电极电势规定为零伏,即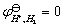 ,称为标准氢电极,然后与其它被测电极进行比较。
,称为标准氢电极,然后与其它被测电极进行比较。
由于氢电极使用不便,常用另外一些易制备、电极电势稳定的电极作为参比电极,常用的参比电极有甘汞电极。
以上所讨论的电池是在电池总反应中发生了化学变化,因而被称为化学电池。还有一类电池叫做浓差电池,这种电池在净作用过程中,仅仅是一种物质从高浓度(或高压力)状态向低浓度(或低压力)状态转移,从而产生电动势,而这种电池的标准电动势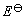 等于零伏。
等于零伏。
例如电池 就是浓差电池的一种。
就是浓差电池的一种。
电池电动势的测量工作必须在电池可逆条件下进行,必须指出,电极电势的大小,不仅与电极种类、溶液浓度有关,而且与温度有关。本实验是在实验温度下测得的电极电势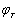 ,由(9-6)式和(9-7)式可计算
,由(9-6)式和(9-7)式可计算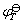 。为了比较方便起见,可采用下式求出298K时的标准电极电势
。为了比较方便起见,可采用下式求出298K时的标准电极电势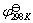 。
。

式中 、
、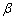 为电极电势的温度系数。对于Cu-Zn电池来说:
为电极电势的温度系数。对于Cu-Zn电池来说:
铜电极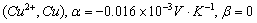
锌电极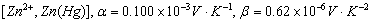
三、仪器和试剂

四、实验步骤
1.电极的制备
(1)锌电极:将锌电极在稀硫酸溶液中浸泡片刻,取出洗净,再浸入汞或饱和硝酸亚汞溶液中约10s,表面上即生成一层光亮的汞齐,用水冲洗晾干后,插入0.1000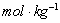
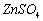 中待用。
中待用。
(2)铜电极:将铜电极在6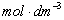 的硝酸溶液中浸泡片刻,取出洗净,将铜电极置于电镀烧杯中作为阴极,另取一个经清洁处理的铜棒作阳极,进行电镀,电流密度控制在20
的硝酸溶液中浸泡片刻,取出洗净,将铜电极置于电镀烧杯中作为阴极,另取一个经清洁处理的铜棒作阳极,进行电镀,电流密度控制在20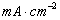 为宜。其电镀装置如图9-1所示。电镀半小时,使铜电极表面有一层均匀的新鲜铜,洗净后放入0.1000
为宜。其电镀装置如图9-1所示。电镀半小时,使铜电极表面有一层均匀的新鲜铜,洗净后放入0.1000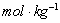
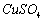 中备用。
中备用。
2.电池组合
将饱和KCl溶液注入50mL的小烧杯内,制盐桥,再将上面制备的锌电极和铜电极
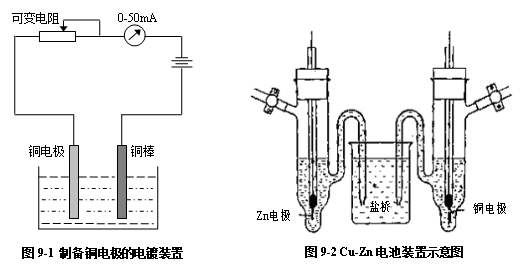 置于小烧杯内,即成Cu-Zn电池:
置于小烧杯内,即成Cu-Zn电池:
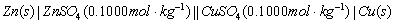
电池装置如图9-2所示。
同法组成下列电池:
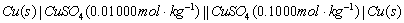
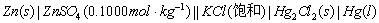
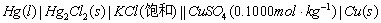
3.电动势的测定
(1)按照电位差计电路图,接好电动势测量线路。
(2)根据标准电池的温度系数,计算实验温度下的标准电池电动势。以此对电位差计进行标定。
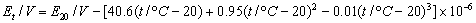
(3)分别测定以上电池的电动势。
五、数据记录及处理
1.将试验数据列表。
标准溶液NaoH浓度为0.102mol/L
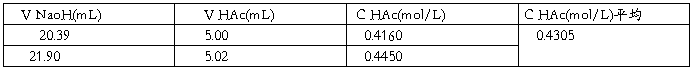
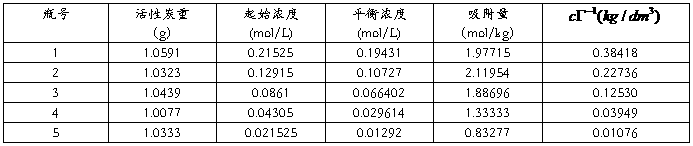
2.计算各瓶中醋酸的起始浓度c0,平衡浓度c及吸附量?(mol? kg-1)。
计算结果如上表。
由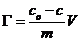 计算吸附量。
计算吸附量。
3.吸附量对平衡浓度作等温线。

4.作c/?-c图,并求出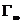 和常数K。
和常数K。
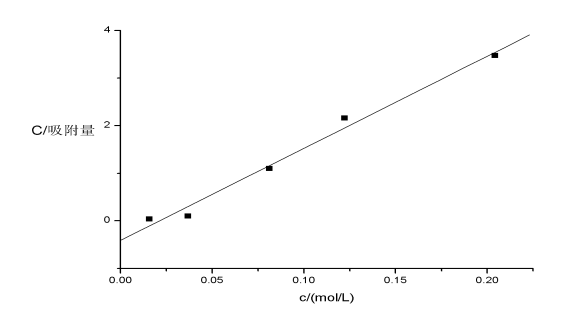
由直线斜率得: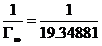
 =0.05168mol/kg
=0.05168mol/kg
由直线截距得: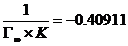
K=-47.29
5.由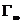 计算活性炭的比表面。
计算活性炭的比表面。

=756.006
● 结果与讨论
1.比表面测定与哪些因素有关,为什么?
a. 测定固体比表面时所用溶液中溶质的浓度要选择适当,即初始溶液的浓度以及吸附平衡后的浓度都选择在合适的范围内。既要防止初始浓度过高导致出现多分子层吸附,又要避免平衡后的浓度过低使吸附达不到饱和。如次甲基蓝在活性炭上的吸附实验中原始溶液的浓度为2g·dm-3左右,平衡溶液的浓度不小于1mg·dm-3。
b. 按朗格谬尔吸附等温线的要求,溶液吸附必须在等温条件下进行,使盛有样品的三角瓶置于恒温器中振荡,使之达到平衡。本实验是在空气浴中将盛有样品的三角瓶置于振荡器上振荡。实验过程中温度会有变化,这样会影响测定结果。
2.由于实验酸碱滴定过程中,滴定的体积存在一定的偏差,所以导致实验结果1和3瓶所测得结果存在偏差,故在酸碱滴定中需要操作规范,使实验结果更精准.
六、注意事项
1.制备电极时,防止将正负极接错,并严格控制电镀电流。
2.甘汞电极使用时请将电极帽取下,用完后用氯化钾溶液浸泡。
七、思考题
1.电位差计、标准电池各有什么作用?如何保护及正确使用?
2.参比电极应具备什么条件?它有什么功用?
3.若电池的极性接反了有什么后果?
附录 SDC-Ⅲ数字电位差计
一、SDC-Ⅲ数字电位差计的特点
一体设计:将UJ系列电位差计、光电检流计、标准电池等集成一体,体积小,重量轻,便于携带。
数字显示:电位差值七位显示,数值直观清晰、准确可靠。
内外基准:即可使用内部基准进行测量,又可外接标准作基准进行测量,使用方便灵活。
误差较小:保留电位差计测量功能,真实体现电位差计对检测误差微小的优势。
性能可靠:电路采用对称漂移抵消原理,克服了元器件的温漂和时漂,提高测量的准确度。
二、使用条件
电源:~220V±10%;50Hz
环境:温度-10℃~40℃;湿度≤85%
三、使用方法
1.开机
用电源线将仪表后面板的电源插座与~220V电源连接,打开电源开关(ON),预热15分钟。
2.以内标或外标为基准进行测量
(1)将被测电动势按“+、-”极性与测量端子对应连接好。
(2)采用“内标”校验时,将“测量选择”至于“内标”位置,将100位旋置于1,其余旋钮和补偿旋钮逆时针旋到底,此时“电位指标”显示为“1.00000V”,待检零指示数值稳定后,按下“采零”键,此时,检零指示应显示“0000”。
(3)采用“外标”校验时,将外标电池的“+、-”极性按极性与“外标”端子接好,将“测量选择”置于“外标”,调节“100~10-4”和补偿电位器,使“电位指示”数值与外标电池数值相同,待“检零指示”数值稳定之后,按下“采零”键,此时“检零指示”为“0000”。
(4)仪器用“内标”或“外标”,校验完毕后将被测电动势按“+、-”极性与“测量”端子接好,将“测量选择”置于“测量”,将“补偿”电位器逆时针旋到底,调节“100~10-4”五个旋钮,使“检零指示”为“-”,且绝对值最小时,再调节补偿电位器,使“检零指示”为“0000”,此时,“电位指示”数值即为被测电动势的大小。
3.关机:首先关闭电源开关(OFF),然后拔下电源线。
四、注意事项
1.置于通风、干燥、无腐蚀性气体的场合。
2.不宜放置在高温环境,避免靠近发热源如电暖气或炉子等。
3.为了保证仪表工作正常,请勿打开机盖进行检修,更不允许调整和更换元件,否则将无法保证仪表测量的准确度。
4.若波段开关旋纽松动或旋纽指示错位,可打开旋纽盖,用备用呆扳手对准槽口拧紧即可。
-
原电池电动势的测定实验报告
实验九原电池电动势的测定及应用一实验目的1测定CuZn电池的电动势和CuZn电极的电极电势2学会几种电极的制备和处理方法3掌握SD…
-
物理化学实验-电池电动势的测定实验报告
原电池电动势的测定与应用华南师范大学化学与环境学院合作指导老师林晓明一实验目的掌握电位差计的测量原理和原电池电动势的测定方法加深对…
-
实验十 原电池电动势的测定
深圳大学实验报告课程名称报告人班级实验时间实验报告提交时间教务部制目的要求1测定CuZn电池的电动势和CuZn电极的电极电位2了解…
-
原电池电动势的测定实验报告 浙江大学
实验报告课程名称:大学化学实验p实验类型:中级化学实验实验项目名称:原电池电动势的测定同组学生姓名:无指导老师##一、实验目的和要…
-
大学物理化学实验报告-原电池电动势的测定
物理化学实验报告院系化学化工学院班级学号姓名实验名称原电池电动势的测定日期同组者姓名史黄亮室温1684气压1017kPa成绩一目的…
-
物化实验报告7-电动势的测定及应用
一实验目的1通过实验加深对可逆电池可逆电极盐桥等概念的理解2掌握对消法测定电池电动势的原理及电位差计的使用方法3通过电池AgAgN…
-
大学物理化学实验报告-原电池电动势的测定
物理化学实验报告院系化学化工学院班级学号姓名实验名称原电池电动势的测定日期同组者姓名史黄亮室温1684气压1017kPa成绩一目的…
-
物理化学实验报告-电池电动势的测定及其应用
电池电动势的测定及其应用摘要在本实验中我们利用对消法测量电池电动势并计算相关热力学常数首先我们通过测量电池AgsAgClsKClm…
- 电池电动势及温度系数的测定-实验报告(四川理工学院)
-
原电池电动势的测定及其应用
电动势的测定及其应用姓名学号学院班级一实验目的1掌握对消法测定电池电动势的原理及电位差计的使用2学会银电极银氯化银电极的制备和盐桥…
-
原电池电动势的测定实验报告 浙江大学
实验报告课程名称:大学化学实验p实验类型:中级化学实验实验项目名称:原电池电动势的测定同组学生姓名:无指导老师##一、实验目的和要…