分析化学设计实验报告单—水果中维生素C的测定
昌吉学院化学与应用化学系
20##—20##学年度第二学期
分析化学设计实验
化学与应用化学系B0901班
做实验者:马国民
二零##年六月十九日
分析化学设计实验报告单
实验名称:柠檬中维生素C含量的测定
院系名称:化学与应用化学系
专业名称:化学
学生姓名:马国民
学生学号:0925814027
指导老师:魏玲老师
化学与应用化学系B0901班
20##年6月19日
分析设计试验实验内容
一、实验来源与原理
维生素C又叫L-抗坏血酸,是一种水溶性维生素。食物中的维生素C被人体小肠上段吸收。一旦吸收,就分布到体内所有的水溶性结构中,正常成人体内的维生素C代谢活性池中约有1500mg维生素C,最高峰值为3000mg维生素C。当维生素C缺乏时,会患坏血病等一些疾病,严重缺乏甚至会造成死亡。人和一些高等动物与植物以及低等动物不同,不能自身合成维生素C,只能从食物中摄取。桔子含水量高,营养丰富,含大量维生素C,枸橼酸及葡萄糖等十余种营养物质。柠檬的营养丰富,在每百克柠檬果肉中,含蛋白质0.9克,脂肪0.2克,碳水化合物5.5克,灰份0.3克,钙24毫克,铁0.1毫克,钾120毫克,尼克酸0.1毫克,维生素C 11毫克以及许多人体必须的微量元素。
维生素C主要生理功能:
近代研究表明VC对人体健康至关重要: 1.胶原蛋白的合成需要维生素C参加,所以VC缺乏 食用富含维生素C的食物可防晒,胶原蛋白不能正常合成,导致细胞连接障碍。人体由细胞组成,细胞靠细胞间质把它们联系起来,细胞间质的关键成分是胶原蛋白。胶原蛋白占身体蛋白质的1/3,生成结缔组织,构成身体骨架。如骨骼、血管、韧带等,决定了皮肤的弹性,保护大脑,并且有助于人体创伤的愈合。 2.坏血病。血管壁的强度和VC有很大关系。微血管是所有血管中最细小的,管壁可能只有一个细胞的厚度,其强度、弹性是由负责连接细胞具有胶泥作用的胶原蛋白所决定。当体内VC不足,微血管容易破裂,血液流到邻近组织。这种情况在皮肤表面发生,则产生淤血、紫癍;在体内发生则引起疼痛和关节涨痛。严重情况在胃、肠道、鼻、肾脏及骨膜下面均可有出血现象,乃至死亡。 3.牙龈萎缩、出血。健康的牙床紧紧包住每一颗牙齿。牙龈是软组织,当缺乏蛋白质、钙、VC时易产生牙龈萎缩、出血。 4.预防动脉硬化。可促进胆固醇的排泄,防止胆固醇在动脉内壁沉积,甚至可以使沉积的粥样斑块溶解。 5.是一种水溶性的强有力的抗氧化剂。可以保护其它抗氧化剂,如维生素A、维生素E、不饱和脂肪酸,防止自由基对人体的伤害。 6.治疗贫血。使难以吸收利用的三价铁还原成二价铁,促进肠道对铁的吸收,提高肝脏对铁的利用率,有助于治疗缺铁性贫血。 7.防癌。丰富的胶原蛋白有助于防止癌细胞的扩散;VC的抗氧化作用可以抵御自由基对细胞的伤害防止细胞的变异;阻断亚硝酸盐和仲胺形成强致癌物亚硝胺。曾有人对因癌症死亡病人解剖发现病人体内的VC含量几乎为零。 8.保护细胞、解毒,保护肝脏。在人的生命活动中,保证细胞的完整性和代谢的正常进行至关重要。为此,谷胱甘肽和酶起着重要作用。谷胱甘肽是由谷氨酸、胱氨酸和甘氨酸组成的短肽,在体内有氧化还原作用。它有两种存在形式,即氧化型和还原型,还原型对保证细胞膜的完整性起重要作用。VC是一种强抗氧化剂,其本身被氧化,而使氧化型谷胱甘肽还原为还原型谷胱甘肽,从而发挥抗氧化作用。酶是生化反应的催化剂,有些酶需要有自由的巯基(-SH)才能保持活性。VC能够使双硫键(-S-S)还原为-SH,从而提高相关酶的活性,发挥抗氧化的作用。从以上可知,只要VC充足,则VC、谷胱甘肽、-SH形成有力的抗氧化组合拳,清除自由基,阻止脂类过氧化及某些化学物质的毒害作用,保护肝脏的解毒能力和细胞的正常代谢。 9.提高人体的免疫力。白细胞含有丰富的VC,当机体感染时白细胞内的VC急剧减少。VC可增强中性粒细胞的趋化性和变形能力,提高杀菌能力。促进淋巴母细胞的生成,提高机体对外来和恶变细胞的识别和杀灭。参与免疫球蛋白的合成。提高CI补体酯酶活性,增加补体CI的产生。促进干扰素的产生,干扰病毒mRNA的转录,抑制病毒的增生。 10.提高机体的应急能力。人体受到异常的刺激,如剧痛、寒冷、缺氧、精神强刺激,会引发抵御异常刺激的紧张状态。该状态伴有一系列身体,包括交感神经兴奋、肾上腺髓质和皮质激素分泌增多。
二、实验设计思路:
碘标准溶液的配制和标定——制备果蔬组织提取液试样预处理 ——样品测定——实验数据处理及分析
三、实验原理
维生素C的结构:
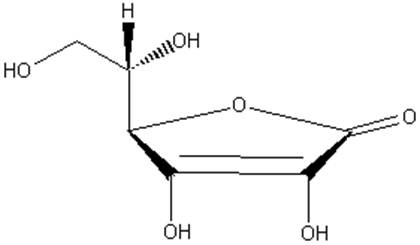
维生素C纯品为白色无臭结晶,熔点在190—192℃,易溶于水,微溶于丙酮,在乙醇中溶解度更低,不溶于油剂。结晶抗坏血酸在空气中稳定,但它在水溶液中易被空气和其他氧化剂氧化,生成脱氢抗坏血酸;在碱性条件下易分解,见光加速分解;在弱酸条件中较稳定。维生素C(C6H8O6)分子结构中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,抗坏血酸分子中的二烯醇基被I2完全氧化后,则I2与淀粉指示剂作用而使溶液变蓝,所以当滴定到溶液出现蓝色时即为终点。由于维生素C的还原性很强,即使在弱酸性条件下,上述反应也进行得相当完全。维生素C在空气中极易被氧化,尤其在碱性介质中更甚,故该滴定反应在稀HAc中进行,以减少维生素C的副反应。此实验使用淀粉作为指示剂,用直接碘量法测定水果中维生素C的含量。I2标准溶液采用间接配制法获得,用Na2S2O3标准溶液标定,样品中加入稀醋酸后,溶液pH控制在3-5范围内方可用碘标准溶液进行滴定。pH值过高或过低都能使其内酯环水解,使其含量下降维生素C的测定受溶液pH值影响较大。pH值太高,空气中氧能与维生素C发生氧化还原反应;pH值太低,溶液中一些强还原性物质能与维生素C作用,这些都使测定结果偏低,并且精密度不高。实验结果表明,溶液pH值以保持在3-5为宜。在实际测定中,用冰醋酸作介质可控制溶液pH值在4左右。
四、实验相关理论计算:
1、Na2S2O3 溶液的标定:
Cr2O72-+6I–+14H+ =2Cr3++3I2+7H2O
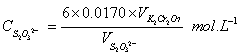
2、碘标准溶液的标定:
2S2O32-+I2 = S4O62-+2I-
C I2=(CV)S2O32-/2V I2
3、为减小仪器误差要求滴定碘标准溶液的体积在20mL则:
m样/M×34%=(CV)碘 但受到条件限制(研钵大小)只能每次称样约为50—90g左右
4、实验结果计算:
W(vc)=m(vc)/m样=[(cv)碘M(vc)]/m样×100%
五、实验主要试剂:
新鲜的柠檬270克左右
容量瓶(250mL)、酸式滴定管(50mL)、锥形瓶、量筒、玻璃棒,尼龙纱布、电子天平、多功能食物粉碎机、漏斗、烧杯、移液管、吸耳球、PH试纸。
0.05mol/L碘溶液、2mol/L醋酸、可溶性淀粉溶液(质量分数为0.02%)、蒸馏水、Na2S2O3溶液、K2Cr2O7 标准溶液
六、实验步骤:
1、标准溶液的标定
1、Na2S2O3 溶液的标定
用移液管吸取25.00mlK2Cr2O7 标准溶液于250ml 锥形瓶中,加5ml 6 mol·L-1 HCl,加10ml 100g/L KI溶液,摇匀后盖上表面皿,在暗处放5分钟后,加100ml水稀释,立即以用待标定的Na2S2O3溶液滴定至浅黄绿色,再加入2ml淀粉溶液, 继续滴至溶液蓝色消失变为绿色即为终点,平行测三次。
2、I2溶液的标定
用酸式滴定管放出25.00ml待标定的I2溶液于250ml 锥形瓶中,加50ml水,用Na2S2O3标准溶液滴定至浅黄色,加入2ml淀粉指示剂, 继续用Na2S2O3标准溶液滴定至溶液蓝色恰好消失即为终点.平行测定3次。
3、Vc含量的测定
立即用I2标准溶液滴定至溶液恰呈蓝色,30秒内稳定不褪色,即为终点,平行测定三次,计算柠檬中维C的含量和相对平均偏差。
2、试样的处理
分别称取三份50—90g柠檬,加入50ml稀醋酸,榨成汁在漏斗中垫上尼龙纱布,将粉碎后的柠檬液及残渣放到锥形瓶中,向锥形瓶中加入2mL淀粉溶液,然后滴加盐酸或醋酸,将pH调至3左右。
3、测定
在滤液中加入2ml淀粉溶液,用I2标准溶液滴定至呈现稳定的蓝色,记录所用标准溶液的体积。平行测三次。
七、实验数据处理及分析:
1、Na2S2O3 溶液的标定
C K2Cr2O7=0.0170 mol/L V K2Cr2O7=25.00ml

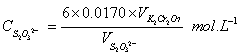
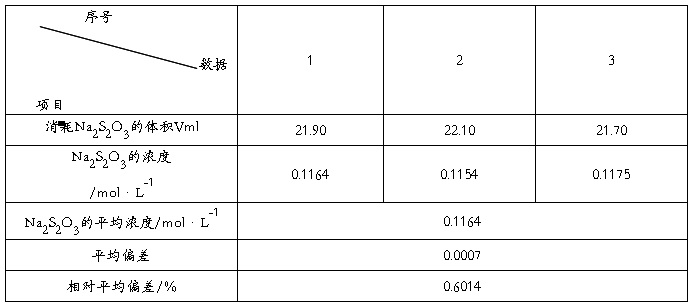
2、I2溶液的标定
V Na2S2O3=2.00 ml C I2=(CV)S2O32-/2V I2
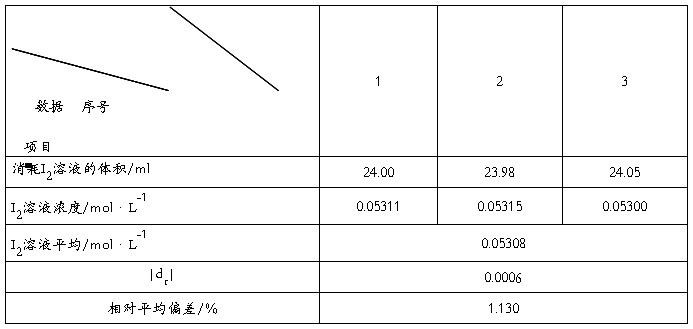
3、 柠檬中Vc含量的滴定
MVC=176.12g/mol
W(vc)=(m(vc)/m样)×100%=([(cv)碘M(vc)]/ m样)×100%

八、实验参考文献:
1、孙培龙 吴石金,《生物化学技术实验指导》,2008,化学工业出版社
2、分析化学实验第三版高等教育出版社
3、分析化学实验——华东化工学院出版社(张济新等编写)
4、分析化学实验——武汉大学出版
5、生物科学——袁玉松,朱婉华,陈均辉
6、维生素C——百度文库
7、基础化学实验(上)——徐家宁,张寒琦,张锁秦
九、设计实验总结:
通过实验自己学会里从哪些方面去分析和设计一个实验,以及实验中应考虑哪些因素,反应条件及相关计算等。
此次实验中我们也发现了一些不足之处,比如样品处理过程中受条件的限制使得一些样品流失和在过滤汁液是由于维生素C的还原性很强,受空气中氧的影响很大,直接碘量法使得溶液与空气接触时间增长,以及某些不溶物对维生素C有吸附作用等都造成测定结果偏低。
实验的成功使我们掌握了自主设计实验的能力,在以后的学习和生活中给了我们很大的鼓舞,不管做任何事,只要相信自己,只要愿意做,认真做,就会有成功的一天!
第二篇:仪器分析实验报告
实验一 自动电位滴定法-氢氧化钠滴定磷酸
专业 班级 姓名 学号
一、实验目的:
1、掌握酸度计,磁力搅拌器或电位滴定仪的使用方法。
2、掌握电位法确定滴定终点的方法。
3、掌握自动电位滴定的方法。
二、实验原理:
NaOH + H3PO4 → NaH2PO4 + H2O
NaOH + NaH2PO4 → Na2HPO4 + H2O
三、实验内容:
四、数据记录:
C(NaOH)= mol.l-1 V(H3PO4)= ml

五、数据处理:(于前表中计算)
1、滴定终点的电动势
PHsp1= ,PHsp2= 。
2、自动滴定

六、问题及讨论:
实验二 荧光分析法——
核黄素(VB2)含量的测定
专业班级 姓名 同组人 学号
一、实验目的:
1、掌握荧光分析仪(分光光度计)的使用方法。
2、掌握荧光物质定量分析的方法。
二、实验原理:
三、实验内容:、
四、数据记录:
最大激发波长 nm , 滤光片波长 。
最大发射波长 nm , 滤光片波长 。
核黄素(VB2)标准液10ug/ml, 空白 蒸馏水 。

五、数据处理:
1、标准曲线;
2、样品中核黄素的含量= (ug/l)。
六、问题及讨论:
实验三 库仑分析法—库仑滴定
维生素C片中Vc的含量测定
专业班级 姓名 同组人 学号
一、实验目的:
1、掌握库仑分析仪的使用方法。
2、掌握库仑滴定的方法。
二、实验原理:
三、实验内容:、
四、数据记录及数据处理:
Vc片的质量 克,配制成 毫升,取 毫升。
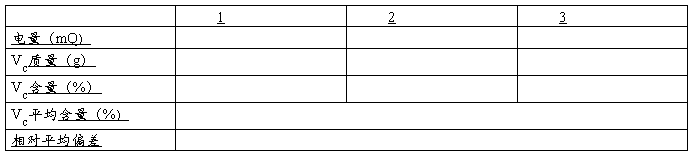
五、问题及讨论:
实验四 离子选择电极分析法——
氟离子含量的测定
专业班级 姓名 同组人 学号
一、实验目的:
1、掌握氟离子选择电极的使用方法。
2、掌握离子选择电极分析法的方法。
二、实验原理:
三、实验内容:、
四、数据记录:
未知样体积: 10.00 毫升,TISAB 10 毫升,配制总体积 毫升。
自来水体积: 50.00 毫升,TISAB 10 毫升,配制总体积 毫升。
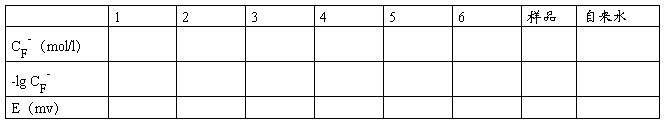
五、及数据处理:
1、标准曲线;
2、样品中氟的含量= mg/l ,
自来水中氟的含量= mg/l 。
六、问题及讨论:
实验五 气相色谱分析法
专业班级 姓名 同组人 学号
一、实验目的:
1、掌握气相色谱仪的使用方法。
2、掌握气相色谱的分离、定性、定量方法。
二、实验原理:
三、实验内容:、
四、数据记录及数据处理:
气化室温度: ℃,色谱柱温度: ℃,检测器温度: ℃。
载气: ,流量: ml/min 。
标准样时间;苯 min ,甲苯 min 。

五、问题及讨论:
-
维生素C的测定实验报告
附1学生实验报告格式浙江万里学院实验报告课程名称生化实验指导教师谭志文汪财生实验项目维生素C的定量测定26二氯酚靛酚法专业班级生物…
-
实验六 维生素C的定量测定
姓名:**年级专业:2012级生物科学同组者:**学号:***实验六维生素C的定量测定(2,6-二氯酚靛酚滴定法)一、实验目的掌握…
-
维生素C的定量测定实验报告
生物化学实验报告维生素C的定量测定26二氯酚靛酚滴定法一实验目的掌握26二氯酚靛酚滴定法测定维生素C的原理和方法二实验原理维生素C…
-
实验三 维生素C的定量测定
实验三维生素C的定量测定一研究背景维生素C的主要作用是提高免疫力预防癌症心脏病中风保护牙齿和牙龈等另外坚持按时服用维生素C还可以使…
-
化学实验报告 实验__直接碘量法测定维生素C的含量
实验报告姓名班级同组人自评成绩项目直接碘量法测定维生素C的含量课程学号一实验目的1熟悉直接碘量法的操作步骤及注意事项2了解维生素C…
-
紫外光度法测定维生素C实验报告
紫外分光光度法测定维生素C片维生素C的含量一实验目的1学习利用紫外吸收光谱测定物质含量的原理和方法2熟练紫外可见分光光度计的操作二…
-
维生素C的测定实验报告
附1学生实验报告格式浙江万里学院实验报告课程名称生化实验指导教师谭志文汪财生实验项目维生素C的定量测定26二氯酚靛酚法专业班级生物…
-
化学实验报告 实验__直接碘量法测定维生素C的含量
实验报告姓名班级同组人自评成绩项目直接碘量法测定维生素C的含量课程学号一实验目的1熟悉直接碘量法的操作步骤及注意事项2了解维生素C…
-
实验六 维生素C的定量测定
姓名:**年级专业:2012级生物科学同组者:**学号:***实验六维生素C的定量测定(2,6-二氯酚靛酚滴定法)一、实验目的掌握…
-
维生素C的定量测定实验报告
生物化学实验报告维生素C的定量测定26二氯酚靛酚滴定法一实验目的掌握26二氯酚靛酚滴定法测定维生素C的原理和方法二实验原理维生素C…
-
实验报告2荧光分光光度法测定维生素B2的含量
实验项目荧光分光光度法测定维生素B2的含量实验题目荧光分光光度法测定维生素B2的含量实验目的1掌握标准曲线法定量分析维生素B2的基…