乙酸正丁酯
乙酸正丁酯制备
班级:11化学 yinshou
一、实验目的:
(1)初步了解和掌握化工产品开发的研究思路和实验研究方法。 (2)学会组织全流程实验,并获得高纯度的产品。 (3)学会分析实验流程及实验结果,提出实验改进方案。
二、实验原理:
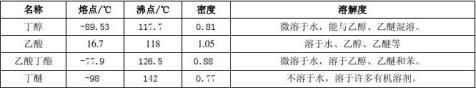
反应:
副反应:
CH3COOH + CH3CH2CH2CH2

3COOCH2CH2CH2CH3 + H2O
CH3CH2CH
2CH23CH2CH=CH + H2O
2CH3CH2CH2CH2

3CH2CH2CH2OCH2CH2CH2CH3 + H2O

为了促使反应向右进行,通常采用增加酸或醇的浓度或连续地移去产物(酯和水)的方式来达到的。在实验过程中二者兼用。至于是用过量的醇还是用过量的酸,取决于原料来源的难易和操作上是否方便等诸因素。提高温度可以加快反应速度。
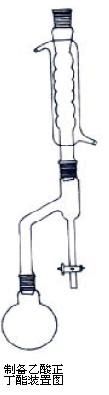
三、实验装置图:
四、物理常数:
五、实验步骤:
(1)加料。在干燥的圆底烧瓶中加入35mL正丁醇、22mL冰醋酸及10滴浓硫酸,摇匀后,加入几粒沸石,再安装好分水器(先从分水器上端小心加水至分水器支管处,然后再放去9~10mL的水,再安装上去),回流冷凝管。
(2)加热回流至分水器中水位不再上升为止(当水充满时,可以由活塞放出)。蒸汽回流的
高度:超过冷凝管进水口高度2~3cm即可。
(3)冷却(不可以拆卸回流冷凝管)后。将烧瓶中的混合物与分水器中的酯层合并,转入分液漏斗中。
(4)依次用10mL水,10mL10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥。
(5)重蒸(略)。
六、操作过程:
1、回流分水反应装置,及时分出反应生成的水,缩短了整个实验时间。本实验体系中有正丁醇—水共沸物,共沸点93℃;乙酸正丁酯—水共拂物,共沸点90.7℃,在反应进行的不同阶段,利用不同的共沸物可把水带出体系,经冷凝分出水后,醇、酯再回到反应体系。为了使醇能及时回到反应体系中参加反应,在反应开始前,在分水器中应先加入计量过的水,使水面稍低于分水器回流支管的下沿,当有回流冷凝液时,水面上仅有很浅一层油层存在。在操作过程中,不断放出生成的水,保持油层厚度不变。或在在分水器中预先加水至支口,放出反应所生成理论量的水(用小量筒量)。
2、洗涤操作(分液漏斗的使用):
(1)洗涤前首先检查分液漏斗旋塞的严密性。
(2)洗涤时要做到充分轻振荡,切忌用力过猛,振荡时间过长,否则将形成乳浊液,难以分层,给分离带来困难。一旦形成乳浊液,可加入少量食盐等电解质或水,使之分层。
(3)振荡后,注意及时打开旋塞,放出气体,以使内外压力平衡。放气时要使分液漏斗的尾管朝上,切忌尾管朝人。
(4)振荡结束后,静置分层;分离液层时,下层经旋塞放出,上层从上口倒出。
3、蒸馏,所用的仪器是干燥的,使乙酸正丁酯充分干燥,从而提高产品质量。
七、注意事项:
1、冰醋酸在低温时凝结成冰状固体(熔点16.6℃)。取用时可温水浴加热使其熔化后量取。注意不要触及皮肤,防止烫伤。
2、在加入反应物之前,仪器必须干燥。
3、浓硫酸起催化剂作用,只需少量即可。也可用固体超强酸作催化剂。
4、本实验中不能用无水氯化钙为干燥剂,因为它与产品能形成络合物而影响产率。
八、参考文献:
1, 乙酸正丁酯合成实验的改进.何节玉,聊城大学学报,第16卷第三期,2003,9. 2, 探索合成乙酸正丁酯的最佳条件. 范永军,化学教学,2007,第5期。
3, 有机合成(下),王宝仁,[m] 中国科学出版社 1985
新催化剂研究
乙酸正丁酯的传统方法用浓硫酸做催化剂,虽然价格低廉、催化活性高,但存在诸如设备易腐蚀,副反应多,产品难分离提纯,含有大量酸性废液,易造成环境污染等。 近年来, 有关杂多酸在酯类合成中的应用已有报道, 它比传统的浓硫酸具有更高的催化活性、选择性好、对设备腐蚀小、对环境无污染等特点。探讨了以磷钼钒杂多酸作催化剂合成乙酸正丁酯的反应, 在催化剂的种类及用量、应时间、反应温度、原料配比等方面进行了研究, 取得了较好的效果。
( 1) 以磷钼钒杂多酸为催化剂催化合成乙酸正丁酯的最佳条件是: 醇酸物质的 量比 1 2B1 催化剂用量为反应液总量的 0 . 6% , 反应时间 85 m in 反应温度为 115e , 乙酸正丁酯的收率为 93% ~ 95 % , 其中, H 5 PM o10 V 2O 40 # H2 O ( V2 ) 的催化活性最高, 酯化率达 95 .6% 。
( 2) 利用磷钼钒杂多酸催化合成乙酸正丁酯的活性高、催化剂用量小、反应条件温和、操作简便, 是酯化反应的理想催化剂。与硫酸相比, 不仅减少三废污染和不腐蚀设备, 而且, 工艺简单, 能降低产品色泽, 催化剂可重复使用, 具有很好的工业化前景。
参考文献:
[1] 磷钼钒杂多酸催化合成乙酸正丁酯的研究 .尹彦冰.化工时刊,第23卷11期
[2]金振兴, 张庆勋. 固体杂多酸催化剂 PW 12 /S i O 2 的制备及对酯 化 合 成 乳 酸 正 丁 酯 的 研 究 [ J]. 化 学 世 界, 1996, 37( 3): 128~ 131
第二篇:固体酸催化酯化合成醋酸丁酯
实验报告
课程名称: 专业实验 指导老师: 成绩:__________________
实验名称: 固体酸催化酯化合成醋酸丁酯 实验类型: 有机合成 同组学生姓名:
一、实验目的和要求(必填) 二、实验内容和原理(必填)
三、主要仪器设备(必填) 四、操作方法和实验步骤
五、实验数据记录和处理 六、实验结果与分析(必填)
七、讨论、心得
一、实验目的
了解与掌握固体酸催化酯化工艺特点。
二、实验原理
有机酸与醇进行酯化反应,是常见的化工过程之一,也是一个典型的酸催化的可逆反应,其反应通式如下:
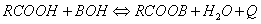
并具有下列关系式(1):
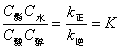
式中:C-物质浓度,k-反应速度常数,K-平衡常数。
为使反应加速常加入少量催化剂。工业上是加浓硫酸或通干燥氯化氢为催化剂。本实验采用固体酸催化剂。
固体酸酯化合成工艺,采用阳离子交换树脂或分子筛固体酸催化剂代替硫酸液体催化剂合成乙酸正丁酯,不仅可以克服因硫酸存在下的容器腐蚀和发生副反应的严重缺点,同时固体酸催化剂来源容易、用量少、能反复使用,催化剂与产品分离容易,便于连续生产,而且产物乙酸正丁酯纯度高的特点。
酯化与水解是可逆的化学平衡。从工业生产角度来看,采用一些简单的措施就可使转化率接近100%,主要的方法是蒸出水或酯。在乙酸正丁酯的合成中,利用水和醇、酯能形成共沸的特点将所生成的水蒸出,带出的酯及醇用分水器分离后返回反应釜,直至反应完全。再精馏后,酯则留在反应釜中。
选用合适的酯化催化剂及其用量在保证酯化反应顺利进行方面有决定性作用。本实验用强酸性阳离子交换树脂,这类离子交换树脂均含有可被阳离子交换的氢质子,属强酸性,有很好的催化活性,即在此酸中心上可进行酸催化酯化反应。
三、实验装置及试剂
1.试剂
乙酸(CH3COOH)沸点118℃,分子量60.05,比重约1.05
正丁醇(C4H9OH)沸点117.8℃,分子量74.12,比重0.81
催化剂阳离子交换树脂用牌号D72型
2.实验装置
如图1所示。
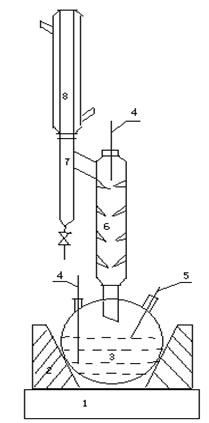
1-磁力搅拌器 2-电加热套 3-三口瓶 4-温度计
5-取样针筒 6-分馏柱 7-分水器 8-回流冷凝管
图1 实验装置示意图
四、实验步骤
1.取20mL醋酸,倒入已知重量的三口瓶(含磁子)内,称出总重,得到醋酸质量。根据醋酸质量按摩尔比1:1算出应加入的正丁醇的体积,量入正丁醇并称重。然后加入1g催化剂。
2.按图连接好装置,然后开冷却水,电加热套和搅拌器。
3.升温并保温,将反应加热至沸,釜液126℃,分馏柱110℃左右。
4.此时蒸出由乙酸丁酯、水和正丁醇组成的共沸混合物,经过分馏柱,收集于分水器中,上层为乙酸丁酯和正丁醇,返回反应釜中。
5.待分水器中水不再增加时,则可以认为酯化过程已终止,关电源和冷却水。
6.待反应釜内温度降至80℃以下时,先放出分水器中的水称重。再把分水器中油层返回反应釜,称重。
7.取釜内样2mL,与0.5mL异丙醇混合均匀,气相色谱中进样0.2μL进行组成分析。
五、实验数据记录及处理
1.原始实验数据记录

2.从原始数据得到以下有用数据:

3.色谱分析
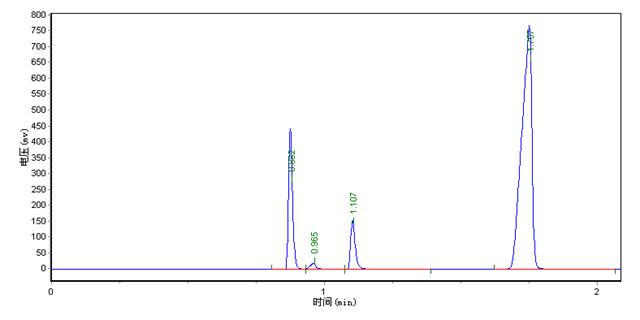
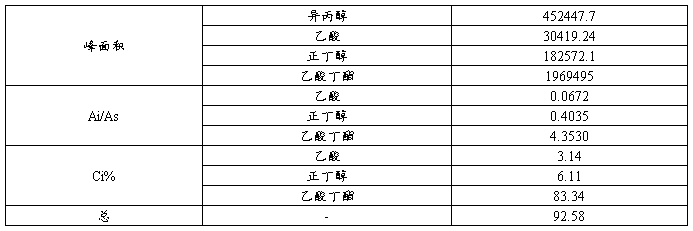
4.进行物料衡算,求损失
反应前: M=19.743+25.268 g =45.011 g
反应后: M’=35.307+5.087 g =40.394 g
则损失率为 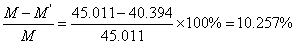
5.计算终点转化率
乙酸: 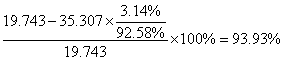
正丁醇: 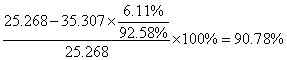
六、实验结果及分析
1.实验中用19.743克乙酸与25.268克正丁醇反应,生成了35.307克产品和5.087克水,损失率达到了10.257%,超过了正常的损失率。这是由于操作时发生失误,分水器没有关紧,反应开始后有一部分液体流出了分水器,对实验结果造成了一定影响。
2.酯化和水解是可逆的化学平衡,反应物的转化率不可能达到100%,本实验中采用蒸出产物水的方法提高了反应物的转化率,乙醇和正丁醇的转化率分别达到了93.93%和90.78%。理论上采用蒸出水的方法能使转化率接近100%,本实验中若增加反应时间能使转化率进一步提高。
3.在色谱分析图谱中,第一个峰是内标物异丙醇,后面依次是乙酸、正丁醇和乙酸丁酯。在进行色谱分析操作时,要熟悉步骤和要点,注射样品速度要快,否则谱峰的形状会改变,结果发生偏差。
七、讨论
本工艺采用间歇式反应,反应设备简单、灵活,在工业上适合小批量的生产。在工艺参数中,本反应对温度控制较为容易,只要溶液沸腾即可,若升高加热套的温度,能使反应速度加快。本工艺采用蒸馏的方法,能很好地分离产物和水,在提高转化率的同时,得到了较为纯净的产品。选用合适的催化剂机器用量在保证酯化反应顺利进行方面有决定性作用,本工艺采用强酸性离子交换树脂,这类树脂含有可被阳离子交换的氢离子,呈强酸性,有很好的催化活性;同时,采用固体酸催化剂能克服因硫酸存在下的容器腐蚀和发生副反应的严重缺点,而且催化剂来源容易,用量少,能反复利用,易于产品分离,便于连续生产,产物纯度高,因此固体酸催化剂有很大的优势。
-
中职教师个人总结
20xx--20xx学年第一学期教师个人总结这学年来,本人在教育教学工作中,始终坚持党的教育方针,面向全体学生,教书育人,为人师表…
-
教师思想作风工作总结
教师职业道德的好坏直接管械着教师的工作态度、教学成绩,关系着学校的声誉,为使我校每个教师有较高的思想道德品质,努力搞好各项工作,本…
-
公寓管理委员会总结 (2)
宿管会20xx---20xx年学期工作总结尊敬的领导、亲爱的伙伴们:大家下午好!在这一年来,公寓管理委员会日常工作总体上安全、平稳…
-
化学教育专业大学生实习总结
一、实习的目的与要求安排教学实习的基本目的,在于通过理论与实际的结合、学校与社会的沟通,进一步提高学生的思想觉悟,尤其是观察、分析…
-
银行工作人员年度工作总结
本人于200x年*月有幸成为建行这个温暖大家庭中的一员,在入职的四个月以来,我被分到**支行实习锻炼。在此锻炼期间,我能积极参加分…