关于仁怀市育英实验学校基层工会换届选举的报告
关于仁怀市育英实验学校基层工会换届选举的报告
仁怀市教育工会:
一、根据《中国工会章程》“关于基层工会换届选举”文件的精神,我校定于20##年10月26日召开第4届教职工代表大会,并选举出新一届工会主席和委员会委员。
二、第4届工会委员由5人组成,其中工会主席1人,组织委员1人,宣传委员1人,劳动财务委员1人,女工文体委员1人。
三、附第4届工会委员会委员名单:
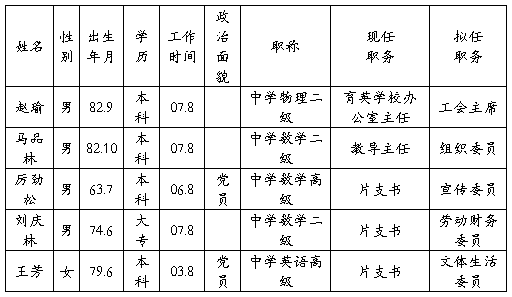
特此报告,请予批复!
中共仁怀市育英实验学校支部委员会
二〇##年十月二十六日
关于黄马中心小学工会换届选举的批复
黄马中心小学教育工会:
报来《关于黄马中心小学新一届工会组成人员报批的报告》悉,经研究,同意你校新一届工会委员会由王志学、王良梅、万细辉、吴秋根、胡永红等五位同志组成,王志学同志任主席,王良梅同志任女工文体委员,万细辉同志任宣传委员,吴秋根同志任组织委员,胡永红同志任劳动财务委员。特此批复!
南昌县教育工会
20##年11月21日
黄马中心小学第十届教育工会选举结果
报 告
南昌县教育工会:
经我校第十届一次教代会选举通过,王志学、王良梅、万细辉、吴秋根、胡永红等五位同志被正式选举为黄马中心小学第十届教育工会委员会委员,王志学同志任工会主席,王良梅同志任女工文体委员,万细辉同志任宣传委员,吴秋根同志任组织委员,胡永红同志任劳动财务委员。
特此报告,请予批复!
中共黄马中心小学总支委员会
二〇##年十一月十日
第二篇:温州育英国际实验学校
温州育英国际实验学校
09-10学年上期第一次月考高二(文)化学试卷
可能用到的相对原子质量:K~39,C~12,N~14,O~16, Na~23, I~127,Cl~35.5,S~32
一、选择题(本大题包括35个小题,每小题2分,共70分。每小题只有一个选项符合题意)
1、有些垃圾可以用卫生填埋、焚烧、堆肥的方法处理。下列垃圾中,不适合用这样的方法处理的是
A.农用塑料薄膜 B.废旧电池 C. 卫生纸 D. 纯棉纺织品
2、室内空气污染的主要来源之一是泡沫绝缘塑料、化纤地毯、书报、油漆等不同程度释放出的气体,该气体是
A.甲烷 B.甲醛 C.一氧化碳 D.二氧化碳
3、O3和O2是 ( )
A.同分异构体 B.同种物质 C.氧的同素异形体 D.氧的同位素
4、科技文献中经常出现的下列词汇,其中与相关物质的颜色并无联系的是( )
A.赤色海潮 B.棕色烟气 C.白色污染 D.绿色食品
5、下列各组名词或现象中,三者间没有逐级因果关系的是 ( )
A.汽车尾气-------光化学污染-------咳嗽和气喘者增多
B.含磷洗衣粉--------水体富营养化--------水栖生物大量死亡
C.人口增多--------空气中CO2浓度增大--------温室效应
D.氟氯烃--------臭氧空洞--------皮肤癌患者增多
6、我国城市环境中的大气污染物主要是( )
A. O2、Cl2、HCl 、酸雨 B. SO2、NO2、CO、烟尘
C. Cl2、CO、CO2、雾 D. HCl、SO2、N2、粉尘
7、我国三峡工程所提供的清洁、廉价、强劲、可再生能源——水电,相当于每年燃烧3000万吨原煤的火力发电厂产生的电能,三峡工程有助于控制 ( )
①温室效应 ②形成酸雨 ③空气中的固体颗粒浓度 ④白色污染
A.只有① B.只有①② C.②③④ D.①②③
8、下列物质中既能与稀盐酸反应,又能与NaOH反应的是( )
A、丙氨酸 B、纤维素 C、糖类 D、汽油
9、农业上用的杀菌剂波尔多液(由硫酸铜和生石灰制成) ,它能防治植物病毒的原因是: ( )
A、硫酸铜使菌体蛋白质盐析
B、石灰乳使菌体蛋白质水解
C、菌体蛋白质溶解于波尔多液
D、铜离子和石灰乳使菌体蛋白质变性。
10、对于淀粉和纤维素的下列叙述正确的是( )
A、互为同分异构体 B、化学性质相同
C、碳氢氧元素的质量比相同 D、属于同系物
11、某工厂排放的酸性废水中含有较多的Cu2+,对农作物和人畜都有害,欲采用化学法除去有害成分,最好是加入下列物质中的( )
A.食盐、硫酸 B.胆矾、石灰水 C.铁粉、生石灰 D.苏打、盐酸
D、向反应后的试管中先用碱液中和后再加入银氨溶液,稍热后试管壁有银镜出现。
12、“84消毒液”在日常生活中被广泛使用,该消毒液无色,PH大于7,对某些有色物质有漂白作用。你认为它的有效成分是( )
A、二氧化硫 B、次氯酸钠 C、高锰酸钾 D、碳酸钠
13、下列物质中,可以作为食品防腐剂的是( )
A、苯甲酸钠 B、L—谷氨酸钠 C、碳酸氢钠 D、乳酸
14、含铝抗酸药容易引起便秘,最好与下列哪种物质共同服用以降低或抵消其副作用( )
A、三硅酸镁 B、氢氧化镁 C、碳酸氢钠 D、碳酸镁
15、.硬水和软水的本质区别是( )
A.硬水浑浊、软水澄清
B.硬水含有杂质、软水含杂质少
C.硬水是不纯净水,软水是纯净水
D.硬水含有较多可溶性钙镁化合物、软水不含或含少量可溶性钙镁化合物
16、大量服用阿司匹林会导致( )
A.便秘 B.胃溃疡、胃出血
C.腹泻 D.食欲不振、缺乏抵抗力
17.人们常用空气污染指数API(Air Pollution Index)来表示空气的质量。某地区各种污染指数分别为:二氧化硫95,二氧化氮48,可吸入颗粒物55。则该地区的空气污染指数为
A.48 B.55 C.95 D.198
18.如果人体摄入的油脂中饱和酯太多,就容易发胖,可能引发高血压、高血脂等疾病。下列油脂中饱和酯含量最高的是
A.豆油 B.花生油 C.芝麻油 D.牛油
19.分类收集生活垃圾,针对各种垃圾不同的特点进行科学处理,既能节约资源,又能防止污染。下列标志不属于垃圾分类收集标志的是
20.下列药品中,属于热镇痛药的是
A.碳酸氢钠片 B.诺氟沙星 C.阿莫西林 D.阿司匹林
29.如果将人体比成一座大厦,那么元素就是构成这座大厦的基石。在人体所含的各种元素中,对人体机能尤其是脑机能的运行起着十分重要作用,被公认为“智慧元素”的是
A.铁 B.铜 C.碘 D.磷
21.动物实验表明,对苯二胺和某些芳香胺类化合物有一定的致癌作用。通常含有苯二胺或其衍生物的是
A.合成染发剂 B.无机染发剂 C.植物染发剂 D.以上三类染发剂均有
22.下列做法合理的是
A.为了使食品较长时间保持色香味和口感,可加放适量的苯甲酸钠
B.为了增加婴幼儿奶粉中的含氮量,可在奶粉中适当添加尿素或三聚氰胺
C.在肉制品加工中加大量的亚硝酸钠以保持肉类新鲜
D.在缺碘地区,人们需要用添加碘单质的食盐来补充碘元素
23.随着工业的发展,大气中CO2的浓度不断增加,温室效应日益严重。为控制大气中CO2含量的增长,下列措施不切实际的是
A.保护地球上的森林资源 B.增加城市绿地面积
C.禁止使用石油、煤碳等化石燃料 D.限制CO2气体的排放
24.日常生活中,常用明矾净化生活用水,明矾在净水过程中所起的作用是
A.消毒 B.沉降 C.软化 D.杀菌
25.有位同学上学时所带的饭盒是聚乙烯(PE)材质的,所有的文具盒是聚氯乙烯(PVC)材质的,PE和PVC都是重要的有机材料。这两种物质中均含有的元素是
A.C B.N C.O D.S
26.下列物质中,属于氧化物的是
A.O2 B.H2O C.HClO D.Cu(OH)2
27.下列物质间的转化过程,属于氧化反应的是
A.C→CO2 B.CuO→Cu C.CaO→CaCO3 D.HCl→NaCl
28.下列说法正确的是
A.天然油脂都是纯净物
B.淀粉和纤维素互为同分异构体
C.农药DDT能有效控制虫害,应大力推广使用
D.利用CO2制造全降解塑料符合绿色化学的要求
29.下列物质的名称及其对应的化学式均正确的是
A.金钢石——C B.纯碱——NaOH
C.硝酸铵——NH4NO3 D.硫酸铁——FeSO4
30.下列说法中,正确的是
A.在氧化还原反应中,金属单质只体现还原性,金属阳离子只体现氧化性
B.按金属活动性顺序,排在前面的金属一定可以把排在后面的金属从它们的盐溶液中置换出来
C.在元素周期表中,非金属元素呈现的最高化合价不超过该元素所在的族序数
D.根据元素周期律,元素的非金属性越强,其氧化物对应水化物的酸性也越强
31、下列说法正确的是
A.氧气的摩尔质量是32g
B. 1mol H2的体积为22.4L
C.等质量的O2和O3,所含原子数相等
D.0.5 molNa2SO4中,含有Na+数约为0.5NA
32、下列离子方程式书写正确的是
A.硫酸和氢氧化钡 Ba2++SO42-=BaSO4 ↓
B.醋酸和氢氧化钠 H++OH-=H2O
C.氯气和水 Cl2+H2O =2H++Cl-+ClO-
D.钠和水反应 2Na+2H2O= 2Na++2OH-+ H2 ↑
32、在强酸性溶液中能大量共存的无色离子组是
A.Na+、SO42-、NO3-、Cl- B.Na+、K+、Cl-、CO32-
C.K+、 Mg2+、 Cl-、 OH- D. Na+、Cu2+、Cl-、NO3-
33.市场上销售的“84”消毒液,其商品标签上有如下的叙述:①本品为无色溶液,呈碱性。②使用时加水稀释。③可对餐具、衣物进行消毒,可漂白浅色物质。根据以上描述,你认为该消毒液的有效成分是
A.SO2 B.Na2SO4 C.KMnO4 D.NaClO
34.关于阿司匹林在临床上的应用,下列说法正确的是
A.阿司匹林有解热镇痛的作用
B.服用阿司匹林后出现胃肠道反应是中毒的表现,应立即停药
C.服用阿司匹林中毒后应立即停药,并静脉滴注 NaHCO3溶液
D.阿司匹林有治疗癌症的作用
35、0.5L 1mol/L的FeCl3溶液与0.2L 1 mol/L的KCl溶液中,Cl-浓度比为
A.5∶2 B.1∶1 C.3∶1 D.1∶3
二、填空
36.请填写下列空白。
(1)在二氧化碳、二氧化硫、二氧化氮、氟氯烃中,能引起温室效应的气体是_______;能造成臭氧层空洞的物质有_______和二氧化氮;能造成酸雨的主要因素是____和二氧化硫含量的增加。
(2)某日空气中各种污染物的污染指数分别为:二氧化硫66,二氧化氮50,可吸入颗粒120。该地区的首要污染物是 。
37.高铁酸钾(K2FeO4)是新型、高效的水处理剂,其氧化性比氯气、臭氧等更强,遇水易变化,在水处理过程中高铁酸钾被还原为Fe3+。则
(1)高铁酸钾中铁元素的化合价为_______。
(2)高铁酸钾除能消毒、杀菌外,还能除去水中的悬浮颗粒的原因是________(用化学方程式表示)。
(3)请再写一种能除去水中悬浮颗粒的混凝剂的名称_______。
38、请解答下列问题。
(1)某品牌抗酸药的主要成分有糖衣、氢氧化镁、淀粉。试写出该抗酸药发挥功效时的离子方程式: 。
(2)甲状腺肿大俗称“大脖子病”,平常人们可通过食用 进行膳食调节而预防。
(3)胃酸可破坏人体常用的补铁剂的结构,将其中的铁元素以Fe2+的形式游离出来。
药物“速力菲”(琥珀酸亚铁薄膜衣片) 适用于明确原因的缺铁性贫血。其主要活性成分是琥珀酸亚铁(含Fe2+ 34.0%-36.0%的无水碱式盐,不溶于水也不溶于乙醇)。性状为薄膜衣片,除去薄膜衣后显暗黄色。使用时与维生素C同服有利于吸收等。
请回答下列问题:
①该药品的薄膜衣的作用是 。
②该药品与维生素C同服效果更好,这是因为维生素C具有 (填“氧化”或“还原”)性。
③探究速力菲中是否含有Fe2+的实验步骤如下:
a.取1颗速力菲,去薄膜衣,研成粉末状;
b.取研细后的粉末,溶于 中,配成浅绿色溶液;
c.取b所得的溶液少许,滴加 ,可以观察到溶液呈浅红色,再滴入氯水或双氧水,溶液迅速变成血红色。
④薄膜衣是一种淀粉制品,淀粉在人体内水解最终转化为 。
(4)邻羟基苯甲酸的结构式为  ,俗名水杨酸,是常用的解热镇痛药,由于它的酸性较强而刺激胃肠道,因此通常将它转化为阿司匹林,阿司匹林的结构为
,俗名水杨酸,是常用的解热镇痛药,由于它的酸性较强而刺激胃肠道,因此通常将它转化为阿司匹林,阿司匹林的结构为 。请回答:
。请回答:
①写出水杨酸的分子式: 。
②与阿司匹林相比,其钠盐或钙盐作为解热镇痛药的优点是 。
三.计算题(本题6分)(相对原子质量:Na、23 C:12 O:16 H:1)
39.(8分) 煤等化石燃料燃烧时产生的SO2会对大气造成污染。如果某火力发电厂每秒燃烧10 kg 煤,煤中硫元素的质量分数为1%。假设煤中的硫全部转化为SO2,试计算该发电厂每天产生的SO2的物质的量是多少?
40、(5分)9.5克碳酸钠和碳酸氢钠的混合物中加入100mL盐酸恰好反应,放出气体2.24L(标准状况)求(1)混合物中有碳酸钠多少克?
(2)盐酸的物质的量浓度是多少?
 温州育英国际实验学校
温州育英国际实验学校
09-10学年上期第一次月考
高二(文)化学答题卷
一、选择题

二、填空题:
36.(1)____ ___; ___ ___, ___ _。
(2) 。
37.(1)___ ____。
(2)_____ ___(用化学方程式表示)。
(3)___ ___。
38、(1) 。
(2)
(3)① 。② ③b. ;c. ,④ 。
(4)① 。② 。
三.计算题(本题13分)
39.(8分)
40、(5分)
答案

36.(1)二氧化碳 氟氯烃 二氧化氮
(2)可吸入颗粒
37.(1)+6
(2)Fe3+ + 3H2O 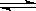 Fe(OH)3(胶体) + 3H+
Fe(OH)3(胶体) + 3H+
(3)明矾
38.(1)Mg(OH)2 + 2H+ = Mg2+ + 2H2O
(2)加碘盐(或海带等)
(3)①将琥珀酸亚铁与空气隔离,防止Fe2+被氧化
②还原
③稀盐酸 KSCN溶液
④葡萄糖
(4)①C7H6O3
②可以缓和对胃黏膜的刺激
39.解:n(SO2) = n(S) = 1000g/kg×10kg×1%×24×3600/32g/mol
=270000mol
答:该发电厂每天产生的SO2的物质的量为270000mol。
40、设Na2CO3和NaHCO3的物质的量分别为x、ymol
x+y=0.1 解得x=0.05mol
106x+84y=9.5 ……2分 y=0.05mol
… …1分
m(Na2CO3)=5.3g ……1分
n(HCl)=0.15mol ……1分 C(HCl)=1.5mol/L………1分
-
工会换届工作报告
围绕中心服务大局凝心聚力努力开创学校工会工作新局面各位代表、同志们:*****第二届工会于20xx年x月x日选举产生,任期五年,现…
-
三份工会换届工作报告
服务大局求实创新为加快我院发展步伐再立新功银川科技职业学院第二届工会会员代表大会工作报告20xx年月日各位代表同志们今天我们隆重召…
-
学校工会换届选举工作程序1
学校工会换届选举工作程序一、工作要点1.选举工会委员会和经费审查委员会一律采用无记名投票、候选人数多于应选人数的差额选举办法。2.…
-
学校工会换届选举结果的报告(参考文本)
学校工会换届选举结果的报告参考文本关于中小学工会第次会员大会选举结果的报告工会此处为上级工会名称我校工会第次会员大会于年月日召开大…
-
官庄湖学校工会换届选举工作实施方案
官庄湖学校工会换届选举工作实施方案官庄湖学校第一届工会代表于20xx年2月选举产生现已任期届满需进行换届改选根据工会法和中国工会章…
-
基层工会换届选举工作基本流程 (带样本)
基层工会换届选举工作基本流程基层工会换届选举工作基本流程基层工会按照《中华人民共和国工会法》和《中国工会章程》规定(三年或者五年)…
-
工会换届工作报告
围绕中心服务大局凝心聚力努力开创学校工会工作新局面各位代表、同志们:*****第二届工会于20xx年x月x日选举产生,任期五年,现…
-
基层工会换届选举报批、选举结果报告(样式)
关于举行××××工会换届选举的报告××××教育工会:××学校工会第×届委员会于××××年××月换届选举产生,至今将满×年。根据《中…
-
学校工会换届选举工作程序1
学校工会换届选举工作程序一、工作要点1.选举工会委员会和经费审查委员会一律采用无记名投票、候选人数多于应选人数的差额选举办法。2.…
-
三份工会换届工作报告
服务大局求实创新为加快我院发展步伐再立新功银川科技职业学院第二届工会会员代表大会工作报告20xx年月日各位代表同志们今天我们隆重召…
-
学校七届工会委员会换届总结
学校第七届工会委员会自20xx年x月开展工作以来,在上级工会的指导下,在学校党总支的正确指导和学校行政的大力支持下,我们认真履行工…