甲基橙的制备
一.实验目的
1. 通过甲基橙的制备学习重氮化反应和偶合反应的实验操作;
2. 巩固盐析和重结晶的原理和操作。
二.实验原理
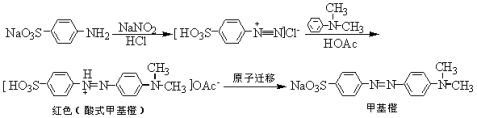
甲基橙是一种指示剂,它是由对氨基苯磺酸重氮盐与N,N-二甲基苯胺的醋酸盐,在弱酸性介质中偶合得到的。偶合首先得到的是嫩红色的酸式甲基橙,称为酸性黄,在碱中酸性黄转变为橙色的钠盐,即甲基橙。
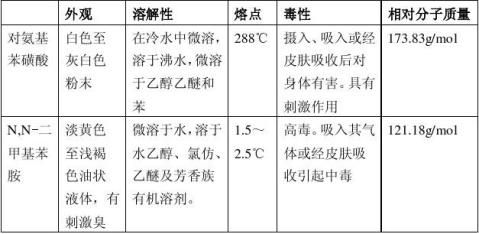
HO3S
NaOHNH2O3SNH3NaO3SNH2H2O
三.实验主要仪器及试剂
仪器:烧杯,布氏漏斗,吸滤瓶,干燥表面皿,滤纸 ,KI-淀粉试纸 。
试剂:对氨基苯磺酸 2.0g,亚硝酸钠 0.8g,5%氢氧化钠10 mL,N,N-二甲基苯胺
1.3 mL, 氯化钠溶液20ml,浓盐酸 2.5mL,冰醋酸 1 mL
,10%氢氧化钠15ml,乙醇4ml.
四.所用化学药品物理性质
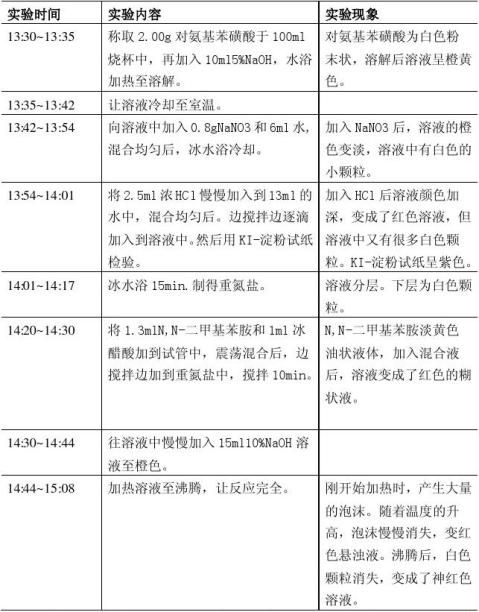
五.实验步骤及现象
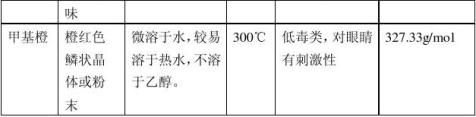
2
六.实验数据处理
已知对氨基苯磺酸的相对分子质量:M1=173.83g/mol;
甲基橙的相对分子质量:M2=327.33g/mol。则理论上2.00g的对氨基苯磺酸可得到甲基橙的质量:m1=(2.00g×M2)÷M1=(2.00g×327.33g/mol)÷173.83g/mol=3.77g;所以实验的产率:
ω=(实际上甲基橙的质量÷理论上甲基橙的质量)×100%
=(3.02g÷3.77g)×100%=80%
七.实验结果讨论
单从实验结果来看,该实验的产率比较高。但从实验的过程来说,却存在着不少的问题。
① 往溶液中加浓HCl时过快,导致溶液变的特别红。
② 偶合反应时,加热溶液至沸腾的过程中,加热速度太快,搅拌不及时,导致泡沫外溢,造成一部分的产品损失。
3

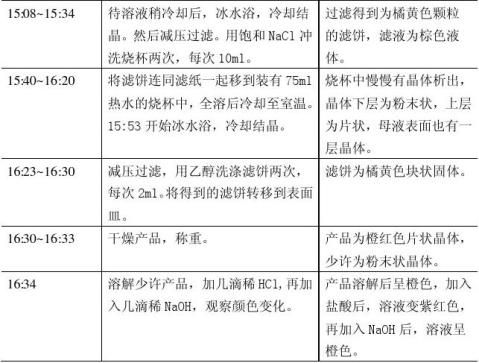
③ 最后重结晶时,冷却至室温的时间不够长,导致最后的产品呈粉末状。 ④ 冰水浴,冷却结晶,要等到溶液温度低于5℃才可以,所以过早的过滤会造成晶体数量的减少。
八.注意事项
① 对氨基苯磺酸为两性化合物,酸性强于碱性,它能与碱作用生成盐而不能与酸作用成盐。
② 重氮化过程中,应严格控制温度,反应温度若高于5℃,生成的重氮盐易与水解为酚,降低产率。
③ 若试纸不显色,需补充亚硝酸钠溶液。
④ 若反应物中含有未作用的N,N-二甲基苯胺醋酸盐,在加入NaOH后。就会有难溶于水的N,N-二甲基苯胺析出,影响产物的纯度。
⑤ 重结晶操作要迅速,否则由于产物呈碱性,在温度高是易变质,颜色变深。 ⑥ 用乙醇洗涤的目的是为了让产品迅速干燥。
4
第二篇:甲基橙的制备问题讨论参考答案
(1)什么叫偶联反应?试结合本实验讨论一下偶联反应的条件。
答:重氮盐在弱酸、中性或碱溶液中与芳胺或酚类作用由偶氮基-N=N-将两个分子偶联起来,生成偶氮化合物的反应,称为偶联反应。
重氮盐与芳胺偶联时,在高pH介质中,重氮盐易变成重氮酸盐,而在低pH介质中,游离芳胺则容易转为铵盐。只有溶液的pH某一范围内使两种反应物都有足够的浓度时,才能有效地发生偶联反应。胺的偶联反应,通常在中性或弱酸性介质(pH=4~7)中进行。
(2)在本实验中,制备重氮盐时为什么要把对氨基苯磺酸变成钠盐?本实验如改成下列操作步骤:先将对氨基苯磺酸与盐酸混合,再滴加亚硝酸钠溶液进行重氮化反应,可以这样做吗?为什么?
答:对氨基苯磺酸是两性化合物,以酸性内盐的形式存在,内盐的形成使对氨基苯磺酸在水中溶解度很小,故通常先将其制成钠盐,再进行重氮化反应。
由于对氨基苯磺酸在酸性条件下在水中溶解度很小,这样做反应较难进行(非均相反应)。
(3)试解释甲基橙在酸碱介质中的变色原因,并用反应式表示。
答:甲基橙在中性或碱性介质中呈黄色,pH=3~4.4。
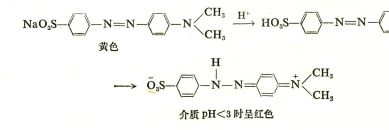
-
甲基橙的制备实验报告(4)沈杰
实验学专班姓指导日机化学实验报告名称院化学工程学院业化学工程与工艺级化工114班名沈杰学号114020xx417教师肖勋文何炎军期…
-
甲基橙的制备实验报告
实验学专班姓指导日机化学实验报告名称院化学工程学院业化学工程与工艺级化工xx班名xxx学号xxx教师期有一实验目的1通过甲基橙的制…
-
甲基橙的制备 有机化学实验报告
实验学专班姓指导日机化学实验报告名称甲基橙的制备业化学工程与工艺级名学号教师房江华李颖期有一实验目的1通过甲基橙的制备学习重氮化反…
- 甲基橙实验报告
-
甲基橙实验报告
有机化学实验报告实验名称学院专业班级姓名学号指导教师日期实验目的1通过甲基橙的制备学习重氮化反应和偶合反应的实验操作2巩固盐析和重…
-
输血科个人总结
履职评价输血科工作直接关系到患者生命安危,如何科学合理地利用血液资源及确保临床的用血安全尤其重要。几年来我院迅速发展,为配合临床工…
-
创建群众满意基层站所活动总结
卫生监督所“群众满意基层站所”创建活动总结创建“群众满意基层站所”活动是践行“三个代表”重要思想、维护人民群众利益的一项重要工作。…
-
放射科主任年终总结
一.加强科室管理科室不断完善标准化的操作规程,全体人员严格按照标准化操作,并有严格的奖惩制度。科室各种资料管理有条有序.资料完整。…
-
团支部工作总结
团队工作总结及来年工作重点XXXX年,××公司团总支在公司团委和党政的正确领导下,积极开展“三个教育”,以服务青年、服务企业为主线…
-
中医院20xx年治未病试点工作总结
根据国家中医药管理局《中医医院“治未病”科建设与管理指南(试行)》要求,我院在20xx年积极落实试点开展中医“治未病”工作任务,充…