开题报告文献综述
文献综述
摘要:通过控制水热反应参数制得氧化镍,对其进行测试确定适宜的水热生长条件,比较不同的生长条件对氧化镍形貌和性能的影响;选择其中电化学性能相对较好的氧化镍,与不同碳源(石墨烯、碳纳米管、生物碳荷叶、椰壳)进行复合,并研究比较制备样品的形貌和电化学性能,比较这些材料对于氧化镍的形貌改变,及电化学性能的改善作用,得到电容量高,循环循环性好的超级电容电极。
关键词:水热反应参数 氧化镍 碳纳米材料 活性炭 复合电极
1 引言
能源是人类生存和发展的重要物质基础[1]。能源存储是缓解能源问题的有效途径。随着科技和社会的迅速发展,对高性能电源的需求量越来越大。这些电源装置不仅高的比能量,而且还要有高的比功率。传统静电电容器尽管有大的比功率,但其比能量较小,因此不能满足实际要求。同时,如今电动汽车等对电源功率的要求逐渐提高,而当今电池却不能达到其要求。在此背景下,超级电容器因为具有传统电容器和电池所不具有的优点而得到了广泛的关注。作为一种新型储能装置,超级电容不仅为能源存储提供了新的思路,更在实际应用中起到了二次电池无法取代的地位。
1.1 超级电容简介
超级电容器又称超大容量电容器、电化学电容器或双电层电容器[2],属于普通电化学储能设备的范畴[3],是一种介于电池电池和传统电容器之间的新型储能器件[4]。常见的几种电源性能对比如图1.1所示[5]。

图1.1 各种储能装置的比能量和比功率的关系
1957年,Becker首先提出了可以将较小的电容器用作储能元件的专利,该专利具有接近电池的比能量[6]。1968年,美国标准石油公司(SOHIO)的Boos提出了利用高比表面积碳材料制作双电层电容器的专利[7],随后,该技术被转让给日本NEC公司,到80年代,日本NEC公司实现了产业化,推出了系列产品,并占据世界双电层电容器市场,从而引起了各国的广泛关注。
电化学电容器是电压存储、高功率电能存储设备。超级电容器不同于电池,在充放电时不发生化学反应,电能的储存或释放是通过静电场建立的物理过程来完成的,电极和电解液几乎不会老化,因此使用寿命长,并且可以实现快速充电和快速大电流放电。最重要的是,超级电容比传统电容储存电荷的能力高出近3~4个数量级。因此超级电容器可以像电池一样储存能量,并具有普通电容器充放电快、效率高、对环境无污染、循环寿命长、使用温度范围宽、安全性能高等特点。超级电容器、静电电容器和电池的性能比较如表1.2所列[8]。

表1.2 超级电容器、静电电容器和电池的性能比较
1.2 超级电容器分类
根据不同的标准,超级电容器可分为不同种类,大致有如下几种分类方法:
(1)按储能机理不同可分为双电层电容器、赝电容器和混合电容器。 双电层电容器是通过界面双电层储存电荷,赝电容器按法拉第赝电容的机理储存电荷,但各种实际电化学电容器的电容同时包含双电层电容和法拉第赝电容两个分量,只是在不同类型的电化学电容器中,这两种电容分量所占的比例不同而已;
(2)按所采用电极材料的不同可分为碳电极电容器、贵金属氧化物电极电容器和导电聚合物电容器。通常,用碳材料作电极时,主要是双电层电容,碳材料表面存在的官能基团只能产生少量的法拉第赝电容。因此一般认为碳电极电化学电容器是双电层电容器。金属氧化物、导电聚合物和其他材料电极电化学电容器的电容主要是法拉第赝电容,同时也有少量的双电层电容。因此一般认为它们是氧化还原电容器;
(3)按其正负极构成与电极上发生反应不同可分为①对称型电容器,两个电极的组成相同且电极反应相同,反应方向相反,如碳电极双电层电容器、贵金属氧化物电容器等;②非对称型电容器,两个电极的组成不同或反应不同,由n型和p型掺杂的导电聚合物作电极的电容器,能表现出更高的比能量和比功率;
(4)按所采用电介质的不同可分为水体系电介质电容器、有机体系电介质电容器、胶体电介质电容器和固体电介质电容器;
(5)按电容量的大小可分为小型(5F以下)、中型(5F~200F)和大型(200F以上)电容器。
1.3 超级电容器结构
目前,商业化生产的超级电容器种类很多,但大多数基于双电层结构。其基本结构主要由电极、电解液、隔膜、集流体和外壳组成,如图1.3.1,其中电极材料是超级电容器性能的最核心影响因素,外壳用于将超级电容器进行封装。

图1.3.1 超级电容器的基本结构
1.4 超级电容器原理
超级电容器通过电化学双电层电容和法拉第赝电容这两种储能机制来储存能量。
1.4.1 电化学双层电容(EDLC )
双电层电容器是利用电极/电解液界面双电层来存储能量的。在库伦力、分子间力、原子间力等各种作用力的共同作用下,固液界面出现稳定的、符号相反的双层电荷,由于界面上存在一个位垒,两层电荷都不能越过边界彼此中和,从而形成紧密的双电层,称为界面双层。双电层电容理论的第一个模型是由Helmholtz于1887年提出的,其原理图如图1.4.1所示,电极上的电位为φ0,由外部对该电容器充电时,一个电极的电位升高至φ0+φ1,而另一个电极的电位则降低至φ0-φ1,这样就储存了电荷。只要φ0+φ1的电位小于双电层的分解电压,便形成一个双电层电容器。在放电时,电子通过外电路上的负载从负极流到正极,使两电极上的电位恢复到φ0,而电解质中的正负离子则分别摆脱负极和正极表面的吸引,重新进入电解质内部[9]。

图1.4.1 双电层电容器原理图
(a)无外加电源 (b)有外加电源
1-双电层;2-电解液;3-电极;4-负载
双电层电容器单电极电容量可表达为
 (1)
(1)
式中:C为电容;ε为介电常数;S为电极板正对面积,即等效面积;d为电容器两极板之间的距离,即等效双电层厚度。
由于每一单元电容器有两个电极,可视为两个串联的电容器,故双电层电容器储存的电量Q与电极间的电压V和电容量之间有如下关系:
 (2)
(2)
电容器存储的能量为
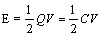 2 (3)
2 (3)
由上式可以看出,为了使双电层电容器存储更多电荷,要求极化电极具有尽可能大的可有效利用的比表面积,从而形成大面积的双电层,提高双电层电容器的性能。通过研究双电层的电极材料、电极组成和电解液提高电容器的电容量、降低等效串联电阻和漏电流,可改善双电层电容器的性能。
1.4.2 赝电容
基于赝电容的电容器是对双电层型电化学电容器的补充,它是在电极表面或体相中二维或准二维空间上,电极活性物质进行欠电位沉积,发生高度可逆化学吸附脱附或氧化还原反应,产生与电极充电电位有关的电容[10]。对于法拉第赝电容,其存储电荷的过程不仅包括双电层上的存储,而且包括电解液中离子在电极活性物质中由于氧化还原反应而将电荷储存于电极中。对于金属氧化物的化学吸脱附机理来说,一般过程为
MOx+yH+(OH)-+y(-)e-→MOx-y(OH)y (4)
电极在外加电场作用下,充电时电解液中的离子在外加电场的作用下由溶液中扩散到电极/溶液界面而后通过界面的电化学反应在电极上积累,电子流出外电路,放电时,离子返回电解液中,存储的电荷通过外电路释放其原理图如图1.4.2所示,充放电是一个法拉第过程。

图1.4.2 赝电容器充电状态电位分布图
E0-Ea 充电状态正极电位 E0-Eb 充电状态负极电位
1.5 超级电容器性能参数[11]
(1)比电容:表示电容器容纳电荷的能力,单位质量或单位体积的电容器所给出的容量,分别称为质量比电容或体积比电容(F/g或F/cm3)。
(2)比能量:指单位质量或单位体积的电容器所给出的能量,分别称为质量比能量或体积比能量(W.h/kg或W.h/L)。
(3)比功率:单位质量或单位体积的超级电容器所给出的功率,表征超级电容器所承受电流的大小。超级电容器的比功率是电池的数量级倍数。
(4)内电阻:指电容器的内部阻力,与电极材料、隔膜、组装方式等有关。
(5)漏电流:指在充电时阻碍电容器电压的升高、放电时加速电压下降的那部分非正常电流。
(6)循环寿命:超级电容器经历一次充电和放电为一个循环,超级电容器循环寿命可达105~106次以上。
1.6 超级电容器电极材料
理想电极材料需要具备高的比表面积,合适的孔隙度,导电性好,足够的电活性位点,高的热稳定性和化学稳定性,成本低等特点。高的比表面积,对于双电层电容有很大的贡献,孔隙度影响比电容和倍率性能,导电性好有利于倍率性能和功率密度的提高,电活性位点主要用于氧化还原反应产生赝电容,热稳定性和化学稳定性高有利于循环的稳定性。
1.6.1 碳材料
碳基超级电容器是根据电双层的储能机制来储能的,基于碳材料的双电层超级电容器由于电极在充放电过程中不发生化学变化而具有优异的循环稳定性,使用寿命长。它们的比容量由有效电极比表面积和孔径分布决定。目前研究较多的超级电容器碳电极材料主要有活性炭、碳纤维、碳气凝胶、石墨烯和碳纳米管等。
活性炭材料具有导电性好、比表面积大、成本低、制备简单、对环境友好等优势,是应用最早、技术最为成熟的超级电容器炭基材料。目前,活性炭已有椰壳基[12-14]、果壳基[15]等不同原料基活性炭材料在超级电容器中用做电极材料。
碳纳米管具有独特的中空结构、良好的导电性、大的比表面积,成为超级电容器的理想材料。
石墨烯是完全离散的单层石墨材料,其整个表面可以形成双电层,并且石墨烯具有高的比表面积和优良的导电性,有利于提高超级电容器的比功率和比能量。因此石墨烯应用于超级电容器上有独特的优势。
1.6.2 金属氧化物
金属氧化物电极由于其氧化和还原反应是可逆的,具有良好的电子导电性,以及在水合氧化物晶格结构中较易进行电子和质子跃迁,从而引起质子嵌入和抽出。因此,它能将赝电容器的可逆反应深入到电极内部,将能量存储在三维空间,提高比能量。
大多数金属氧化物除二氧化钌[16]外,导电性都很低,金属氧化物的高电阻率,增加了电荷迁移阻力,因此,功率密度和倍率性能差,限制了超级电容在实际中的应用;单纯的金属氧化物在充放电过程中容易因为应变引起电极开裂,导致稳定性差;金属氧化物的比表面积,孔分布以及孔隙度难以调控。而钌作为贵金属,价格高昂,且氧化钌孔隙率不高,不利于商业化。
氧化镍由于其资源广泛、价格低廉、环境友善等特点而备受人们的关注,是发展超级电容器极具潜力的候选电极材料。
氧化镍的制备方法有很多,包括电化学沉积法[17-18],水解法[19],水热反应法[20]等。水热反应法,是在密闭容器中,通过加热创造一个高温高压环境,以水溶液为反应介质,使难溶或不溶的物质溶解,重结晶,以合成新的物质。
水热法便于控制温度,可以在相对较低的反应温度下进行(100-200℃),提高了实验的安全性;水热法在反应过程中,在密闭体系中产生高温高压环境,反应速率更快,提高了生产效率;水热法生长的物质颗粒小,形状可控;水热法具有环境友好,操作简单,生产成本低的优点。
通过控制水热反应参数[20-24]:pH,表面剂、水热反应时间、热处理温度等,可以制备不同形貌(纳米线、纳米片、多孔等)的氧化镍。
1.6.3 金属氧化物与碳基复合电极材料
碳基材料和过渡金属氧化物的复合物作为超级电容器的电极,结合了过渡金属氧化物的高比电容和碳基材料的大比表面积,同时具备了两种材料的优点,弱化了各自的缺点。碳结构不仅可以作为金属氧化物的物理支持,还提供了电荷传输通道,并且具有高的电子传导性,在大的充电放电电流下具有良好的倍率性能,功率密度不衰减的优点,金属氧化物是存储电荷和能量的主要来源。利用这种协同效应,可以大幅降低材料成本。
通过将氧化镍与活性炭[25-28]、碳纳米管[29] 、石墨烯[30]等碳基材料复合,发挥各自的优势,得到高性能的电极材料。
参考文献
[1] 江泽民. 对中国能源问题的思考[J]. 上海交通大学报,2008,42(3):345-359.
[2] John M.Miller. Ultracapacitor Applications[M]. London: Institution of engineering and Technology, 2011.
[3] B.E.Conway. Electrochemical Capacitors: Their Nature Function,and Application,Chemistry Department,University of Ottawa, Ottawa, Ontario, Canada.Available online.
[4] 刘玉荣. 碳材料在超级电容器中的应用[M]. 北京:国防工业出版社,2013.
[5] Yoda S,Lshihara K. The Advent of Battry-based Societies and the Global Environment in the 21st Century[J]. Power Sources, 1999, 81(81-82): 162-169.
[6] Becker H I. Low Voltage Electrolytic Capacitor[P]. USP 2800616,1954.
[7] Boos D L. Electrolytic Capacitor Having Carbon Paste Electrodes[P]. USP 3536963,1970.
[8] Pandolef A G, HollenkamPA F. Carbon Properties and Their Role in Supercapacitors [J]. Power Sources, 2006, 157(1): 11-27.
[9] Burke A. Ultracapacitors:Why,How,and Where Is the Technology[J]. Power Sources, 2000, 91(1): 37-50.
[10] Jiang H, Ma J, Li C. Mesoporous carbon incorporated metal oxide nanomaterials as supercapacitor electrodes[J]. Advanced Materials, 2012, 24(30): 4197-4202.
[11] Koch V R. Recent Advances in Electrolytes for Electrochemical Double Layer Capacitors[C]. 1st International Symposium on Large Ultracapacitor Technology and Application, Honolulu, Hawaii. 2005.
[12] 郑祥伟,胡中华,刘亚菲,等. 中等比表面积高容量活性炭电极材料制备和表征[J]. 复旦学报(自然科学版),2009,48(1):58-65.
[13] 刘亚菲,胡中华,任炼文,等. 高性能活性炭电极材料在双电层电容器中的应用[J]. 新型炭材料 ,2007,24(4):355-360.
[14] 周鹏伟,李宝华,康飞宇. 椰壳活性炭基超级电容器的研制与开发[J]. 新型炭材料,2006,21(2):125-131.
[15] 杨静,刘亚菲,陈晓妹,等. 高能量和比功率炭电极材料[J]. 物理化学报,2008, 24(1):13-19.
[16] Shaikh J S, Pawar R C, Devan R S, et al. Synthesis and characterization of Ru doped CuO thin films for supercapacitor based on Bronsted acidic ionic liquid[J]. Electrochimica Acta, 2011, 56(5): 2127-2134.
[17] Nan K W, Kim K B. A Study of the NiOx Electrode Via Electrochemical Route For Supercapacitor Applications and Their charge Storage Mechanism [J]. Electrochem.Soc., 2002, 149(3): A346-A354.
[18] Srinivasan V, Weidner J W. An Electrochemical Route For Making Porous Nickel Oxide Electrochemical Capacitors[J]. Electroehem.Soc.,1997,144(8):L210-L213.
[19] 王晓峰,孔祥华,刘庆国,等.氧化镍超级电容器的研究[J]. 电子元件与材料,2000,19(5):669-673.
[20] Liu X M, Zhang X G, Fu S Y. Preparation of Urchinlike NiO Nanostructures and Their Electrochemical Capacitive Behaviors[J]. Mater. Res.Bull., 2006,41(3): 620 -627.
[21] Xiaojun Zhang, Wenhui Shi, Jixin Zhu. Synthesis of Porous NiO Nanocrystals with Controllable Surface Area and Their Application as Supercapacitor Electrodes[J]. Nano Res. 2010, 3(9): 643–652.
[22] P. Justin, Sumanta Kumar Meher, G. Ranga Rao.Tuning of Capacitance Behavior of NiO Using Anionic, Cationic, and Nonionic Surfactants by Hydrothermal Synthesis[J]. J. Phys. Chem. C 2010, 114: 5203–5210.
[23] Yanzhen Zheng, Haiyang Ding, Milin Zhang. Preparation and electrochemical properties of nickel oxide as a supercapacitor electrode material[J]. Materials Research Bulletin .2009,44:403–407.
[24] U.M. Patil, R.R. Salunkhe, K.V. Gurav. Chemically deposited nanocrystalline NiO thin films for supercapacitor application[J]. Applied Surface Science .2008,255:2603–2607.
[25] Yuan G H. Jiang Z H, Aramata A, et al. Electrochemical Behavior of Activated carbon capacitor Material Loaded With Nickel Oxide [J]. Carbon, 2005(43): 2913-2917.
[26] Jong Hyeok Park, O. Ok Park, Kyung Hee Shin,et al. An Electrochemical Capacitor Based on a Ni(OH)2/Activated Carbon Composite Electrode[J]. Electrochemical and Solid-State Letters, 2002,5(2): H7-H10.
[27] Qinghua Huang, Xianyou Wang, Jun Li,et al. Nickel hydroxide/activated carbon composite electrodes for electrochemical capacitors[J]. Journal of Power Sources ,2007,164:425–429.
[28] Anirudha Jena , N. Munichandraiah, S.A. Shivashankar. Carbonaceous nickel oxide nano-composites: As electrode materials in electrochemical capacitor applications[J]. Journal of Power Sources ,2013,237:156-166.
[29] anzhen Zheng, Milin Zhang, Peng Gao. Preparation and electrochemical properties of multiwalled carbon nanotubes–nickel oxide porous composite for supercapacitors[J]. Materials Research Bulletin, 2007,42:1740–1747.
[30] Hailiang Wang, Hernan Sanchez Casalongue, Yongye Liang, et al. Ni(OH)2 Nanoplates Grown on Graphene as Advanced Electrochemical Pseudocapacitor Materials[J]. J.AM.CHEM.SOC,2010,132:7472-7477.
-
开题报告文献综述范本
某框架结构文献综述报告浅谈我国多层混凝土框架结构设计1.前言随着社会的发展,钢筋混凝土框架结构的建筑物越来越普遍.由于钢筋混凝土结…
- 开题报告&文献综述范文
-
开题报告文献综述范文
学生姓名学号专业技术经济班设计论文题目资本运营及某某企业资本运营的案例分析指导教师200年4月21日目录毕业论文开题报告1论文题目…
-
开题报告文献综述范文
开题报告文献综述范文学生姓名学号专业技术经济班设计论文题目资本运营及某某企业资本运营的案例分析指导教师200年4月21日目录毕业论…
-
开题报告文献综述范文
开题报告文献综述范文学生姓名学号专业技术经济班设计论文题目资本运营及某某企业资本运营的案例分析指导教师200年4月21日目录毕业论…
-
开题报告和文献综述怎么写
(一)论文名称论文名称就是课题的名字第一,名称要准确、规范。准确就是论文的名称要把论文研究的问题是什么,研究的对象是什么交待清楚,…
-
开题报告中的文献综述怎么写?
文献综述及其写作方法写文献综述是我们写论文的第一步,也是非常重要的一步。在我们要写一个文章或研究某一个问题时,我们一般首先做的就是…
-
开题报告和文献综述的写法
开题报告一课题开题报告的含义与作用开题报告就是当课题方向确定之后课题负责人在调查研究的基础上撰写的报请上级批准的选题计划它主要说明…
- 开题报告&文献综述范文
-
这学期就用了!开题报告、文献检索账号、文献综述、外文翻译、抄袭检测软件
这学期就用了开题报告文献检索账号文献综述外文翻译抄袭检测软件论文目录都在这了都在这了有备无患拿去吧来源齐祥涛的日志开题报告文献综述…
-
开题报告,文献综述,外文翻译
开题报告、文献综述、外文翻译、论文反抄袭软件、论文目录,就差论文正文了,其他都全了!!开题报告主要包括以下几个方面:(一)论文名称…