药物化学及药物合成反应实验指导书
药物化学及药物合成反应实验指导书
(供药学、制药工程、药剂、药学专升本、 药学专科、药分专科专业用)
药物化学-制药工程教研室编写
安徽中医学院自编
1
前 言
我国加入世界贸易组织(WTO)以来,制药行业迎来难得的发展机遇,也面临着前所未有的挑战。我国的药物研究正经历着一个从仿制为主到创制新药为主的历史性转变时期,如何抓住机遇,顺利实现这个历史性转变,关键在于创新型人才的培养。药物化学是药学类各专业和制药工程专业重要的专业课,也是一们实验性很强的课程,在药学类创新型人才培养方面发挥着重要作用。安徽中医学院药物化学-制药工程教研室积极探索药物化学与药物合成反应实验课教学改革,并依据药物化学及药物合成反应教学大纲的要求编定了本实验指导用书,目的是通过实验加深理解药物化学的基本理论和基本知识,掌握合成药物的基本方法,掌握对药物进行结构改造与修饰的基本方法,了解拼合原理在药物化学中的应用,进一步巩固有机化学实验的操作技术及有关理论知识,培养学生理论联系实际的作风,实事求是,严格认真的科学态度与良好的工作习惯。在实验指导用书的编写中,介绍了药物的绿色合成内容和文献来源,安排了一些中药有效成分的合成,以及中药活性物质的结构修饰与改造内容,充分体现了中医药院校的特色和实用性。
本实验指导用书由三部分组成,第一部分介绍了实验室的安全常识和基本知识;第二部分介绍了十六个药物合成和中药有效提取、合成及结构改造与修饰内容;第三部分为附录介绍了生产工艺中避免使用和限制使用的溶剂和部分与药物化学或合成相关的文献来源,供实际工作中参考使用。
本实验教材是药化化学-制药工程教研室教学经验的集体总结,限于水平,难免有误,我们要在使用过程中不断总结经验,收集反映,以便进一步修正提高。
安徽中医学院药物化学-制药工程教研室
20xx年12月
2
目 录
第一部分 实验须知
一、 实验室安全
二、 化学药品、试剂的存储及使用
三、 废品的销毁
四、 实验室中一般注意事项
五、 实验记录和实验报告
第二部分 实验项目
一、苯妥英的制备
二、贝诺酯的制备
三、磺胺醋酰钠的制备
四、对羟基苯乙酮的制备
五、桂皮酰哌啶的制备
六、烟酸的制备
七、香豆素-3-羧酸的合成
八、苯佐卡因的合成
九、1,4-二氢吡啶类钙离子拮抗剂的绿色合成
十、阿司匹林的合成
十一、哌嗪枸橼酸盐的合成
十二、阿魏酸哌嗪盐的合成
十三、氟哌酸的合成
十四、去甲斑蝥素中间体的合成
十五、苦参生物碱的提取
十六、氧化苦参碱的化学合成
附录一:生产工艺中避免使用和限制使用的溶剂 附录二:部分与药物化学或合成相关的文献来源
3
第一部分 实验须知
一、 实验室安全
药物化学及药物合成反应和有机化学一样是一门实践性很强的学科,因此,在进入实验室工作之前,希望参加实验者必须对实验课程的内容,要有充分的准备,而且要通晓实验室的一些基本规则,遵守实验室安全操作须知,才能避免可能发生的一些危险情况。
(一)眼睛安全防护
在实验室中,眼睛是最容易受到伤害的。飞溅出的腐蚀性化学药品和化学试剂,进入眼睛会引起灼伤和烧伤;在操作过程中,溅出的碎玻璃片或某些固体颗粒,也会使眼睛受到伤害;更有甚者,有可能发生的爆炸事故,更容易使眼睛受到损伤。因此在实验室中,最重要的是要佩戴合适的护目镜。护目镜一般是有机玻璃的,并有护眶,可以遮挡住整个眼睛。为了安全起见,在进入实验室后要养成戴护目镜的习惯。
一旦有化学药品或酸、碱液溅入眼睛,应赶快用大量的水冲洗眼睛和脸部,并赶快到最近的医院进行治疗。如有固体颗粒或碎玻璃进入眼睛,请切记不要揉眼睛,立即去有关医院进行治疗。
(二)预防火灾
有机药物合成实验中,由于经常使用挥发性强的、易燃性的各种有机试剂或溶剂,最容易发生的危险就是火灾。因此在实验室中应严格遵守实验室的各项规章制度,从而预防火灾的发生。
在实验室或实验楼内禁止吸烟。实验室中使用明火时应考虑周围的环境,如周围有人使用易燃易爆溶剂时,应禁用明火。
4
一旦发生火灾,不要惊慌,须迅速切断电源、熄灭火源,并移开易燃物品,就近寻找灭火器材,扑灭着火。如容器中少量溶剂着火,可用石棉网、湿抹布或玻璃盖住容器口,扑灭着火;其他着火,如有机溶剂着火,应采用干粉灭火器进行扑灭,并立即报告有关部门或打119火警电话报警。
在实验中,万一衣服着火了,切勿奔跑,否则火借风势会越烧越烈,可就近找到灭火喷淋器或自来水龙头,用水冲淋使火熄灭。
(三)割伤、烫伤和试剂灼伤的处理
1. 割伤
遇到割伤时,如无特定的要求,应用水充分清洗伤口,并取出伤口中的碎玻璃或残留固体,用无菌的绷带或创口贴进行包扎、保护。大伤口应注意压紧伤口或主血管,进行止血,并急送医院进行处理。
2. 烫伤
因火焰或因触及灼热物体所致的小范围的轻度烫伤、烧伤,可通过立即将受伤部位浸入冷水或冰水中约5 min以减轻疼痛。重度的大范围的烫伤或烧伤应立即去医院进行救治。
3. 化学试剂灼伤
对于不同的化学试剂灼伤,处理方法不一样。
(1)酸------立即用大量水冲洗,再用3%~5%NaHCO3溶液淋洗,最后用水冲洗10~15 min。严重者将灼伤部位拭干包扎好,到医院治疗。
(2)碱------立即用大量水冲洗,再用2%醋酸溶液或1%硼酸溶液冲洗,以中和碱,最后再用水冲洗10~15 min。严重时处理同上。
5
(3)溴------立即用大量水冲洗,再用10%硫代硫酸钠溶液淋洗或用湿的硫代硫酸钠纱布覆盖灼伤处,至少3h。
(4)有机物-------用酒精擦洗可以除去大部分有机物。然后再用肥皂和温水洗涤即可,如果皮肤被酸等有机物灼伤,将灼伤处浸在水中至少3 h,然后请医生处理。
(四)中毒预防
有毒物质溅入口中尚未咽下者应立即吐出,用大量水冲洗口腔。如已吞下,应根据毒物性质进行解毒,并立即送有关医院救治。
刺激性及神经性毒物中毒,先用牛奶或鸡蛋使之冲淡或缓和,再设法催吐,使误入口中的毒物吐出,并送医院救治。
吸入气体中毒者,将中毒者移至室外通风处,解开衣领或纽扣,使其呼吸新鲜空气,必要时实施人工呼吸。
二、化学药品、试剂的存储及使用
(一) 化学药品的贮存
一般实验室中不应存储过多的化学药品和试剂,应实行需要多少,领用多少的原则。在大多数情况下,实验室所用的化学药品都存储在玻璃瓶中,高粘度的液体放在广口瓶中,一般性液体存放在细颈瓶中,NaOH和KOH溶液保存在带橡皮塞或塑料塞的瓶中。对于能够与玻璃发生反应的化合物(如HF),则使用塑料或金属容器,碱金属放在煤油中,黄磷则以水覆盖。
对光敏感的物质,包括醚在内,都有形成过氧化物的倾向,在光线的作用下更是如此,应将它们贮藏在棕色玻璃瓶中。
6
对产生毒性或腐蚀性蒸气的物质(如溴、发烟硫酸、盐酸、氢氟酸)建议放在通风橱内专门的地方。
少量对潮气和空气敏感的物质常密封贮存于玻璃安瓿中。
某些毒品(如氰化物、砷及其化合物等)应按有关部门的规定进行保管和贮存。
(二) 化学药品使用中的注意事项
有机溶剂具有易燃和有毒两个特点。
易燃的有机溶剂(特别是低沸点易燃溶剂)在室温时有较大的蒸气压,当空气中混杂易燃有机溶剂的蒸气达到某一极限时,遇有明火即发生燃烧爆炸。而且有机溶剂蒸气都较空气的密度大,会沿着桌面或地面漂移至较远处,或沉积在低洼处。因此,在实验室中用剩的火柴梗切勿乱丢,以免引起火灾。也不要将易燃溶剂倒入废物缸中,更不能用开口容器盛放易燃溶剂。
有机溶剂以较为隐蔽的方式产生对人体的毒害,在使用中应注意最大限度地减少与有机溶剂的直接接触,不要掉以轻心。实验室应充分通风。在正规、小心操作下,有机溶剂不致造成任何健康问题。操作有毒试剂和物质时,必须戴橡皮手套或一次性塑料手套,操作后立即洗手。注意切勿让有毒物质接触五官或伤口。
三、废弃物的处理
碎玻璃和其他锐角的废物不要丢入废纸篓或类似的盛器中,应该使用专门的废物箱。不要把任何用剩的试剂倒回试剂瓶中,因为其一会对试剂造成污染,影响他人的实验;其二由于操作的疏忽导致错误引入异 7
物,有时会发生剧烈的化学反应甚至会引起爆炸。
危险的废品,如会放出毒气或能够自燃的废品(活性镍、磷、碱金属等),决不能丢弃在废物箱或水槽中。不稳定的化学品和不溶于水或与水不混溶的溶液也禁止倒入下水道,应将它们分类集中后处理。对能与水混溶,或能被水分解或腐蚀性液体,倒掉处理时,必须用大量的水冲洗。金属钾或钠的残渣应分批小量地加到大量的醇中予以分解(操作时戴防护目镜)。
四、实验室中一般注意事项
1、实验进行之前,应当认真预习有关实验内容,了解基本原理和方法。
2、应严格按照实验步骤进行操作,实验进行中,必须思想集中,认真观察反应是否正常,不得擅自离开。
3、养成及时记录的良好习惯,记录观察到的现象、结果等写出实验报告。
4、药品试剂必须严格按规定定量取用,取出的药品试剂不可再倒回原瓶中,以免带入杂质。取用完毕,应立即盖上瓶塞,归还原处。
5、遵从教师指导,注意安全,发生意外事故,立即报告教师。
6、保持实验室整洁、干燥,做到桌面、地面整洁。实验完毕,及时洗净仪器,整理实验室,关水、电。
五、实验记录和报告
做好实验记录和实验报告是每一个科研人员必备的基本素质。实验记录应记在专门的实验记录本上,实验记录本应有连续页码。所有观察 8
到的现象、实验时间、原始数据、操作和后处理方法、步骤均应及时、准确、详细地记录在实验记录本上,并签名,以保证实验记录的完整性、连续性和原始性。将实验情况记录在便条纸、餐巾纸、纸巾等容易失落或损失的地方的任何做法都是错误的。
在做实验前,对所做的实验应该充分做好预习工作。预习工作包括反应的原理,可能发生的副反应、反应机理、实验操作的原理和方法,产物提纯的原理和方法,注意事项及实验中可能出现的危险及处置办法,应给出详细的报告。同时还要了解反应中化学试剂的化学计量和用量,对化学试剂和溶剂的理化常数等要记录在案以便查询。
实验记录格式:
实验题目: 实 验 人:
一、 实验目的:
二、 反应原理(反应方程式):例如 A + B
三、 投料比
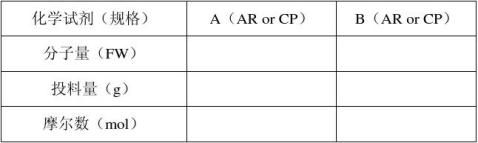
A + BC + DC + D
9
四、实验操作步骤
五、实验现象及监控记录
六、实验结果[产品 (g),收率。m.p. ℃。光谱数据及编号]。
七、分析讨论(小结)。
10
第二部分 实验项目
实验一、苯妥英钠(Phenytoin Sodium)的合成
苯妥英钠(Phenytoin Sodium), 化学名为5,5-二苯基-2,4-咪唑烷二酮钠盐,又名大伦丁钠(Dilantin Sodium)。为乙内酰脲类抗癫痫药物。它抗惊厥作用强,虽然毒性较大,并有致畸形的副作用,但仍是控制癫痫大发作和部分性发作的首选药物,但对癫痫小发作无效。
本品为白色粉末,无臭,味苦,微有引湿性。在空气中渐渐吸收CO2,转化成苯妥英。
苯妥英钠的化学结构式:
HNONa
分子式:C15H11N2NaO2,分子量:274.25。
一、实验目的
1. 掌握安息香缩合反应的基本原理和操作方法。
2. 熟悉乙内酰脲环合原理和操作。
3. 了解苯妥英合成的基本路线。
二、实验内容
1.二苯乙醇酮的制备
2.二苯乙二酮的制备
3.苯妥英钠的制备
三、实验原理
苯妥英通常用苯甲醛为原料,经安息香缩合,生成二苯乙醇酮,随后 11
氧化为二苯乙二酮,再在碱性醇液中与脲缩合、重排制得。
CHO
Vit BNaOH
四、实验材料与设备 1.实验设备、仪器
OOOHH
HNOO
ONaOH
HNONaHNONa
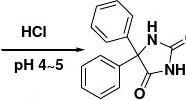
NaOH, C2H5OH
pH 11~12圆底烧瓶(100ml)、三颈烧瓶、球形冷凝管、布氏漏斗、抽滤瓶、循环水真空泵、 2.实验材料、试剂
苯甲醛 、VitB1盐酸盐 、95%乙醇、65%~68%硝酸、尿素、盐酸,NaOH。 五、实验步骤 1.安息香缩合【注1】
在200ml圆底烧瓶中加入VitB1盐酸盐3.6g、12ml蒸馏水和30 mL 95%乙醇,塞住瓶口,不时摇动,待VitB1盐酸盐溶解后,放在冰浴中冷却。10分钟后,将2 mol/L氢氧化钠溶液10 mL加入圆底烧瓶中,充分摇动后立即加入苯甲醛20mL

,混合均匀,然后在圆底烧
12
瓶中加搅拌子,上面加冷凝管,放水浴中搅拌并加热回流,水浴温度控制在60~75℃之间,回流1小时后加热到80~90℃再回流1小时。反应液呈橘红色均相溶液,冷却反应物至室温,抽滤得浅黄色晶体,冷水洗,抽干得粗品供下步使用。
2. 二苯基乙二酮的制备
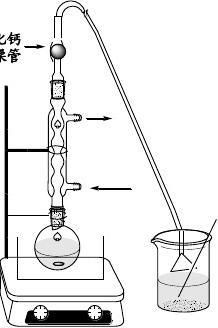
取8.5g粗制的安息香于50m1或
100ml圆底烧瓶中,加10ml浓硝酸,安装
回流冷凝器以及气体吸收装置,在沸水浴
上加热,如果反应器太小,搅拌子不能正
常搅拌,需加入沸石并随时振摇,直至二
氧化氮气体逸去完全(约2小时),趁热倾
出反应物至盛有200 ml冷水的烧瓶中,不
断搅拌,直至油状物结晶成为黄色固体,抽滤,用水充分洗去HNO3(可用pH试纸测量判断),干燥得二苯基乙二酮,m.p. 89~92℃(纯二苯基乙二酮的m.p. 95℃)。
3.苯妥英的制备
将二苯基乙二酮粗品8g,尿素3 g置于150 mL圆底烧瓶中,加入15%氢氧化钠溶液25 mL,95%乙醇40 mL,回流1小时后倾入300 mL冷水中,放置半小时待沉淀完全,滤去黄色的二苯乙炔二脲沉淀,滤液用15%盐酸酸化至沉淀完全析出,抽滤得白色苯妥英,如果产品颜色较深,应重新溶于碱液后,加活性碳煮沸10 min左右,冷却后,再酸化得白色针状结晶,mp:295~298℃。
13
将苯妥英混悬于4倍水中,水浴上温热至40℃,搅拌下滴加20%NaOH溶液至全溶,加活性碳少许,加热5 min,趁热抽滤,放冷,析出结晶(如滤液析不出结晶,可加氯化钠至饱和),抽滤,少量冰水洗涤,干燥得苯妥英钠,称重,计算收率。
六、注意事项
1.苯甲醛极易氧化,长期放置有苯甲酸析出,本实验苯甲醛中不能含苯甲酸,因此临用前需蒸馏。
HNONH
2.副产物二苯乙炔二脲的生成(结构式如下) 3.硝酸氧化时,有大量NO2逸出,必须用导管导入NaOH溶液中吸收。
七、实验报告内容
写出实验目的、原理、所用仪器及型号,记录实验过程、现象及结果,并进行分析与讨论。
八、思考题
1.安息香缩合反应的反应液,为什么自始至终要保持碱性?
2.形成乙内酰脲时,产生的副产物是什么?
3.苯妥英能溶于NaOH溶液中的原因是什么?
[注1]:通常将生成的二苯乙醇酮称为安息香,所以这一类反应也称为安息香缩合反应。早些年此反应的催化剂是氰化钾或氰化钠,由于氰化物是剧毒物,如果使用不当会有危险性,本实验使用维生素B1作催化剂,其特点在于原料易得、无毒、反应条件温和,而且产率也比较高。
14
创新实验设计:二苯基乙二酮的非硝酸氧化法合成
OOHHOOX = HNO3; FeCl3. 6H2O; NaNO2/(CH3CO)2O; Cu(OAc)2/NH4NO3/AcOH
将同学分组,安排学生查阅文献,设计不同的氧化方法,合成二苯基乙二酮,并比较各氧化方法之间的收率,熔点,产品纯度以及三废污染情况的差异,最终得出最佳合成工艺条件。
1. FeCl3.6H2O为氧化剂的合成
在装有球形冷凝器的250 mL圆底烧瓶中,依次加入FeCl3.6H2O 14 g,冰醋酸15 mL,水6 mL及沸石一粒,在石棉网上直火加热沸腾5 min。稍冷,加入安息香2.5 g及沸石一粒,加热回流50 min。稍冷,加水50 mL及沸石一粒,再加热至沸腾后,将反应液倾入250 mL烧杯中,搅拌,放冷,析出黄色固体,抽滤。结晶用少量水洗,干燥,得粗品,测熔点,计算收率。
2. NaNO2/(CH3CO)2O为氧化体系的合成
在250 mL圆底烧瓶中,加入安息香10.6 g, NaNO2 10.8 g及醋酐30 g,在冰水浴冷却下,搅拌反应30 min,加水200 mL溶解未反应的NaNO2,抽滤,水洗涤至中性,干燥,得二苯基乙二酮,测熔点,计算收率。
3. Cu(OAc)2.H2O/NH4NO3/AcOH为氧化体系的合成
在反应瓶中加入Cu(OAc)2.H2O (0.14 g, 7 mmol)、NH4NO3 (6 g, 76 mmol)及安息香 (12.8 g, 60 mmol)和80%的AcOH溶液 (45 mL),搅拌下, 15
回流反应1.5 h后,冷却,抽滤,得黄色针状结晶,母液加入95%乙醇 (4 mL)可再得部分晶体,合并结晶,用无水乙醇重结晶,干燥,得二苯基乙二酮纯品,测熔点,计算收率。
创新实验设计:正交设计法优选苯妥英合成工艺
正交设计法是优化合成工艺常用的方法之一。由于正交设计法是基于数理统计原理来科学合理地安排实验,并按一定规律分析处理实验结果,从而能够较快地找到工艺的最佳条件,且具有可判断诸多因素中何种影响因素是主要因素,以及判断影响因素之间的相互影响情况等优点。
本实验采用正交设计法对苯妥英合成最后一步(即二苯乙二酮与尿素缩合)进行工艺优选,选取三个因素进行实验,即尿素加入量(配料比)(A),碱(NaOH)浓度(B)和反应时间(C),并确定了它们的实验水平(A: 1g,2g;B: 10% , 15%;C:60 min,80 min)。实验目的是考察因子A,B,C对苯妥英收率有什么影响,并确定最佳工艺条件;进一步了解杂环的合成方法。
实验步骤为:将二苯乙二酮(联苯甲酰)2g,尿素g置于150mL
园底烧瓶中,加入 %NaOH溶液25mL,95%乙醇40mL,回流 min后倾入300mL冷水中,放置半小时待沉淀完全,滤除黄色的二苯乙炔二脲(副产物)沉淀。滤液用15%盐酸酸化至沉淀完全析出,抽滤得白色苯妥英,如果产品颜色较深,应重溶于碱液,再酸化得白色针状结晶,mp:295-298℃。干燥称重,计算产率。
16
OO
OHNaOH, C2H5OH
L8(27)正交实验方案及结果表
操作组号
实验号 1 2 3 4 5 6 7 8 K1 K2 R
尿素(A)/g
1 1 1 1 2 2 2 2
碱量(B)/% 时间(C)/ min
10 10 15 15 10 10 15 15
60 80 60 80 60 80 60 80
收率
/%
----- ----- -----
1, 9,17,25 2,10,18,26 3,11,19,27 4,12,20,28 5,13,21,29 6,14,22,30 7,15,23,31 8,16,24,32 ――――――― ――――――― ―――――――
对实验结果进行极差分析和方差分析,确定最佳工艺,并解释原因。
17
实验二、磺胺醋酰钠的制备
磺胺是临床上应用最早的磺胺类抗菌药,但水溶性小,不便应用,磺胺分子中的磺酰氨基近乎中性。虽可与NaOH成盐而水溶性增大,但极易水解,水溶液呈强碱性,也不能应用于临床,如果将磺酰氨基进一步酰化,酸性增强,成钠盐后,水解性减低,碱性减弱,能在临床上应用,乙酰化的产物为磺胺醋酰。其钠盐近中性,可配成滴眼剂使用。
一、 实验目的
1.了解磺胺醋酰合成的基本路线.
2.熟悉pH、温度等条件在药物合成中的重要性.
3.掌握利用理化性质的差异来分离纯化产品的方法.
二、 实验内容
磺胺醋酰的制备及产品的分离纯化。
三、实验原理
在碱性条件下以磺胺为原料与乙酸酐反应,磺酰氨基乙酰化制备得到磺胺醋酰,再与氢氧化钠反应制备磺胺醋酰钠。
H2NSO2NH2NaOHH2NSO2NHH2NSO2NCOCH3
NaOHH2NSO2NCOCH3
H2N(CH3CO)2ONaOHSO2NHCOCH3
注:乙酐酰化时有副产物双乙酰化物产生。 H3NHSO2NHCOCH3
18
四、实验材料与设备
1.实验设备、仪器
圆底烧瓶(100 mL),球形冷凝管,布氏漏斗,抽滤瓶,温度计,恒温磁力搅拌器,三颈瓶,抽滤瓶,布氏漏斗。
2.实验材料、试剂
NaOH(分析纯),磺胺(药用),醋酐(分析纯),盐酸(分析纯),活性碳(化学纯)。
五、实验步骤
(一) 磺胺醋酰的制备
在装有搅拌、温度计、回流冷凝管的250 mL三颈烧瓶中,加入26 g磺胺(SA)和22.5%的NaOH溶液(33 mL)。搅拌,水浴逐渐升温至50~55℃,待物料溶解后,滴加Ac2O(7.5 mL),5 min后加入77%NaOH溶液4.5 mL(注1),并保持反应液pH在12~13之间,剩余13 mL醋酐与14.5 mL 77%NaOH溶液以每隔5 min每次2 mL(注2)交替加入。加料期间的反应温度维持在50~55℃及pH在12~14(注3)。加料完毕后,继续搅拌30 min。反应结束后将反应液倾入250 mL烧杯中,加水30 mL稀释,滴加浓盐酸酸化至pH 7,于冰水浴中冷却1 h左右,析出未反应原料磺胺,过滤,滤饼用少量冰水洗涤(注4),滤液与少量洗液合并后用浓盐酸调pH至4~5,有固体析出,过滤,将滤饼压紧抽干(注5),滤饼用3倍量的10%盐酸溶液溶解,放置30 min,抽滤除去不溶物,滤液加少量活性碳室温脱色10 min,过滤,滤液用40%的NaOH溶液调pH至5,析出磺胺醋酰粗品,过滤,滤饼用10倍左右的水加热,使产品溶 19
解,趁热过滤,滤液放冷,慢慢析出结晶,过滤,干燥得磺胺醋酰精制品,m.p. 179~182℃。
(二) 磺胺醋酰钠的制备
将所得磺胺醋酰精制品放入100 mL烧杯中,以少量水浸润后,于水浴上加热至90℃,用滴管滴加40%NaOH溶液至pH为7~8恰好溶解,趁热过滤,滤液移至烧杯中,冷却析出晶体,滤取结晶,干燥,得磺胺醋酰钠产品。
六、附注
1. 本实验中使用NaOH溶液有多种不同浓度,在实验中切勿用错,否则会导致实验失败。
2. 滴加醋酐和NaOH溶液是交替进行,每滴完一种溶液后,让其反应5 min后,再滴加另一种溶液。滴加是用滴管加入,滴加速度以液滴一滴一滴滴下为宜。
3. 反应中保持反应液pH在12~13之间很重要,否则收率将会降低。
4. 在pH为7时析出的固体不是产物,应弃去。产物在滤液中,切勿搞错。在pH 4~5析出的固体是产物。
5. 在本实验中,溶液pH的调节是反应能否成功的关键,应小心注意,否则实验会失败或收率降低。
6. 氢氧化钠固体及其溶液具有强腐蚀性,不慎粘有时,应及时用大量清水冲洗。
7. 醋酐具有催泪性和腐蚀性,取用时在通风橱中进行,不慎粘有时,应及时用大量清水冲洗。
20
七、实验报告内容
写出实验目的、原理、所用仪器及型号,记录实验过程、现象及结果,并进行分析与讨论。
八、思考题
1.反应中用NaOH的作用是什么?
2.在制备SA时,芳伯胺基可发生酰化吗?
3.该制备中产生哪些副产物,应如何减少副产物提高收率?
21
实验三、桂皮酰哌啶的制备
胡椒碱是一种治疗癫痫病的药物。民间用“白胡椒加红心萝卜”治疗癫痫病作为秘方相传,经临床观察和药理试验,发现起治疗作用的是白胡椒, 并进而发现其有效成分是胡椒碱。
但胡椒碱的结构比较复杂,不容易合成。如果由胡椒提取则成本太高,不能大量生产。利用药物化学中的同系原理对胡椒碱进行结构改造时,发现3-(3,4-亚甲基二氧苯基)-丙烯酰哌啶也具有类似胡椒碱的药理作用,其结构简单,便于合成,已用于临床。临床上亦称为抗癫灵。 O
胡椒碱N抗癫灵ON
抗癫灵的结构简化物—桂皮酰哌啶结构更加简单,经药理实验证明,其药理作用与抗癫灵类似,并且具有广谱的抗惊作用,有一定的研究价值。
桂皮酰哌啶的化学结构:
桂皮酰哌啶
分子式:C14H17NO,分子量:215.30。
本品为白色或类白色晶体,无臭,无味。在乙醇中溶解,几乎不溶于水,m.p. 121~122℃。
一、实验目的
1.掌握氯化、酰化的基本原理。
2.熟悉无水操作及产品精制的方法。
3.了解桂皮酰哌啶的合成路线。
22
二、实验内容
1.桂皮酸的制备。
2.桂皮酰氯、桂皮酰哌啶的制备。
三、实验原理
芳香醛和酸酐在酸酐相应的碱金属盐存在下,发生类似醇醛缩合反应得到α,β-不饱和芳香酸。这个反应用于合成桂皮酸称为Perkin反应。生成的桂皮酸与二氯亚砜进行酰氯化反应得到酰氯化物,最后和哌啶缩合得到产物桂皮酰哌啶。
CHO
(CHCO)O
O
NOOH66OCl
四、实验材料与设备
1.实验设备、仪器
圆底烧瓶、空气冷凝管、CaCl2干燥管、长颈圆底烧瓶、球形冷凝管、克氏蒸馏烧瓶、温度计。
2.实验材料、试剂
苯甲醛、酸酐、无水醋酸钾、Na2CO3、无水苯、SOCl2、哌啶(六氢吡啶)、盐酸、无水Na2SO4、乙醇、活性碳。
五、实验步骤
1.桂皮酸的制备
23
配料比(重量比):苯甲醛∶醋酐∶醋酸钾=
1∶1.43∶0.6,在250 mL圆底烧瓶中加入20 g苯甲
醛,20ml醋酐和新熔焙过的12 g KOAc。安装空气
冷凝器及CaCl2干燥管,在油浴上加热回流振摇使溶
解,维持油浴温度160℃(内温约150℃)1.5小时,
然后升温至170℃加热2.5小时。(内温约160℃~
170℃)。
反应完成后,取下反应瓶,将反应物倒入125 mL
热水中,并用少量水冲洗反应瓶,在反应液中加入适量Na2CO3,调pH至8然后倒入500 mL圆底烧瓶中进行水蒸汽蒸馏,除尽未反应的苯甲醛后,加入适量活性炭约2匙,煮沸15分钟,趁热抽滤,冷却后,慢慢滴加浓盐酸酸化,边加边搅拌,使桂皮酸结晶析出完全,抽滤,水洗涤,干燥得粗品,用稀乙醇(V(水) ∶V(95%EtOH) = 3∶1)重结晶,得桂皮酸结晶,熔点131.5~132 ℃。
2.桂皮酰氯、桂皮酰胺的制备
配料比(重量比)∶桂皮
酸∶SOCl2∶C6H6∶哌啶=1∶0.89∶
19.04∶1.15,将干燥的桂皮酸7.4 g投
入250 mL圆底烧瓶中,加入60 mL苯,
加入SOCl2 4 mL,安装回流冷凝器,氯
化钙干燥管,气体吸收装置,在油浴上
加热回流至无HCl产生,约2.5~3 h
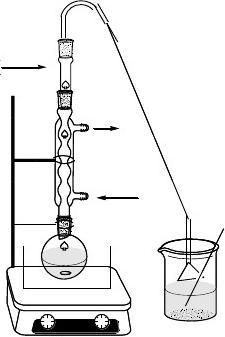
,
24
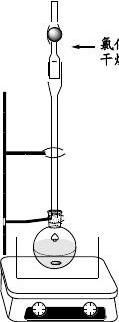
浴温90℃~100℃酰氯化反应完成后改换成蒸馏装置,减压蒸除苯,得到桂皮酰氯的结晶(熔点36℃或浆状物),蒸出的酸性苯勿倒入池中,回收。
将桂皮酰氯用100 mL无水苯温热溶解,分次加入哌啶10 mL充分振摇,密塞于室温放置2小时完成胺解反应。
将沉淀的哌啶盐酸盐抽滤除去,苯溶液用水洗两次(每次100 mL),分出水层,苯层再用10%HCl约100 mL洗至酸性,分离除去酸水,苯层再用饱和Na2CO3洗至微碱性,再用H2O洗至中性,分出苯层,加入无水Na2SO4干燥1小时(无水Na2SO4用前应先干燥,再使用)减压蒸馏除苯,析出产品,用EtOH重结晶,得桂皮酰哌啶,熔点121℃~122℃。
六、注意事项
1.苯甲醛容易被空气氧化生成苯甲酸,工业品或开口放置过的化学纯品均应重蒸。
2.桂皮酸的制备过程中无水条件的控制是反应的关键,无水醋酸钾必须新鲜熔融制得,方法:将含水醋酸钾在瓷蒸发器中加热,盐先在自身的结晶水中溶化,水分蒸发后再结晶成固体,强热使固体再熔化,并不断搅拌片刻,趁热倒在乳钵中,固化后研碎置于干燥器中待用。
3.醋酐中如含有水则分解成醋酸,影响反应,所以醋酸含量较低时应重蒸,SOCl2易吸水分解,用后应立即盖紧瓶塞,在通风柜中量取。
七、报告内容
写出实验目的、原理、所用仪器及型号,记录实验过程、现象及结果,并进行分析与讨论。
25
八、思考题
1.桂皮酸合成为什么必须在无水条件下进行?
2.醋酸钾为何必须新鲜熔融,如想提高收率可采取什么措施?
3.从羧酸制备酰氯有哪些方法?选用SOCl2的优点是什么?
4.苯酰氯化后蒸出的酸性苯中有哪些杂质?应如何将其处理回收?
5.桂皮酸合成反应中将反应物倒入事先沸腾的热水中,为什么?
26
实验四、烟酸的制备
烟酸(Nicotinic acid)学名为吡啶-3-羧酸,又称维生素B5,是B族维生素中的一种,富集于酵母、米糠之中,可用于防治糙皮病,也可用作血管扩张药,并大量用作食品和饲料的添加剂。作为医药中间体,可用于烟酰胺、尼可刹米及烟酸肌醇酯的生产。
烟酸的化学结构:
NCOOH分子式:C6H5NO2; 分子量:123
本品为无色针状结晶,m.p. 236~239℃。
一、实验目的
1.掌握高锰酸钾氧化法对芳烃的氧化原理及实验方法
2.熟悉酸碱两性有机化合物的分离纯化技术
3.了解烟酸的合成路线。
二、实验内容
1. 3-甲基吡啶的氧化反应
2. 烟酸的精制 三、实验原理
烟酸可以由喹啉经氧化、脱羧合成,但合成路线长,且所用的试剂为腐蚀性的强酸。因此可以通过对3-甲基吡啶的氧化来制取。
H2SO4
+2KMnO4
351% COOHCOOH_CO39% +2MnO2+KOH+H2O27
四、实验材料与设备
1. 仪器和设备
球形冷凝器、圆底烧瓶、三颈烧瓶、尾接管、布氏漏斗、抽滤瓶、圆底烧瓶、温度计、恒温磁力搅拌器。
2. 试剂和药品:3-甲基吡啶、 高锰酸钾、浓盐酸
五、实验步骤
1、投料比
化学试剂
分子量(FW)
投料量(g)
摩尔数(mol) 3-甲基吡啶 93 5 0.054 高锰酸钾 157.9 21 0.108 浓盐酸 36.5 适量 活性碳 适量
2、操作步骤
在配有回流冷凝管、温度计和搅拌子的
三口烧瓶中。加入3-甲基吡啶5 g、蒸馏水
200 mL水,水浴加热至85℃。在搅拌下,
分批加入高锰酸钾21 g, 控制反应温度在
85~90℃,加毕,继续搅拌反应1 h。停止反
应,改成常压蒸馏装置,蒸出水及未反应的
3-甲基吡啶,至流出液呈现不浑浊为止,约蒸出130 mL水,停止蒸馏,趁热过滤,用12 mL沸水分三次洗涤滤饼(二氧化锰),弃去滤饼, 合并滤液与洗液,得烟酸钾水溶液。
将烟酸钾水溶液移至500 mL烧杯中,用滴管滴加浓盐酸调pH值至3-4(烟酸的等电点的pH值约3.4,注意:用精密pH试纸检测),冷却析晶,过滤,抽干,得烟酸粗品。

28 加料口
3、精制
将粗品移至250 ml圆底烧瓶中,加粗品5倍量的蒸馏水,水浴加热,轻轻振摇使溶解,稍冷,加活性碳适量,加热至沸腾,脱色10 min,趁热过滤,慢慢冷却析晶(注1),过滤,滤饼用少量冷水洗涤,抽干,干燥,得无色针状结晶烟酸纯品,mp236~239℃。
六、附注
1.慢慢冷却结晶,有利于减少氯化钾在产物中的夹杂量。
2.氧化反应若完全,二氧化锰沉淀滤去后,反应液不再显紫红色。如果显紫红色,可加少量乙醇,温热片刻,紫色消失后,重新过滤。
3.精制中加入活性碳的量可由粗品的颜色深浅来定,若颜色较深可多加一些。
七、实验报告内容
写出实验目的、原理、所用仪器及型号,记录实验过程、现象及结果,并进行分析与讨论。
八、思考题:
1. 氧化反应若反应完全,反应液呈什么颜色?
2. 为什么加乙醇可以除去剩余的高锰酸钾?
3. 在产物处理过程后,为什么要将pH值调至烟酸的等电点?
4. 本实验在烟酸精制过程中为什么要强调缓慢冷却结晶处理?冷却速度过快会造成什么后果?
5. 如果在烟酸产物中尚含有少量氯化钾,如何除去?试拟定分离纯化方案。
29
实验五、香豆素-3-羧酸的合成
香豆素又名1,2-苯并吡喃酮,白色斜方晶体或结晶粉末,存在于许多天然植物中。它最早是1820年从香豆的种子中发现的,也含于薰衣草、桂皮的精油中。香豆素为香辣型,表现为甜而有香茅草的香气,是重要的香料,常用作定香剂,用于配制香水、花露水香精。香豆素的衍生物除用作香料外,还可以用作农药、杀鼠剂、药物等。
由于天然植物中香豆素含量很少,大量是通过合成得到的。1868年,Perkin用邻羟基苯甲醛(水杨醛)与醋酸酐、醋酸钠一起加热制得,称为Perkin合成法。
OHCOOH+OH- HOOH+CHO(CH3CO)2OCHCOONaOHCCCOONaHHO+HO
水杨醛和醋酸酐首先在碱性条件下缩合,经酸化后生成邻羟基肉桂酸,接着在酸性条件下闭环成香豆素。
本实验采用改进的方法进行合成,用水杨醛和丙二酸酯在有机碱的催化下,可在较低的温度合成香豆素的衍生物。这种合成方法称为Knovengel反应。水杨醛与丙二酸酯在六氢吡啶催化下,缩合生成中间体香豆素-3-甲酸乙酯。后者加碱水解,不但酯基而且内酯也被水解,然后再次环内酯化即生成香豆素-3-羧酸。
30
一、实验目的
1.掌握 Knovengel反应的基本原理和操作方法.
2.熟悉回流和重结晶的操作.
3.了解Perkin合成法。
二、实验内容
1.香豆素-3-甲酸乙酯的合成
2.香豆素-3-羧酸的合成
三、实验原理
凡具活性亚甲基的化合物(如丙二酸酯、β-酮酸酯、氰乙酸酯、硝基乙酸酯等)在氨、胺或其羧酸盐的催化下,与醛、酮发生醛醇型缩合,脱水而得α,β-不饱和化合物的反应称为Knovengel反应。
四、实验材料与设备
1.实验设备、仪器
圆底烧瓶、干燥管、锥形瓶、球形冷凝管、恒温磁力搅拌器、布氏漏斗、抽滤瓶
2.实验材料、试剂
水杨醛(5 g,0.014 mol)、丙二酸二乙酯(6.8 mL,0.045 mol) 31 CHO+CH2(COOC2H5)2NCOOC2H5NaOHCOONaCOONaOCOOH
六氢吡啶(0.5 mL)、无水乙醇(25 mL)、冰醋酸(2滴)、95%乙醇(适量)、NaOH、HCl、无水氯化钙。
五、实验步骤
1.香豆素-3-甲酸乙酯的合成
在干燥的100 mL圆底烧瓶中,加入4.2 mL水杨醛、6.8 mL丙二酸二乙酯、25 mL无水乙醇、0.5 mL六氢吡啶和2滴冰醋酸,放入几滴沸石后,装上回流冷凝管,冷凝管上口接一氯化钙干燥管。在水浴上加热回流2 h。稍冷后将反应物转移到锥形瓶中,加入30 mL水,置于冰浴中冷却。待结晶完全后,过滤,晶体每次用2-3 mL50%冰冷过的乙醇洗涤2-3次。粗产物为白色晶体,经干燥后重约6-7 g,mp 92-93℃。粗产物可用25%的乙醇水溶液重结晶,mp 93℃。
2.香豆素-3-羧酸的合成
在100 mL圆底烧瓶中加入4 g香豆素-3-甲酸乙酯、3 g氢氧化钠、20 mL95%乙醇和10 mL水,加入几粒沸石,装上回流冷凝管,用水浴加热至酯溶解后,再继续回流15 min。稍冷后,在搅拌下将反应混合物加到盛有10 mL浓盐酸和50 mL水的烧杯中,立即有大量白色结晶析出。在冰浴中冷却使结晶完全。抽滤,用少量冰水洗涤晶体,压干,干燥后重约为3 g,mp 188℃。粗品可用水重结晶。
纯品香豆素-3-羧酸的熔点为190℃(dec)。
六、报告内容
写出实验目的、原理、所用仪器及型号,记录实验过程、现象及结果,并进行分析与讨论。
32
七、思考题
1. 试写出利用Konvengel反应制备香豆素-3-羧酸的反应机理。反应中加入醋酸的目的是什么?
2. 如何利用香豆素-3-羧酸制备香豆素?
创新实验设计:微波辐射技术合成香豆素-3-羧酸乙酯
CHO+CH2(COOC2H5)2NMWOCOOC2H5将同学分组,安排学生查阅文献,选择传统加热和微波辐射技术方法,合成香豆素-3-羧酸乙酯,并比较两种方法之间的收率,熔点,产品纯度以及三废污染情况的差异,最终得出最佳合成工艺条件。
微波辐射(Microwave irradiation)方法具有较高的加热效率。将该技术应用于合成反应中,可以缩短反应时间、节约溶剂、提高收率、减少三废污染。近年来,微波辐射促进化学反应的研究受到了广泛关注,逐渐形成了一门新兴学科---微波化学。本创新实验在微波辐射作用下,采用水杨醛和丙二酸二乙酯反应,考察无溶剂或添加少量溶剂对香豆素-3-羧酸乙酯收率的影响,并与传统加热方法进行比较。
在圆底烧瓶中,加入水杨醛(5 g, 0.014 mol)、丙二酸二乙酯(6.8 ml, 0.045 mol)、无水乙醇(或不加)、六氢吡啶0.5 mL和2滴冰醋酸,充分摇匀后,将圆底烧瓶置于微波反应器中,装上回流冷凝管,用480 W微波辐射3~8 min。反应结束后,将反应物转移到烧杯中,加水30 mL,置于冰水浴中冷却,待析晶完全后,过滤,滤饼用2~3 mL50%冷乙醇洗涤2~3 33
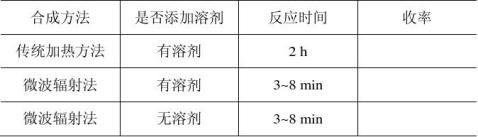
次。粗产品用25%的乙醇水溶液重结晶,干燥,称重,计算收率,测熔点。结果列表,并对实验结果进行分析。
表1 反应条件,反应时间及收率
34
实验六、苯佐卡因的合成
外科手术所必需的麻醉剂或称止痛剂,是一类已被研究透彻的药物。化学家在这方面充分显示了他们的才能,他们对天然药物古柯碱研究的结果最终以更理想的合成品来替代它们,这种合成品作用更强,且无副作用和危险性。
最早的局部麻醉药是从南美洲生长的古柯植物中提取的古柯碱或称可卡因,但具有容易成瘾和毒性大等缺点,在搞清楚了古柯碱的结构和药理作用之后,人们已合成和试验了数百种局部麻醉剂,苯佐卡因和普鲁卡因仅是其中的两种。已经发现的有活性的这类药物均有如下共同的结构特征:分子的一端是芳环,另一端则是仲胺或叔胺,两个结构单元之间相隔1-4个原子连结的中间链。苯环部分通常为芳香酸酯,它与麻醉剂在人体内的解毒有密切的关系;氨基还有助于使此类化合物形成溶于水的盐酸盐以制成注射液。
芳香族残基中间链
胺基3
H2NOOCOOCH3可卡因OCH2CH2NCH2CH32CH3普鲁卡因
35 H2NOCH2CH3苯佐卡因RAOO(CH2)nNBR1R2C局部麻醉剂的通式
本实验阐述了局部麻醉药苯佐卡因的制备,它是一种白色的晶体粉末,制成散剂或软膏用于疮面溃疡的止痛。
一、实验目的和要求
1.掌握文献查阅和局麻药苯佐卡因合成路线选择的基本原理和评价.
2.熟悉氧化、酯化、还原、酰化反应的原理和操作方法.
3.了解化合物的酸碱性进行纯化的方法.
二、实验原理
苯佐卡因通常有两条合成路线:方法一由对硝基甲苯首先被氧化成对硝基苯甲酸,再经乙酯化后还原而得。
CH3COOH[O]CHOH
H2SO4NO2NO2NO2NH2 COOC2H5[H]2H5
这是一条比较经济合理的路线。
方法二采用对甲苯胺为原料,经酰化、氧化、水解、酯化一系列反应制备苯佐卡因。
NH2NHCOCH3
(CHCO)O CHOH
H2SO4NH2COOC2H5 CH31 KMnO2 H, H2OCH3NH2
此路线虽然比方法一以对硝基甲苯为原料长一些,但原料易得,操作方便,适合于实验室小量制备。
两条路线均有大量文献报道。现将两种合成方法列出,根据同学查阅文献的情况和兴趣,自己确定合成方法。 36
三、实验内容(在文献检索的基础上,指导教师审核)
1.以对硝基甲苯为原料,经氧化、酯化、还原反应合成苯佐卡因.
2.以对氨基甲苯为原料,经酰化、氧化、酯化反应合成苯佐卡因.
四、实验仪器
三颈烧瓶、圆底烧瓶、干燥管、烧杯、锥形瓶、球形冷凝管、机械搅拌器、布氏漏斗、抽滤瓶.
苯佐卡因的制备(方法一)
一、对硝基苯甲酸的合成(氧化反应)
[试剂]
对硝基甲苯 (10 g m.p. 51~54℃)、重铬酸钾 (34 g)、浓硫酸 (40 mL)、5%硫酸 (40 mL)、5%NaOH (75 mL)、10%硫酸 (150 mL)、活性碳(适量)
[实验步骤]
在三颈烧瓶中加入对硝基甲苯(10 g,73 mmol)、重铬酸钾(34 g,0.115 mol)和水(65 mL),搅拌下小心滴加浓硫酸(40 mL),滴加过程中,控制反应体系内温度不超过60 ℃ ,必要时用水浴冷却之,当加入一半量硫酸后,注意控制温度,勿使反应过分剧烈。硫酸加毕后,升温至微沸,缓缓回流1 h,至反应液呈绿色,冷却到50 ℃ ,将反应液倒入烧杯中,加入冷水80 mL, 搅拌析出晶体,抽滤,用冷水(40 mL)分两次洗涤滤饼。
粗品对硝基苯甲酸为黄黑色,可将其置于5%的硫酸40 mL中,加 37
热10 min,以溶解铬酸,冷却,过滤,抽干,得晶体。再将晶体溶于温热的5%氢氧化钠溶液中,冷却,过滤(注1),滤液中加入约0.5 g的活性炭,温热至约 50 ℃,振摇或搅拌5-10 min后过滤。滤液冷却,搅拌下将滤液滴加到10%的硫酸(150 mL)中,冷却,析出晶体充分,过滤(注2),用冷水洗涤,干燥,计算收率,测定熔点(注3)。
[注]:
1. 这一步是除去未反应的对硝基甲苯和铬酸,将铬酸变成氢氧化铬后除去。
2. 硫酸不能反加到滤液中,否则生成的沉淀包含杂质,影响产物的纯度。
3. 必要时用水、乙醇、苯或冰醋酸重结晶。
二、对硝基苯甲酸乙酯的制备(酯化反应)
[试剂]
对硝基苯甲酸 (8 g)、浓硫酸 (9.6 g,5.3 mL)、95%乙醇 (20 mL)、5%的碳酸钠溶液
[实验步骤]
将95%的乙醇(20 mL)置于100 mL干燥的圆底烧瓶中,慢慢加入浓硫酸(5.3 mL),再加入对硝基苯甲酸(8 g),装上球形冷凝管,于85℃水浴中搅拌、回流1.5 h, 至对硝基苯甲酸固体消失(注1),瓶底有透明的油状物。反应完毕后,取下圆底烧瓶,在剧烈振摇下冷却(注2)析出晶体,然后倒入80 mL冷水中,搅拌,过滤,得滤液(I)。滤饼用水洗涤2次,然后置于5%的碳酸钠溶液中,使pH = 8左右,以溶去未 38
反应的对硝基苯甲酸,过滤,得到滤液(II),滤饼用水洗涤至中性,减压干燥,得对硝基苯甲酸乙酯,计算收率,测定熔点(本品熔点较低,注意干燥温度)。合并滤液(I),(II),用酸酸化,过滤,可以回收部分未反应的对硝基苯甲酸。
[注]:
1. 若沉淀没有完全溶解,说明酯化还未进行完全,可视情况酌量补加硫酸和乙醇再继续回流之。
2. 必须剧烈振摇,使油层乳化,这样冷却后析出的结晶颗粒细,以后用碳酸钠处理时易除去酸,否则会结块,用碳酸钠不易处理。
三、苯佐卡因的合成(还原反应)
[试剂]
对硝基苯甲酸乙酯 (8 g)、铁粉 (7.2 g)、醋酸 (1 g)、95%乙醇 (90 mL)、10%硫化钠溶液、活性碳 (0.1-0.2 g).
[实验步骤]
将铁粉7.2 g、水24 mL和醋酸1 g置于装有搅拌器和温度计的100 mL三颈烧瓶中,80℃ 搅拌15 min(注1),然后缓慢加入(注2)对硝基苯甲酸乙酯,于80℃剧烈搅拌(注3)三小时。冷却到40℃,过滤,滤饼用水洗涤至中性,将滤渣移入100 mL烧杯中,加乙醇分三次热提取(50 mL一次,20 mL二次),于70℃水浴上加热,搅拌5 min过滤,合并三次的滤液。加10%硫化钠溶液一滴,检查有无铁离子,若有,再加硫化钠溶液至不再有黑色沉淀产生为止(此时需过滤),加活性炭,加热 39
15 min脱色,趁热过滤,滤液浓缩至20 mL,冷却,析出晶体,过滤,用少量70%左右的稀醇洗涤,得白色结晶,必要时用稀醇进行重结晶(W:V = 1:5),本品的m.p. 91-92℃。用TLC检测纯度,计算收率。
[注]:
1. 先加热15 min的目的是使Fe活化,同时生成催化剂Fe(Ac)2。
2. 对硝基苯甲酸乙酯加入时反应放热,如加料速度快,则导致冲料。
3. 铁粉重,必须剧烈搅拌,才能使之不致沉积在烧瓶底部,使反应完全。
[思考题]
1. 用重铬酸盐氧化时,除生成对硝基苯甲酸外,可能还有哪些副产物存在,如何分离及充分利用?
2. 试述酯化反应的基本原理,指出做好酯化反应的关键在哪里?在纯化酯化产物时应注意哪些问题?
苯佐卡因的制备(方法二)
一、对氨基苯甲酸的合成
对氨基苯甲酸是一种与维生素B有关的化合物(又称PABA),它是维生素B10(叶酸)的组成部分。细菌把PABA作为组分之一合成叶酸,磺胺药则具有抑制这种合成的作用。
对氨基苯甲酸的合成涉及三个反应。第一步反应是将对甲苯胺用醋酸酐处理转化为相应的酰胺,这是一个制备酰胺的常用方法,其目的是在第二步用高锰酸钾氧化反应中保护氨基,避免氨基被氧化,形成的酰 40
胺在所采用的氧化条件下是稳定的。
第二步是将对甲基乙酰苯胺中的甲基被高锰酸钾氧化为羧基。氧化过程中,紫色的高锰酸钾被还原成棕色的二氧化锰沉淀。鉴于溶液中有氢氧根离子生成,故要加入少量的硫酸镁作缓冲剂,使溶液碱性变得不致太强而使酰胺基发生水解。反应产物是羧酸盐,经酸化后可使生成的羧酸从溶液中析出。
最后一步是酰胺水解,除去起保护作用的乙酰基,此反应在稀酸溶液中很容易进行。
[反应式]
NH2NHCOCH3
(CH3CO)2O
CH3COONa+
3
NHCOCH3
2KMnO4
COOK
3
+
2COOKCOOHNH2+ CH3COOH+ 2MnO2 + H2O + KOHCH3COOH CH3NHCOCH3+3
[试剂]
对甲苯胺 (7.5 g, 0.07 mol)、醋酸酐 (8.7 g, 8 mL, 0.085 mol)、醋酸钠(CH3COONa·3H2O) (12 g)、高锰酸钾 (20.5 g, 0.13 mol)、硫酸镁晶体(MgSO4·7H2O) (20 g,0.08 mol)、乙醇、盐酸、硫酸、氨水.
[实验步骤] 41
1. 对甲基乙酰苯胺的合成
在500 mL烧杯中,加入7.5 g对甲苯胺,175 mL水和7.5 mL浓盐酸,必要时在水浴上温热搅拌促使溶解。若溶液颜色较深,可加入适量的活性碳脱色后过滤。同时配置12 g三水合醋酸钠溶于20 mL水的溶液,必要时温热至所有的固体溶解。
将脱色后的盐酸对甲苯胺溶液加热至50℃,加入8 mL醋酸酐,并立即加入预先配制好的醋酸钠溶液,充分搅拌后将混合物置于冰浴中冷却,此时应析出对甲基乙酰苯胺的白色固体。抽滤,用少量冷水洗涤,干燥后称重,计算收率,测定熔点。对甲基乙酰苯胺纯品的熔点为154℃。
2. 对乙酰氨基苯甲酸的合成
在600 mL烧杯中,加入上述制得的对甲基乙酰苯胺(约7.5 g)、20 g七水合结晶硫酸镁和350 mL水,将混合物在水浴上加热到约85℃。同时制备20.5 g高锰酸钾溶于70 mL沸水的溶液。
在充分搅拌下,将热的高锰酸钾溶液在30 min内分批加入到对甲基乙酰苯胺的混合物中,以免氧化剂局部浓度过高破坏产物。加完后,继续在85℃搅拌15 min。
混合物变成深棕色,趁热用两层滤纸抽滤除去二氧化锰沉淀,并用少量热水洗涤二氧化锰。若滤液呈紫色,可加入2-3 mL乙醇煮沸直至紫色消失,将滤液再用滤纸过滤一次。
冷却无色滤液,加20%硫酸酸化至溶液呈酸性,此时应生成白色固体,抽滤,压干,干燥后得到对乙酰氨基苯甲酸。计算收率,测定熔点。纯品的熔点为250-252℃。湿品可直接进行下一步合成。
42
3. 对氨基苯甲酸的合成
称量上步得到的对乙酰氨基苯甲酸,将每克湿产物用5 mL18%的盐酸进行水解。将反应物置于250 mL圆底烧瓶中,在石棉网上用小火缓缓回流30 min。待反应物冷却后,加入30 mL冷水,然后用10%氨水中和,使反应混合物对石蕊试纸恰成碱性,切勿使氨水过量。每30 mL最终溶液加1 mL冰醋酸,充分振摇后置于冰水浴中骤冷以引发结晶,必要时用玻棒摩擦瓶壁或放入晶种引发结晶。抽滤收集产物,干燥后以对甲苯胺为标准计算累计产率,测定产物的熔点。纯品的熔点为186-187℃。实验得到的熔点略低一点(注1)。
[注释]
1. 对氨基苯甲酸不必重结晶,对产物重结晶的各种尝试均未获得满意的结果,产物可直接用于合成苯佐卡因。
[思考题]
1. 对甲苯胺用醋酸酐酰化反应中加入醋酸钠的目的何在?
2. 对甲乙酰苯胺用高锰酸钾氧化时,为何要加入硫酸镁结晶?
3. 在氧化步骤中,若滤液有色,需要加入少量乙醇煮沸,发生了什么反应?
4. 在最后水解步骤中,用氢氧化钠代替氨水中和可以吗?中和后加入醋酸的目的何在?
43
4. 对氨基苯甲酸乙酯(苯佐卡因)的合成
[反应式]
+ C2H5OH
NH2HSO COOC2H5+ H2ONH2
[试剂]
对氨基苯甲酸 (2 g, 0.0145 mol)、95%乙醇 (25 mL)、浓硫酸 (2 mL)、10%碳酸钠溶液、乙醚、无水硫酸镁.
[实验步骤]
在100 mL圆底烧瓶中,加入2 g对氨基苯甲酸和95%乙醇25 mL,旋转烧瓶使大部分固体溶解。将烧瓶置于冰水浴中冷却,加入2 mL浓硫酸,立即产生大量沉淀(在接下来的回流中沉淀将逐渐溶解),将反应混合物在水浴上搅拌、回流1 h。
将反应混合物转入烧杯中,冷却后分批加入10%碳酸钠溶液中和(约需12 mL),可观测到有气体逸出,并产生泡沫(发生了什么反应?),直至加入碳酸钠溶液后无明显气体释放。反应混合物接近中性时,检查溶液pH值,再加入少量碳酸钠溶液至pH值为9左右。在中和过程中产生少量固体沉淀(生成了什么物质?)。将溶液倾倒入分液漏斗中,并用少量乙醚洗涤固体后并入分液漏斗。向分液漏斗中加入40 mL乙醚萃取,振摇后分出醚层。经无水硫酸镁干燥后,在水浴上蒸出乙醚和大部分乙醇,至残留油状物约2 mL为止。残留物用乙醇-水重结晶,计算收率,测定熔点。
44
纯品的熔点为91-92℃。
[思考题]
1. 本实验中加入浓硫酸后,产生的沉淀是什么物质?试解释之。
2. 酯化反应结束后,为什么要用碳酸钠溶液而不用氢氧化钠溶液进行中和?为什么不中和至pH为7而要使溶液pH为9左右?
3. 如何由对氨基苯甲酸为原料合成普鲁卡因(procaine)?
45
实验七、阿魏酸哌嗪盐和阿魏酸川芎嗪盐的合成
我国中药资源丰富,从传统的中药中筛选出活性成分作为先导化合物,利用现代药物化学研究原理对先导化合物进行药物设计、合成,从中筛选出疗效更好、副作用少、生物利用度高的药物具有重要的理论意义和临床应用价值。川芎嗪(Ligustrazine,Lig)是川芎中主要活性成分,化学名为2, 3, 5, 6-四甲基吡嗪,简称四甲基吡嗪(Tetramethylpyrazine, TMP),现已人工合成。药理学研究表明,川芎嗪具有扩张血管、抑制血小板聚集、防止血栓形成、改善脑缺血等多种作用。川芎嗪衍生物的研究受到了人们的高度关注。阿魏酸是当归、川芎等传统活血化淤中草药的主要有效成分之一,现已人工合成。药理学研究表明,具有抑制血小板聚集、抑制5-羟色胺从血小板中释放、阻止静脉旁路血栓形成、抗动脉粥样硬化、抗氧化、增强免疫功能等作用。阿魏酸分子结构中含有羧基和酚羟基,具有较强的酸性。阿魏酸较难溶于冷水,可溶于热水、乙醇、乙酸乙酯,易溶于乙醚。为增加阿魏酸的溶解度,以便于注射给药,同时结合药物拼合原理,人们利用阿魏酸的酸性,将其与无机碱(如NaOH)、有机碱(如哌嗪、川芎嗪)等成盐,得到了阿魏酸钠、阿魏酸哌嗪、阿魏酸川芎嗪等盐类修饰物。其中阿魏酸钠在临床上主要用于动脉粥样硬化、冠心病、脑血管病、肾小球疾病、肺动脉高压、糖尿病性血管病变、脉管炎等血管性病症的辅助治疗;亦可用于偏头痛、血管性头痛的治疗。阿魏酸哌嗪适用于各类伴有镜下血尿和高凝状态的肾小球疾病的治疗,以及冠心病、脑梗死、脉管炎等疾病的辅助治疗。阿魏酸川芎嗪具有抗血小板聚集、扩张微血管、解除血管痉挛、改善微循环、活血化 46
淤作用;并对已聚集的血小板有解聚作用。
H3HO
阿魏酸
COOH
H3C
NN川芎嗪
CH3
CH3
哌嗪
HC
3
一、实验目的
1. 熟悉药物拼合原理及其应用。
2. 掌握中药有效成分的结构修饰原理及其在新药开发中应用。 3. 掌握阿魏酸哌嗪、阿魏酸川芎嗪的制备原理及操作方法。 二、实验内容
1. 阿魏酸哌嗪盐的合成。 2. 阿魏酸川芎嗪盐的合成。
3. 阿魏酸哌嗪盐和阿魏酸川芎嗪盐的精制。 三、实验原理
阿魏酸分子结构中含有羧基和酚羟基,具有较强的酸性。阿魏酸较难溶于冷水,可溶于热水、乙醇、乙酸乙酯,易溶于乙醚。为增加阿魏酸的溶解度,以便于注射给药,同时结合药物拼合原理,人们利用阿魏酸的酸性,将其与无机碱(如NaOH)、有机碱(如哌嗪、川芎嗪)等成盐,得到了阿魏酸钠、阿魏酸哌嗪、阿魏酸川芎嗪等盐类修饰物。
H3HO
COOH
H3C+
H3C
NN
CH


H3HO
COOH
2
H3HO
COOH
+HN
H3COHO
COOH
2H3CH3C
NN
33
47
四、实验设备、仪器
磁力搅拌器、100 mL圆底烧瓶、250 mL烧杯、布氏漏斗、抽滤瓶。 五、化学试剂
六水合哌嗪、盐酸川芎嗪、无水乙醇、阿魏酸、蒸馏水、活性碳、NaOH。
六、实验步骤
(一)、阿魏酸哌嗪盐的合成与精制 1. 投料比
化学试剂 分子量(FW) 投料量(g) 摩尔数(mol)
六水合哌嗪 194 1.94 0.01
阿魏酸 194 3.90 0.02
无水乙醇
60 mL
蒸馏水
活性碳 适量
2.操作步骤
在圆底烧瓶中加入阿魏酸 (3.9 g, 0.02 mol)、无水乙醇30 mL,加热溶解。在烧杯中加入六水合哌嗪 (1.94 g, 0.01 mol), 加乙醇10 mL,加热溶解备用。在搅拌下将哌嗪乙醇溶液趁热加到阿魏酸乙醇溶液中,水浴温度控制在60℃左右,再搅拌1 h,冷却,过滤,滤饼用无水乙醇洗涤。干燥得阿魏酸哌嗪盐白色针状晶体4 g左右,收率约为75%。m.p. 157-160℃。
(二)、阿魏酸川芎嗪盐的合成与精制 1.投料比
化学试剂 分子量(FW) 投料量(g) 摩尔数(mol)
川芎嗪 136 1.36 0.01
阿魏酸 194 3.90 0.02
无水乙醇
60 mL
蒸馏水
活性碳 适量
2.操作步骤
在圆底烧瓶中加入阿魏酸 (3.9 g, 0.02 mol)、无水乙醇30 mL,加热
48
溶解。在烧杯中加入川芎嗪 (1.36 g, 0.01 mol), 加乙醇7 mL,加热溶解备用。在搅拌下将川芎嗪乙醇溶液趁热加到阿魏酸乙醇溶液中,水浴温度控制在60℃左右,再搅拌1 h,冷却,过滤,滤饼用无水乙醇洗涤。用25%乙醇重结晶,干燥得阿魏酸川芎嗪盐白色针状晶体4 g左右,计算收率。m.p. 168-170℃。
[思考题]
1. 阿魏酸哌嗪盐和阿魏酸川芎嗪盐的设计原理是什么?
2. 请思考阿魏酸哌嗪盐和阿魏酸川芎嗪盐的含量测定方法。
3. 增加难溶性药物的吸收,有那些方法?
49
附录一:生产工艺中避免使用和限制使用的溶剂
药物的合成和精制均涉及到溶剂的使用,尤其是合成工艺最后几步反应和精制工艺中所使用的溶媒会影响原料药的质量,为了保障药物的质量和用药安全,以及保护环境,需要对残留溶剂进行控制。根据ICH(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceutical for Human Use)关于溶剂残留量指导原则(19xx年12月27日生效)的规定,结合美国药典(the United States Pharmacopoeia, USP)、英国药典(British Pharmacopoeia, BP)、欧洲药典(European Pharmacopoeia, EP)的相关内容,我国于20xx年3月颁布了化学药物残留溶剂研究的技术指导原则[(H)GPH7-1]。根据中国药典和化学药物残留溶剂研究的技术指导原则对残留溶剂的规定,在生产工艺中应避免使用的溶剂有苯、四氯化碳等5种,详见表2-1;应限制使用的溶剂有乙腈、氯仿等27种,详见表2-2。
表2-1 生产中避免使用的溶剂
溶剂
苯 四氯化碳 1,2-二氯乙烷 1,1-二氯乙烯 1,1,1-三氯乙烷
限制浓度(%)
0.0002 0.0004 0.0005 0.0008 0.15
影响 致癌
毒性并影响环境
毒性 毒性 有害环境
表2-2 生产中限制使用的溶剂
溶剂 乙腈 氯苯 三氯甲烷 环己烷 1,2-二氯乙烯 二氯甲烷 1,2-二甲氧基乙烷
限制浓度(%)
0.041 0.036 0.006 0.388 0.187 0.06 0.01 溶剂 甲醇 2-甲氧基乙醇 甲基丁基酮 甲基环己烷 N-甲基吡咯烷酮
硝基甲烷 吡啶
50
限制浓度(%)
0.3 0.005 0.005 0.118 0.053 0.005 0.02
N,N-二甲基乙酰胺 N,N-二甲基甲酰胺
二氧六环 2-乙氧基乙醇 乙二醇 甲酰胺 正己烷
*
0.109 0.088 0.038 0.016 0.062 0.022 0.029
四氢噻吩 四氢化萘 四氢呋喃 甲苯
1,1,2-三氯乙烯 二甲苯* 0.016 0.01 0.072 0.089 0.008 0.217
通常含有60%间二甲苯、14%对二甲苯、9%邻二甲苯和17%乙苯
在生产工艺中应尽量避免使用表1-1所列出的溶剂,如果一定要用,就要严格控制,且在成品中要做残留量的检查。尤其在成品精制工艺中更应慎重选择重结晶溶剂。
51
附录二:部分与药物化学相关的文献来源
*ACS数据库(http:)中与药物化学或合成有关的杂志:
1. Journal of medicinal chemistry (J. Med. Chem).
2. Journal of organic chemistry (J. Org. Chem).
3. Journal of American Chemistry (J. Am. Chem. Soc).
4. Organic Letters (Org. Lett).
5. Organic process research & development (Org. Process. Res. Dev).
6. Journal of Natural products (J. Nat. Prod).
*ELSEVIER数据库(http:)中与药物化学或合成有关的杂志.
1. Bioorganic & medicinal chemistry (Bioorg. Med. Chem).
2. Bioorganic & medicinal chemistry Letters (Bioorg. Med. Chem. Lett).
3. Bioorganic Chemistry (Bioorg. Chem).
4. European journal of medicinal chemistry (Eur. J. Med. Chem).
5. Tetrahedron
6. Tetrahedron letters (Tetrahedron. Lett).
7. Tetrahedron: Asymmetry (Tetrahedron: Asym).
*John Wiley(http:www3.)数据库中与与药物化学或合成有关的杂志.
1. Angewandte chemie international edition (Angew. Chem., Int. Ed).
2. European journal of organic chemistry (Eur. J. Org. Chem).
*RSC () 数据库中与与药物化学或合成有关的杂志.
52
1. Chemical communication.
2. Green Chemistry
3. New Journal of Chemistry
4. Organic & Biomolecular Chemistry
*Thieme-connect or synthsis)数据库中与药物化学或合成有关的杂志.
1. Synthesis
2. Synlett
*Taylor & Francis---synthetic communications (synthetic commun) *Science Links Japan (http://sciencelinks.jp/j-east) 数据库中与药物化学或合成有关的杂志.
1. Chemical pharmaceutical Bulletin (Chem pharm bull).
2. Antibiotics & Chemotherapy
*万方数据、维普中文科技期刊、CNKI中国期刊全文数据库中部分与药物化学或合成有关的杂志.
1. 中国药物化学杂志.
2. 药学学报.
3. 中国药科大学学报
4. 沈阳药科大学学报
53
5. 有机化学
6. 化学学报
7. 高等学校化学学报
8. 中国医药工业杂志
9. 化学试剂
10. 化学世界
11. 中国化学(英文 Chinese Journal of Chemistry)
12. 中国化学快报(英文 Chinese Chemistry Letters)
13. 合成化学
14. 中国新药杂志
15. 中国现代应用药学杂志
16. 中国药学杂志
部分与药物化学或合成有关的专利检索网址
http://www. 部分与药物化学或合成有关的文献检索工具
SciFinder connecting to CAS… (CA的在线检索系统) CA(Chemical Abstract) (有纸质手工检索和光盘检索) 贝尔斯坦/盖墨林(Beilstein/Gmelin)
54
-
药化实验报告模板
药物化学实验报告模板实验室间20xx年10月28日天气晴温度2225扑炎痛的合成一实验原理二主要试剂及仪器原料名称阿司匹林氯化亚砜…
-
药物化学实验报告
北京广播电视大学医药分校北京广播电视大学药物化学实验报告姓名高振峰学号1311001456929组别A组成绩实验名称阿司匹林乙酰水…
-
药 物 化 学 实 验
药物化学实验王瑞孙铁民沈阳药科大学药物化学教研室20xx年9月1前言药物化学实验是依据药物化学教学大纲的要求编定目的是通过实验加深…
-
药物化学实验报告
北京广播电视大学医药分校北京广播电视大学药物化学实验报告姓名学号组别20xx秋药学班成绩实验名称阿司匹林乙酰水杨酸的合成实验时间2…
-
药物化学实验报告
药物化学实验报告的要求一目的要求二反应式照片中的反应式与SA制备分离的基本原理三原料试剂主要物理常数图五实验操作现象记录每页纸分成…
-
区域地质调查总结
一、基本内容1.区调是一项基础性、公益性、具有战略意义的综合性基本地质工作,是所有地质工作的先行步骤和地质科学不断发展的基础。2.…
-
消防安全教育工作总结
比中小学比中小学学校消防安全工作是学校综合治理的重要内容,关系到学校财产安全和教师员工的生命安全。对于这项工作,在学校的统一部署下…
-
第二课堂总结报告
20xx-20xx学年秋季学期电14班第二课堂活动总结本次素拓活动以“规划生活,践行人生”为主题展开访谈与实践相结合的活动,共历时…
-
军医年终总结
军医年终工作总结本人在院工作近一年,后定在外科工作,在科室领导关心及科室同志的帮助下,很好的完成了各项工作任务,使自己较快的熟悉新…
-
爱国卫生运动半年总结
永乐镇爱国卫生运动半年总结为进一步推动我镇爱国卫生运动,巩固创建“市级卫生城镇”阶段性成果,打造整洁、卫生、舒适的城镇环境,保障全…