《北京市医疗器械经营企业检查验收标准》
北京市医疗器械经营企业检查验收标准
北京市药品监督管理局关于印发《北京市医疗器械经营企业检查验收标准》的公告
发布时间:20##-02-01
《北京市医疗器械经营企业检查验收标准》已经于20##年12月12日第15次局务会审议通过,现予以印发,20##年2月1日起实施。原《北京市医疗器械经营企业检查验收标准》(试行)(京药监市〔2005〕22号)同时停止执行。
特此公告。
附件:北京市医疗器械经营企业检查验收标准
二〇##年十二月十五日
《北京市医疗器械经营企业检查验收标准》
总则:
一、根据《医疗器械监督管理条例》和《医疗器械经营企业许可证管理办法》制定本标准。
二、北京市行政区域内《医疗器械经营企业许可证》的核发、换证、变更和监督管理工作适用于本标准。
三、本标准根据《医疗器械分类目录》(国药监械[2002]302号),结合北京市医疗器械经营企业实际情况,将医疗器械产品划分以下类别:
A类:Ⅲ-6846植入材料和人工器官、Ⅲ-6877介入器材;
B类:Ⅲ-6821医用电子仪器设备、Ⅲ-6822医用光学器具、仪器及内窥镜设备、Ⅲ-6845体外循环及血液处理设备、Ⅲ-6854手术室、急救室、诊疗室设备及器具;
C类:Ⅲ-6815注射穿刺器械、Ⅲ-6863口腔科材料、Ⅲ-6864医用卫生材料及敷料、Ⅲ-6865医用缝合材料及粘合剂、Ⅲ-6866医用高分子材料及制品;
D类:Ⅲ-6822医用光学器具、仪器及内窥镜设备(软性、硬性角膜接触镜及护理用液);
E类:Ⅱ-6846植入材料和人工器官(助听器);
F类:除上述类外的其它类代号医疗器械。
四、经营医疗器械的门店及药品零售企业申请“Ⅲ-6815注射穿刺器械、Ⅲ-6866医用高分子材料及制品”经营范围的按本标准F类专用部分要求验收。
申请 “Ⅲ-6822医用光学器具、仪器及内窥镜设备” 经营范围的非验配类企业按B类专用部分要求验收;申请“Ⅱ-6846植入材料和人工器官”经营范围的非验配类企业按F类专用部分要求验收。
五、本标准分为通用部分和专用部分,企业应符合本标准通用部分要求和申请特定经营范围所涉及的专用部分要求。检查验收时,现场验收结果全部符合本标准的,评定为验收合格,有不符合本标准的,评定为验收不合格。
六、经营体外诊断试剂及国家食品药品监督管理局另有规定的医疗器械产品的经营企业验收标准从其规定。
七、本标准由北京市药品监督管理局负责解释。

第二篇:北京市医疗器械经营企业检查验收标准
北京市医疗器械经营企业检查验收标准
(试行)
一、根据国家食品药品监督管理局《医疗器械经营企业许可证管理办法》以及《北京市实施〈医疗器械经营企业许可证管理办法〉暂行规定》,制定本标准。
二、本标准适用于北京市行政区域内《医疗器械经营企业许可证》的发证、换证、变更和监督管理工作。
三、根据国家食品药品监督管理局20xx年发布的《医疗器械分类目录》,将医疗器械产品划分以下类别。
(一)器械类: 6801、6802、6803、6804、6805、6806、6807、6808、6809、6810、6812、6813、6816、6820、6827。
(二)设备、器具类: 6821(Ⅱ类)、6822(Ⅱ类)6823、6824、6825、6826、、6831、6834、6840、6841、6845、6854、6855、6856、6857、6858。
(三)大型医用设备类: 6824、6825、6828、6830、6832、6833。
(四)植入、介入及人工器官类: 6821(Ⅲ类)、6822(Ⅲ类)6846、6877。
(五)医用材料类: 6863、6864、6865、6866(6866-1除外)。
(六)诊断试剂类。
(七)一次性无菌类: 6815、6866。
(八)软件类:6870。
(九)验配类: 角膜接触镜、助听器。
四、 经营一次性无菌及国家食品药品监督管理局另有规定的医疗器械产品从其规定。
五、 同为一个法定代表人的两个及两个以上医疗器械经营企业实行统一电子化管理、统一采购、配送并统一质量管理标准的可集中设置仓库,仓库总面积与各企业合计经营规模相适应。
六、 现场验收时,应根据企业经营医疗器械的范围确定合理缺项并逐项进行检查,现场验收结果全部符合本标准的,评定为验收合格,有不符合本标准的,评定为验收不合格。
七、 现场检查时,应按以下表格内项目进行:
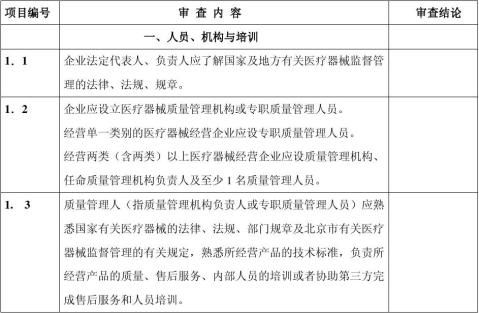
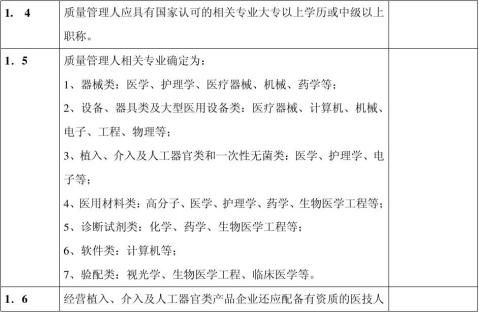
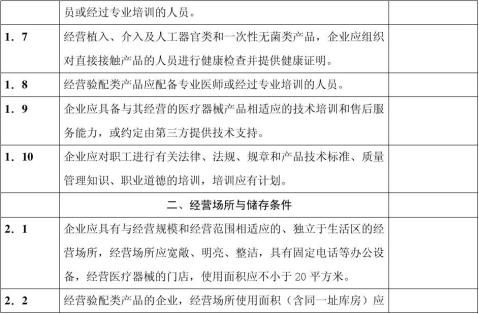
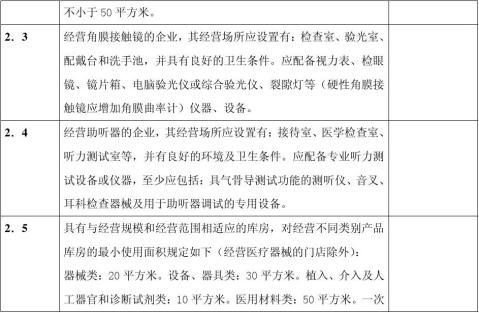
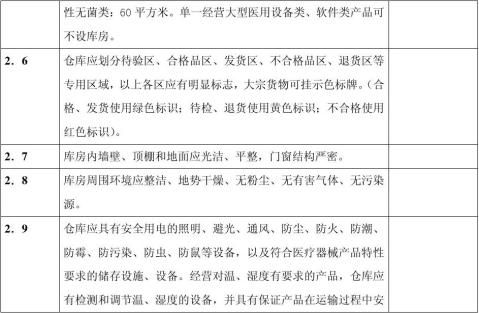
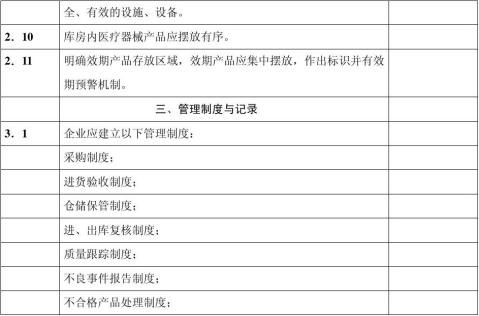
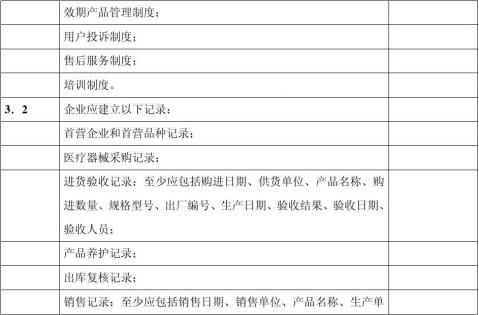

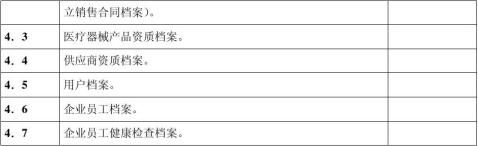
-
医疗器械经营企业自查报告
医疗器械经营企业自查报告企业名称富阳毛源昌眼镜店盖章主要经营产品种类或名称医疗器械第类软性角膜接触镜及护理用液的另售企业负责人杨淑…
-
医疗器械经营企业20xx年度自查报告
附件1第三类医疗器械批发企业企业名称盖章企业地址隶属区局企业负责人手机联系人电话手机年度基本情况表填报单位填报时间年度自查情况表填…
-
第三类医疗器械经营企业质量管理的自查报告
第三类医疗器械经营企业质量管理自查报告一企业基本信息二自查结论填表人签章日期填表说明1企业基本信息中电话可多填销售方向包括零售批发…
-
20xx年度医疗器械经营企业年度自查报告(非常实用的模板)
20xx年度医疗器械经营企业年度自查报告企业名称XXXX医药或医疗器械有限公司经营范围第三类注射穿刺器械6815医用电子仪器设备6…
-
医疗器械经营企业自查报告1
医疗器械经营企业自查报告企业名称宁夏源丰医药有限公司盖章企业地址银川市兴庆区丽景街东侧宁夏新世纪冷链物流中心6号楼04号商业房企业…
-
医疗器械注册产品分析报告
XXXXXX产品质量跟踪报告一试产期间产品的生产销售情况1试产期间XXXXX产品生产的批次为X数量为XXX2试产期间XXXXX产品…
-
医疗器械检验机构注册检验报告统一格式
附件1医疗器械检验机构注册检验报告统一格式封面检验报告报告编号委托方样品名称型号检验类别注册检验注册补充检验其他检验国家食品药品监…
-
医疗器械经营企业现场检查整改报告
关于医疗器械经营企业许可验收现场检查缺陷项目整改情况的报告天津市食品药品监督管理局20xx年5月29日天津市食品药品监督管理局现场…
-
医疗器械产品检测报告认可须知
医疗器械产品检测报告认可申请须知一依据1医疗器械注册管理办法20xx年8月9日国家食品药品监督管理局令第16号公布第十三条申请第二…
-
湖南省医疗器械经营企业检查验收标准企业自查报告
湖南省医疗器械经营企业检查验收标准企业自查报告衡阳市食品药品监督管理局我公司根据湖南省食品药品监督管理局的有关规定认真的组织医疗器…