化学实验预习报告
化学实验预习报告
班级 小组成员
实验名称:海带中碘元素的分离及提存(检验)
一、实验目的:
二、实验原理:
1、查资料知海带中碘元素主要为I-形式存在, 少量以有机碘和IO3- 存在。
2、可使用某些 剂(如 )将I-转化为I2,然后检验I2的存在,并分离I2,有关反应的离子方程式为(任写一条):
3、可使用 溶液检验I2,用 萃取并 方法分离出I2。
三、实验步骤:

实验几个注意之处
1、海带已经称取好
2、灼烧灰化的过程大约需要5—6分钟,干海带逐渐变成黑色粉末或细小颗粒即可
3、用坩埚钳夹持坩埚,边加热边用玻璃棒搅拌,以使海带充分灼烧,加快灰化的速度。
4、移动坩埚时必须使用坩埚钳,避免烫伤
5、灼烧完毕,应将坩埚、玻璃棒放在石棉网上冷却,不可直接放在冷的实验台上,防止温度很高的坩埚骤冷而破裂
6、过滤操作应注意“一贴、二低、三靠”
7、用约1mL蒸馏水洗涤沉淀得滤液
8、使用分液漏斗之前应先检漏和洗涤
9、萃取后打开上口的塞子或将旋塞的凹槽对准上口的小孔,静置,待完全分层后,分液。
第二篇:工程化学实验报告册
工程化学实验报告册
班级
学号
姓名
实验一 水的纯化与水质检验
班级 姓名 学号 日期
一、实验目的
二、数据记录与处理
1、电导率的测定

2、水中主要离子的鉴定(记录现象)

结论:
3、自来水中碱度离子的检验
实验现象记录:
结论:
4、水中Ca2+、Mg2+离子总量的测定
EDTA标准溶液的浓度: (mol/l)
水样(自来水)的体积V水样: (ml)
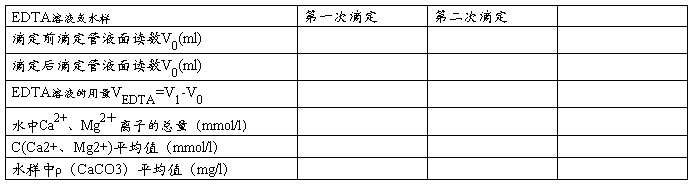
三、讨论
四、思考题
在实验中,为什么取水样时必须用移液管,而取缓冲溶液和蒸馏水时,则可以量筒取?
实验二 配合物的制备和性质
班级 姓名 学号 日期
一、实验目的:
二、实验步骤:
1.配合物的制备
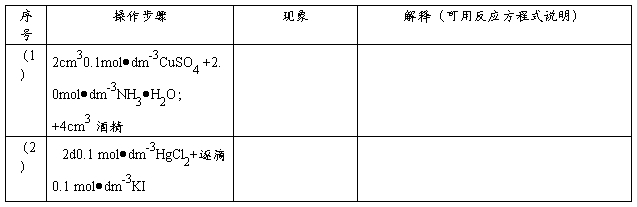
2.配离子的离解平衡及其稳定性
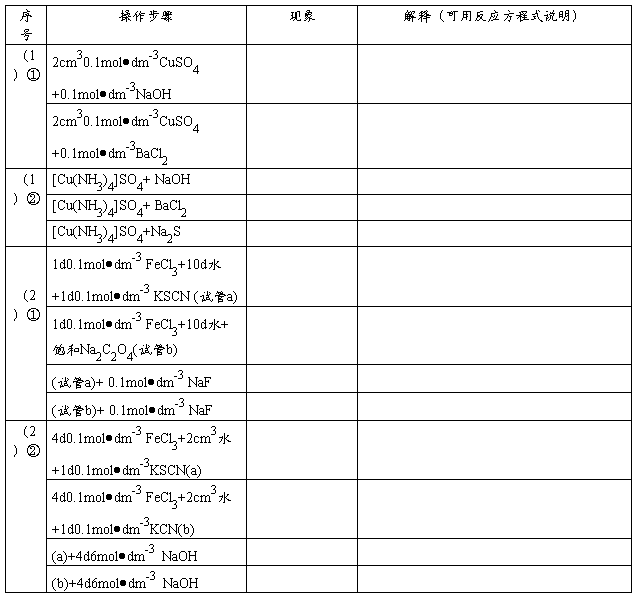
结论:
3.配离子离解平衡的移动

4..螯合物的形成
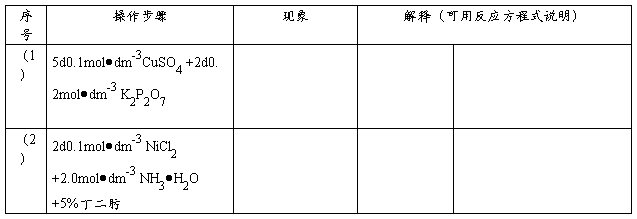
三、讨论:
四、思考题
结合本实验举例说明哪些因素影响配离子的离解平衡?
实验三 电 化 学
班级 姓名 学号 日期
一、实验目的
二、数据记录及处理
1、EDTA标准溶液的浓度
(1)Sn2+—Fe3+原电池符号:
原电池的正极反应:
负极反应:
(2)NaCl溶液的电解
本实验电解NaCl溶液
阳极(铜丝)反应:
阴极(铜丝)反应;
解释阴极出现酚酞显色的现象:
2、浓度和介质对电极电位的影响
(1)离子浓度与电极电位的关系
原电池 (—)Zn︱ZnSO4(c1)‖CuSO4(c2)︱Cu(+)
未加氨水时原电池的电动势:E=
Cu2+\Cu极加氨水时电动势的变化情况:
Zn2+\Zn极加氨水时电动势的变化情况:
依据能斯特方程式解释实验结果
(2) 溶液介质对电极电势的影响
原电池 (—)Zn︱ZnSO4(c1)‖K2Cr2O7(c2),Cr3+(c3),H+(c4)︱C(+)
未加酸碱时原电池的电动势:E=
Cu2+\Cu极加氨水时电动势的变化情况:
Zn2+\Zn极加氨水时电动势的变化情况:
依据能斯特方程式解释实验结果
3、分解电压的测定

作图:分解电压-电流曲线
根据曲线及反应现象。可知水的分解电压为
电解池的阴极反应:
阳极反应:
4、金属腐蚀的防止
(1)缓释剂法:
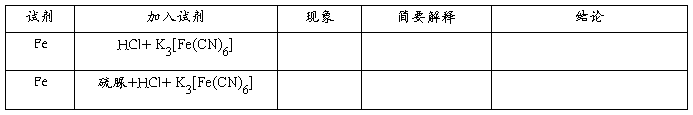
(2)阴极保护法:
在在阳极附近滴入2~3滴0.1 mol·dm-3K3[Fe(CN)6]溶液,现象
阴极发生的反应:
阳极发生的反应:
三、思考题
两极铜丝电解NaCl溶液时,阴阳两极各发生什么反应,为什么发生这些反应?
实验四 邻二氮菲分光光度法测铁
班级 姓名 学号 日期
一、 实验目的
二、 实验数据记录
1、邻菲罗林-铁吸收曲线上的最大吸收波长A= nm。
2、标准曲线的绘制
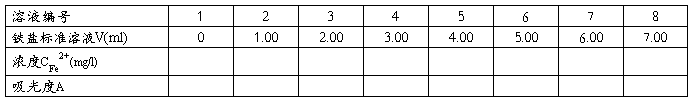
贴图处
3、水中总铁量的测定
(1)在分光光度计上测得水样的吸光度A水样=
(2)根据A水样标准曲线的斜率、截距求得:
水样中铁的浓度(即铁总量): (mg/l)
三、 讨论
四、思考题
在水处理时,为什么要首先加HCl较长时间的煮沸?其中加盐酸羟胺,起到什么作用?
-
无机化学预习实验报告
无机化学预习实验报告实验名称室温气压年级组姓名实验室指导教师日期实验目的实验原理实验试剂及产物物理常数实验步骤实验结果注意事项指导…
-
生物化学实验预习及实验报告范例
目录预习报告示范2实验还原糖和总糖的测定2实验二Fehling试剂直接热滴定定糖法2实验报告示范15实验还原糖和总糖的测定15实验…
-
化学实验预习报告
工科化学实验预习报告实验题目三草酸合铁酸钾的制备实验目的1熟悉络合物的基本知识2掌握合成K3FeC2O433H2O的基本原理和操作…
-
有机化学实验预习报告(示例)
南昌大学预习实验报告示例实验项目名称阿司匹林的制备及物理常数测定一实验目的二实验基本原理或主副反应式五实验装置图用铅笔画1反应装置…
-
有机化学实验预习报告模板
有机化学专业实验预习报告模板带气体吸收的回流装置分液蒸馏装置及操作四主要仪器及装置如回流装置加热套100mL圆底单口烧瓶球形冷凝管…
-
化学实验报告格式
化学实验报告格式例一定量分析实验报告格式(以草酸中h2c2o4含量的测定为例)实验题目:草酸中h2c2o4含量的测定实验目的:学习…
-
化学实验报告格式示例
化学实验报告格式示例例一定量分析实验报告格式(以草酸中H2C2O4含量的测定为例)实验题目:草酸中H2C2O4含量的测定实验目的:…
-
基础化学实验报告格式
院系年级专业姓名学号课程名称基础化学实验实验日期年月日实验地点指导老师测定实验例二氧化碳相对分子质量的测定实验报告院系年级专业姓名…
-
化学实验报告格式
提示1每一次实验前要求写预习报告否则不能做没有预习的实验2每次实验前交上一次实验的实验报告和预习报告预习报告夹在实验报告中交上来3…
-
初中化学探究性实验学习问卷调查报告
初中化学探究性实验学习问卷调查报告初中化学探究性实验学习问卷调查报告大泉源乡中学张宏伟化学是一门以实验为基础的科学实验在化学教学中…
-
化学实验研究报告
?化学实验研究报告我们初三学习了一个学期的化学,从中学到了很多有趣的知识,初步学会了用简单的仪器和药品进行实验的方法,同时也对化学…