大黄中蒽醌类成分的提取、分离和鉴定(实验报告)
大黄中蒽醌类成分的提取、分离和鉴定
一、 实验目的
(1)熟悉蒽醌类成分的提取分离方法
(2)掌握pH梯度提取法的原理和操作技术
(3)学习蒽醌类化合物鉴定方法
二、 实验器材
材料及试剂:大黄粗粉、浓硫酸、NaHCO3、Na2CO3、NaOH、浓盐酸、乙酸乙酯、石油醚、乙醚、普通滤纸、薄层层析硅胶板(2.5 cm×10 cm)、广泛PH试纸、剪刀、铅笔、尺子、点样毛细管、样品管等。
仪器:500mL圆底烧瓶、球形冷凝管(30cm)、橡皮管、烧杯、滴管、层析缸(广口瓶)、250mL分液漏斗、布氏漏斗、抽滤瓶、水浴锅、集热式磁力搅拌器、磁子、循环水式多用真空泵、铁架台等。
三、 实验原理
大黄为蓼科植物,味苦,性寒,具有泻热通肠、凉血解毒、逐瘀通经等功效。其主要成分为为蒽醌化合物,含量约为3%~5%,大部分与葡萄糖结合苷,游离苷元有大黄酸、大黄素、芦荟大黄素、大黄酚、大黄素甲醚等。其中,大黄酸具有羧基,酸性最强;大黄素具有β-酚羟基,酸性第二;芦荟大黄素连有羟甲基,酸性第三;大黄素甲醚和和大黄酚的酸性最弱。根据以上化合物的酸度差异,可用碱性强弱不同的溶液进行梯度萃取分离。

大黄酸 R1=H R2=COOH
大黄素 R1=CH3 R2=OH
芦荟大黄素 R1=CH2OH R2=H
大黄素甲醚 R1=CH3 R2=OCH3
大黄酚 R1=CH3 R2=H
四、 实验内容
大黄素的提取、分离流程图
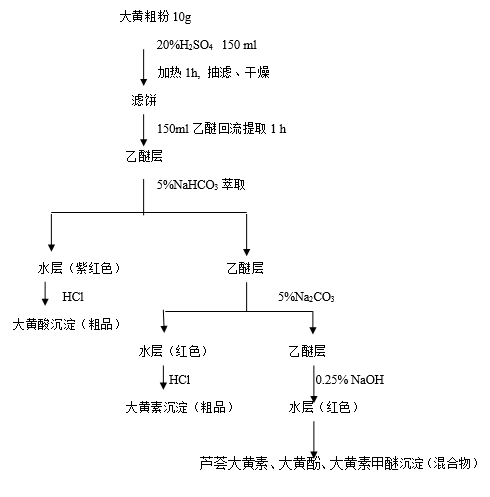
具体操作步骤
1. 游离蒽醌的提取
(1)酸水解:称取大黄粗粉10g,加20%H2SO4水溶液150mL,在水浴上加热1小时,放冷,抽滤,滤饼用NaOH溶液洗至近中性(pH约为6),于70℃干燥后,研碎,置250mL圆底烧瓶中,加入乙醚150mL回流提取1小时(调45℃,回流即可),得到乙醚提取液。
(2)蒽醌类成分的提取:乙醚提取液经薄层层析检查有大黄酸、芦荟大黄素、大黄素、大黄素甲醚和大黄酚。薄层板为硅胶—CMC粘合板,展开剂为石油醚(60~90℃):乙酸乙酯(7:3)近水平或直立展开,在可见光下,可看到四个斑点。其中最上面黄色斑点为大黄酚和大黄素甲醚的混合物,在此条件下,不能分开,其余3个斑点依Rf值(由大到小)的顺序是大黄素(橙色斑点)、芦荟大黄素(黄色斑点)、大黄酸(黄色斑点),记录图谱并计算Rf值。
2. PH梯度萃取分离
(1)将乙醚提取液加入250mL分液漏斗中(使用前先检漏),以35 mL 5 % NaHCO3水溶液萃取三次,乙醚层经薄层层析检查(展开剂同上),指示已提尽大黄酸后,合并三次NaHCO3萃取液,用浓盐酸酸化至PH 2-3左右,析出大黄酸沉淀。(注意:加酸时应缓慢加入,以防酸液溢出,如出现分层现象,需将上层乙醚蒸去才能析出固体)。抽滤后,刮下颗粒并称重。
(2)经5% NaHCO3水溶液萃取后的乙醚层,继以35 mL 5 % Na2CO3水溶液萃取三次,乙醚层经薄层检查(展开剂同上),指示已提尽大黄素后,合并三次Na2CO3萃取液,用浓盐酸酸化至PH2-3左右,析出大黄素沉淀。(酸化时注意操作同前)。抽滤后,刮下颗粒并称重。
(3)经5% Na2CO3水溶液萃取过后乙醚层以35 mL 0.25% NaOH水溶液萃取四次,乙醚层经薄层检查(展开剂同上),指示已提尽后,合并三次 NaOH萃取液,用浓盐酸酸化至PH2-3左右,析出芦荟大黄素、大黄酚和大黄素甲醚沉淀混合物。(酸化时注意操作同前)。抽滤后,刮下颗粒并称重。
3. 样品鉴定
(1) 碱液试验 分别取各蒽醌结晶数毫克置于样品管中,加2%氢氧化钠溶液1ml,观察颜色变化。凡有互为邻位或对位羟基的蒽醌呈蓝紫至蓝色,其它羟基蒽醌呈红色。
五、 注意事项:
(1)游离蒽醌的提取要控制温度,回流不宜太剧烈。
(2)pH梯度萃取分离时,以保证提取充分,可以用薄层色谱作监测。
(3)注意碱液浓度及萃取时的静置时间对实验结果的影响。
六、 数据记录、结果讨论与分析:


分别取各上述沉淀(蒽醌结晶)数毫克置于样品管中,加2%氢氧化钠溶液1ml后,观察到各样品管中溶液均呈红色、但第1根管中颜色略淡。
七、 思考题
1、 简述大黄中5种游离羟基蒽醌化合物的酸性与结构的关系。
答:

A大黄酸 R1=H R2=COOH
B大黄素 R1=CH3 R2=OH
C芦荟大黄素 R1=CH2OH R2=H
D大黄素甲醚 R1=CH3 R2=OCH3
E大黄酚 R1=CH3 R2=H
酸性:A>B>C>E≈D
2.pH梯度萃取法的原理是什么?如何利用该方法分离大黄中的5种游离羟基蒽醌化合物?
答:pH梯度萃取法的原理是由于溶剂系统pH变化而改变了它们的存在状态(游离型或解离型),从而改变了他们在溶剂系统中的分配系数。
由于各羟基蒽醌结构上的不同所表现的酸性不同,用pH梯度萃取法分离他们;大黄酚和大黄素甲醚酸性相近,利用其极性的差异,用柱色谱分离之。
3.结合本实验,思考设计实验方案所需因素?
答:游离蒽醌的提取要控制温度,回流不宜太剧烈。要注意碱液浓度及萃取时的静置时间对实验结果的影响。
八、 参考文献
(1) 吴立军主编,《天然药物化学实验指导》北京;人民卫生出版社,2011
(2)康廷国主编,《中成药薄层色谱鉴别》.北京:人民出版社,1995
(3)徐选明,刘新 大黄中大黄素提取工艺的优化 中国中医药信息杂志 2004,11,5
(4)李乃明,丁宙 大黄素的分离和结构鉴定 广州医学院学报 1985,13,3
(5)朱庆玲,李瑞和 大黄中大黄素的提取工艺研究 时珍国医国药 2006,17,3
第二篇:大黄中游离蒽醌的提取与分离和鉴定
实验一 大黄中游离蒽醌的提取与分离和鉴定 实验编号:1
日期:
学时数: 6学时
地点:
任课教师:
实验目的:掌握从大黄中提取和分离游离蒽醌的方法
实验原理:大黄中有多种游离蒽醌及其苷类,总含量约2-5%。主要有大黄酸、大黄素、大黄酚、芦荟大黄素、大黄素甲醚以及它们的葡萄糖苷等。从大黄中提取分离游离蒽醌时,先用20%硫酸加热使苷类水解,保留滤饼,滤饼用乙醚加热回流提取总蒽醌苷元(游离蒽醌),提取液作TLC鉴识。 实验对象:大黄
主要仪器、试剂:电热套、烧杯、20%硫酸、薄层硅胶G 、0.5%CMC-Na。 实验操作步骤: 酸水解:取大黄10g ,粉碎,加20%硫酸水溶液100ml,水浴上加热3-4小时,抽滤,滤饼水洗后自然干燥。
铺薄层硅胶G板: 薄层硅胶G :0.5%CMC-Na(1:3)
实验注意事项: ①加热温度不要太高。 ②溶液保持微沸,防止药渣炭化。 ③不断搅拌。
后记:
实验一 大黄中游离蒽醌的提取与分离和鉴定
实验编号:2
日期:
学时数: 6学时
地点:
任课教师:
实验目的:1.掌握从大黄中提取和分离游离蒽醌的方法。
2.掌握蒽醌类的色谱鉴别方法。
实验原理:大黄中有多种游离蒽醌及其苷类,总含量约2-5%。主要有大黄酸、大黄素、大黄酚、芦荟大黄素、大黄素甲醚以及它们的葡萄糖苷等。从大黄中提取分离游离蒽醌时,先用20%硫酸加热使苷类水解,保留滤饼,滤饼用乙醚加热回流提取总蒽醌苷元(游离蒽醌),提取液作TLC鉴识。 实验对象:大黄滤饼
主要仪器、试剂:电热套、圆底烧瓶、冷凝管、乙醚、硅胶薄层板、石油醚、乙酸乙酯
实验操作步骤: 总羟基蒽醌苷元的提取:取干燥滤饼,放入100ml圆底烧瓶中,加入乙醚50ml,回流提取3-4小时,得乙醚提取液。
乙醚提取液经薄层层析检查有大黄酸、芦荟大黄素、大黄素、大黄素甲醚和大黄酚。薄层板为硅胶G-CMC-Na,展开剂为石油醚(60-90℃)-乙酸乙酯(7:3),直立展开。
实验注意事项: ①加热回流时电热套电压小于50v。
②取石油醚(60-90℃)7ml,乙酸乙酯3ml,混合均匀。。 ③控制点样量,
注意点样斑点位置。④仔细观察斑点、溶剂前沿移动距离。
后记:结论:在可见光下可看到4个斑点,Rf最大的黄色斑点为大黄酚和大黄素甲醚的混合物,其余3个斑点依Rf由大到小分别为大黄素(橙色斑点),芦荟大黄素(黄色斑点),大黄酸(黄色斑点
实验二 芦丁的提取及鉴定
实验编号:1
日期:
学时数: 8学时
地点: 新校区F楼6楼天然药物化学实验室
任课教师:
实验目的:学习和掌握用碱提取—酸沉淀提取黄酮苷的原理和方法。 实验原理:槐米中有黄酮苷—芸香苷(芦丁), 芸香苷(芦丁)是由槲皮素与芸香糖连接而成的二糖苷,能溶于热水。本试验采用碱提取—酸沉淀提取芸香苷。
实验对象: 槐米
主要仪器、试剂:电热套、烧杯、石灰水、PH试纸、抽滤瓶 。 实验操作步骤: 1.提取:槐花米—粉碎—碱水提取—加酸沉淀-—放置—粗品芦丁—精制—芦丁(纯品)。
2.粉碎:称槐米40克,粉碎。
3.碱提:在1000ml烧杯中加入500ml蒸馏水,加热煮沸后,将槐米粗粉投入,继续直火 煮沸2-3分钟,在搅拌下,加入石灰乳,调PH8-9,加热保持微沸30分钟,趁热过滤收集,滤渣加160ml蒸馏水, 加入石灰乳,调PH8-9,同上操作再提一次,滤液合并,滤渣弃去。
4.酸沉:将滤液在60-70℃,小心加浓HCL,调PH3-4,放6小时以上,析出沉淀。
实验注意事项: ①碱提时加入石灰乳调PH8-9,不要太高。
②溶液保持微沸。
③酸化时将滤液在60-70℃,小心加浓HCL,调PH3-4,不要太低。 后记:
实验二 芦丁的提取及鉴定(精制)
实验编号:2
日期:
学时数: 8学时
地点:新校区F楼6楼天然药物化学实验室
任课教师:
实验目的:粗品芦丁的精制
实验原理: 粗品芦丁能溶于热水,去除不溶性杂质,最后用甲醇重结晶。
实验对象: 粗品芦丁
主要仪器、试剂:电热套、圆底烧瓶、冷凝管、甲醇
实验操作步骤: 精制 :粗品芦丁放在1000ml烧杯中,加500ml蒸馏水,加热煮沸,至全部溶解,趁热抽滤,滤液放冷,即析出黄色沉淀,待沉淀完全后,抽滤,收集沉淀,干燥。用甲醇重结晶,得精品芦丁。 实验注意事项: (1)用甲醇重结晶时加热回流时电热套电压小于50v。
(2)粗品芦丁全部溶解,趁热抽滤。
(3)重结晶时甲醇的用量应适当,用量过多,则结晶不易析出;用量过少,又会带入较多的杂质。
后记:
实验二 芦丁的提取及鉴定
实验编号:3
日期:
学时数: 8学时
地点:新校区F楼6楼天然药物化学实验室
任课教师:
实验目的:(1)芦丁的水解,鉴定;
(2)掌握黄酮类成分的主要性质及黄酮苷、苷元和糖的鉴定方法。
实验原理: ,
实验对象: 精品芦丁
主要仪器、试剂:电热套、圆底烧瓶、冷凝管、甲醇、正丁醇、醋酸、葡萄糖、鼠李糖、盐酸、镁粉、醋酸镁、醋酸铅、氧氯化锆、三氯化铝
实验操作步骤: 1.水解 :取1克芦丁加1%H2SO4100ml与烧杯中,加热微沸,30分钟,开始为澄清,逐渐析出黄色针状结晶,待沉淀完全后,抽滤,收集沉淀,水解母液留作糖的纸层析鉴定。
2. 芦丁、槲皮素的鉴定:
(1)糖的检出——圆形滤纸层析
取水解芦丁的滤液20ml,加Ba(OH)2细粉中和至pH7,滤除生成的BaSO4白色沉淀,滤液在水浴上小心浓缩近干(约1ml)注意防止炭化,加甲醇5ml,作为检识糖的样品溶液。
展开剂:正丁醇-醋酸-水(4-1-5上层)。
对照品:葡萄糖、鼠李糖(各2mg,分别溶于2ml甲醇中) 展开方式:径向展开
显色剂:苯胺邻苯二甲酸盐试剂(或,邻苯甲酸苯胺),喷雾后,105℃加热3~5分钟,有糖处显棕色或棕红色斑点。
(2)化学方法鉴别黄酮类成分
a.盐酸-镁粉反应
b.醋酸镁反应
c.醋酸铅沉淀反应
d.氧氯化锆
e.点滴反应
实验注意事项: ①糖的检出——圆形滤纸层析点样量不要太多。
后记:
实验三 氧化苦参碱的提取分离与纯制
实验编号:1
实验日期:
实验地点:
任课教师:
学时数:2+8
实验目的:掌握渗漉法和离子交换法提取生物碱的方法和原理
实验原理:1.生物碱溶于酸水
2.阳离子交换树脂提取、分离生物碱
实验对象:苦参
主要仪器、试剂:渗漉筒、烧杯、玻璃棒
阳离子交换树脂柱、阳离子交换树脂、pH试纸、培养皿 0.5%盐酸、碘化铋钾、蒸馏水
主要操作步骤:
总碱的提取:
(1)酸水提取:称取250g风干粉碎的苦参中加入适量0.5%的盐酸液,使其浸没药料,充分湿润,放置一小时。将如上酸水浸泡好的药材及溶液装入渗漉筒,待全部加完,继续补充加入0.5%的盐酸液,浸过药面,放置过夜(此步骤在实验前一天提前完成)。
继续加入0.5%的盐酸液或蒸馏水,(当渗漉液的酸性过大,改加蒸馏水渗漉,将渗漉液的pH控制在3-4之间)以1mL/min的流速进行渗漉,收集渗漉液约3750Ml,到渗漉液生物碱反应微弱为止。
(2)交换:将上述渗漉液pH控制在3-4之间,上柱交换,流速自快至慢,流出液要经常以碘化铋钾检查,如发现有未被交换的生物碱流下时,可调整流速继续进行交换,待渗漉液全部通过树脂后,把树脂倒入烧杯中,用蒸馏水洗涤数次,除去非阳离子杂质,然后滤干,放入大培养皿中自然干燥。
实验注意事项:
装渗漉筒时,药材应压实,尽赶空气,渗漉筒切勿走干。
当渗漉液的酸性过大,改加蒸馏水渗漉,将渗漉液的pH控制在3-4之间。 如发现有未被交换的生物碱流下时,可调整流速继续进行交换。
离子交换树脂柱切勿走干。
后记:(教学体会、学生对教学内容的反应等)
实验二 氧化苦参碱的提取分离与纯制
实验编号:2
实验日期:
学时数: 8
实验地点:
任课教师:
实验目的:学习索氏提取器的使用方法
实验原理:1.生物碱碱化后,溶于氯仿
2.索氏提取器氯仿连续提取将生物碱从阳离子交换树脂上洗脱下来 实验对象:交换了生物碱的阳离子交换树脂
主要仪器、试剂:索氏提取器、烧杯、水浴锅
阳离子交换树脂、圆底烧瓶、冷凝管、漏斗、滤纸 浓氨水、氯仿、丙酮
主要操作步骤:
总碱的提取:
(1) 总碱洗脱:
将晾干后的树脂放入烧杯中,加浓氨水20mL,充分搅匀,使湿润度合适,(树脂充分膨胀,但又无不吸收的过剩水份溢出)盖好, 静置20分钟后,装入索氏提取器中,用300mL氯仿在水浴上回流洗脱,至提尽生物碱为止。回收氯仿,尽力抽干。残剩物用2-3倍量丙酮溶解,尽快出现结晶,放置一定时间,过滤,得氧化苦参碱粗晶,(实际是总碱)用丙酮重结晶一次,得精品。
实验注意事项:
加浓氨水20mL,充分搅匀,使湿润度合适,使树脂充分膨胀,但又无不吸收的过剩水份溢出。
索氏提取器使用时要小心,易碎裂。
后记:(教学体会、学生对教学内容的反应等)
实验二 氧化苦参碱的提取分离与纯制
实验编号:3
实验日期:
学时数: 8
实验地点:
任课教师:
实验目的:学习使用Al2O3薄层、柱层析法分离鉴定生物碱的方法
实验原理:生物碱可以采用Al2O3薄层、柱层析法分离
实验对象:总碱粗品,Al2O3薄层,Al2O3柱层析
主要仪器、试剂:层析柱、棉花、点滴板、试管、玻璃板、毛细管、 Al2O3、碘化铋钾、圆底烧瓶、冷凝管、漏斗、滤纸
甲醇、氯仿、丙酮
主要操作步骤:
氧化苦参碱的分离与纯制:
取一根洗净干燥的1:45的层离柱,在下端塞一点棉花,倒入一些氯仿,使棉花湿润,并放出氯仿液,以赶尽气泡后,缓缓加入30g氧化铝,以氯仿作媒介湿法装柱,最后加入拌有200mg氧化苦参碱精品,薄层检查两个点的少量氧化铝,再放入一点棉花,先用30mL氯仿,后用氯仿:甲醇(99:1)的混合溶剂洗脱,流速控制1mL/min,流分每10 mL收集一份,收集中要经常以点滴板做生物碱显色反应的检查,薄层检识后,相同流分合并,回收溶剂至干,得氧化苦参碱部分用少量丙酮溶解,放置析晶,所得纯品为氧化苦参碱,测mp,并进行薄层检识。
苦参生物碱的薄层层析:
样品:氧化苦参碱标准品,粗品,柱层析中任一流份
展开剂:氯仿:甲醇 19:1或19.5:0.5
显色剂:改良碘化铋钾
实验注意事项:
湿法装柱要尽量赶尽气泡
氯仿:甲醇(99:1)的混合溶剂洗脱,流速控制1mL/min,不能过快。流分每10 mL收集一份,薄层检识后,相同流分再合并。
后记:(教学体会、学生对教学内容的反应等)
-
实验报告设计 叶绿体中色素的提取和分离
叶绿体中色素的提取和分离一实验目标1知识方面1探究叶绿体中含有几种种色素理解它们的特点及与光合作用的关系2了解纸层析法的原理2能力…
-
叶绿体色素的提取分离实验报告
叶绿体色素的提取分离理化性质实验报告第一部分提取与分离一实验目的学习应用薄层色谱法分离叶绿体色素的实验方法二实验原理叶绿体是进行光…
-
绿叶中色素的提取和分离的实验报告
绿叶中色素的提取和分离的实验报告一实验目的1学会提取和分离叶绿体中色素的方法2比较观察叶绿体中四种色素理解它们的特点及与光合作用的…
-
9实验报告绿叶中色素的提取和分离
实验报告九绿叶中色素的提取和分离实验目的1进行绿叶中色素的提取和分离2探究绿叶中含有几种色素材料用具菠菜绿叶干燥的定性滤纸试管棉塞…
-
《叶绿体色素的提取和分离》 实验报告
叶绿体色素的提取和分离实验报告实验目的1学习叶绿体色素的提取分离方法2通过叶绿体色素提取分离方法的学习了解叶绿体色素的相关理化性质…
-
肉桂油提取分析实验报告
XX大学化学化工学院本科学生综合性设计性实验报告实验课程化学工程与工艺专业实验实验项目植物性香料肉桂油的提取与分析专业化学工程与工…
-
中药化学成分提取分离技术 实验报告格式
中药化学成分提取分离技术实验报告女贞子化学成分提取分离技术专业年级学号姓名药剂学20xx级M20xx75250孙雨一研究背景女贞子…
-
蒸馏、萃取实验报告单
蒸馏萃取实验报告单姓名班级一实验室制取蒸馏水1蒸馏是利用物质沸点的不同加热使液体混合物中的液体变为气体挥发出来再冷凝为液体除去难挥…
-
蒸馏、萃取实验报告单
实验报告单姓名班级一实验室制取蒸馏水1蒸馏是利用物质的不同加热使液体混合物中的液体变为气体挥发出来再冷凝为液体除去难挥发或不挥发杂…
-
植物中天然香料的提取及香料成分分析实验报告
广州大学化学化工学院本科学生综合性设计性实验报告实验课程化工专业实验实验项目植物中天然香料的提取及香料成分分析专业化学工程与工艺班…
- 柱色谱分离实验报告