10银纳米粒子制备实验报告
开放实验总结报告
学生姓名 班级 学号
所在院系 专业
开放实验室名称:
218-218,221实验室
日期2011.12
一、实验项目概况
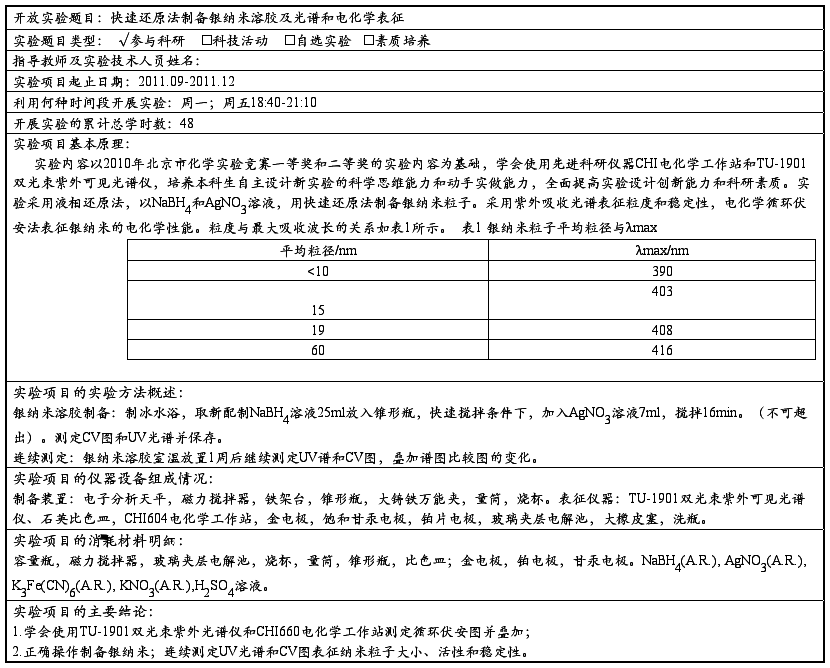
二、实验项目技术报告
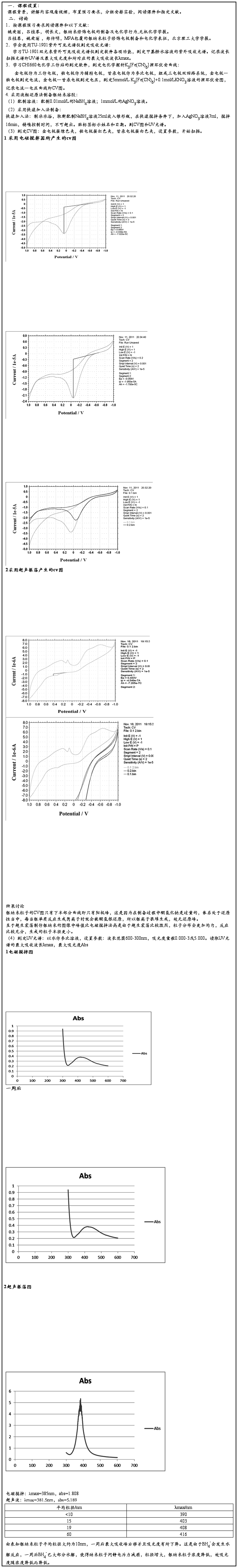
三、实验的体会与建议

四、评价与认定

第二篇:银纳米粒子的合成和表征实验报告
银纳米粒子的合成和表征
一、实验目的
1、学会还原法制备银纳米粒子的方法;
2、熟练掌握TU-1901紫外分光光度仪测量吸收光谱;
3、锻炼实验操作能力以及根据实验现象分析原理,独立思考能力。
二、实验原理
1、化学还原法制备纳米银:
2KBH4+2AgNO3+6H2O→2Ag+2KNO3+2H3BO3+7H2↑
(反应开始后BH4-由于水解而大量消耗:BH4-+H++2H2O→中间体→HBO2+4H2↑)
还原法制得的纳米银颗粒杂质含量相对较高,而且由于相互间表面作用能较大,生成的银微粒之间易团聚,所以制得的银粒径一般较大,分布很宽。
2、TU-1902双光束紫外可见分光光度仪
测量原理:由于银纳米粒子的粒度不同,对于不同波长的光有不同程度的吸收,根据其吸收特性,即最大吸收峰对应的波长,可以判断粒子的大小。
银纳米粒子平均粒径与λmax:

三、实验仪器与试剂
仪器:电子分析天平、磁力搅拌器、量筒(5mL)、烧杯(一大一小)、移液管(5mL)、容量瓶(50mL)、比色管(50mL)、TU-1902双光束紫外可见光谱仪、滴管、洗瓶、洗耳球、手套等。
药品试剂:1mmol/L AgNO3溶液、KBH4(固体)、蒸馏水、冰块等。
四、实验步骤、实验现象及数据处理
1、配制1.5mmol/L KBH4溶液
(1)减量法称取0.04gKBH4固体于小烧杯中,少量蒸馏水溶解,转移至50mL容量瓶中,用蒸馏水洗涤并将洗液转移至容量瓶中(重复3次),用蒸馏水定容至刻度线,摇匀。得15mmol/L KBH4溶液。
(2)用移液管移取上述溶液5mL至50mL比色管,用蒸馏水定容至刻度线,摇匀。得1.5mmol/L KBH4溶液。
实验数据:m(KBH4)=22.6177g-22.5792g=0.0385g
c1(KBH4)=m/(MV)=0.0385g/(53.94g/mol×50mL)=14.3mmol/L
c(KBH4)=c1V1/V2=(14.3mmol/L×5mL)/50mL=1.43mmol/L
2、制备纳米银:
量筒移取15mL1.5mmol/L KBH4溶液于烧杯中,放入磁子,在冰浴、搅拌条件下,逐滴加入2.5mL1mmol/LAgNO3溶液,继续搅拌15min。
现象:开始滴加AgNO3后溶液变黄,之后颜色逐渐加深,一段时间后变成黄棕色。
3、银纳米粒子的表征
(1)测量银纳米粒子的吸收曲线:
光谱测量 → 设置测量参数 → 基线测量(蒸馏水) → 样品测量 → 导出数据(得表1):

由上表,绘制银纳米粒子吸收曲线:

由上图可确定最大吸收波长λmax=395nm,并由此初步判断实验所得银粒子大小约为10~15nm。
(2)绘制稀释倍数与吸光度曲线
移液管分别移取2mL、2.5mL、5mL银纳米粒子溶液于3支10mL比色管中,用蒸馏水稀释定容至刻度线,摇匀。分别测其吸光度并记录,得表2。

由上表,绘制稀释倍数与吸光度曲线,得:
五、实验总结
本次实验中各操作较为准确和熟练,但是所得到的结果并不是很好,溶液的颜色较深,而且最后的稀释倍数和吸光度曲线并非直线。分析其原因,可能为:
1、滴加AgNO3溶液时速度太快,且总量(2.5mL)相对较多,生成的银纳米颗粒密度较大,由于布朗运动发生一定的聚沉现象,故使得所得溶液颜色较深。
2、搅拌速率有些慢。搅拌速率太慢时,银纳米颗粒运动速率较慢,也会使生成的银纳米颗粒发生一定的聚沉。
3、实验室仪器不足,当我们制备好银纳米溶液要测量吸光度时,排了很久的队才轮到我们测,测量的时候所制得的银纳米溶液已变色(稀释倍数不同,颜色变化也不同)了。
4、绘制稀释倍数与吸光度曲线时,样品总数太少,且每一个稀释倍数的溶液只测一次,导致误差较大。
-
甲基橙的制备 有机化学实验报告
实验学专班姓指导日机化学实验报告名称甲基橙的制备业化学工程与工艺级名学号教师房江华李颖期有一实验目的1通过甲基橙的制备学习重氮化反…
-
甲基橙的制备实验报告
实验学专班姓指导日机化学实验报告名称院化学工程学院业化学工程与工艺级化工xx班名xxx学号xxx教师期有一实验目的1通过甲基橙的制…
-
甲基橙的制备实验报告(4)沈杰
实验学专班姓指导日机化学实验报告名称院化学工程学院业化学工程与工艺级化工114班名沈杰学号114020xx417教师肖勋文何炎军期…
- 甲基橙实验报告
-
甲基橙实验报告
有机化学实验报告实验名称学院专业班级姓名学号指导教师日期实验目的1通过甲基橙的制备学习重氮化反应和偶合反应的实验操作2巩固盐析和重…
-
无水乙醇的制备实验报告
化学工程学院实验专班姓日指导机化学实验报告名称无水乙醇的制备业化学工程与工艺级化工136班名白慧超学号134020xx636期20…