实验五:电导率的测定及其应用
 宁 波 工 程 学 院
宁 波 工 程 学 院
物理化学实验报告
专业班级 化本092 姓名周培 实验日期 2011年4月14日
同组姓名 徐浩,郑志浩 指导老师 刘旭峰,王婷婷
实验名称 实验五、电导的测定及其应用
一、实验目的
1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。
2、用电导法测量醋酸在水溶液中的解离平衡常数。
3、掌握恒温水槽及电导率仪的使用方法。
二、实验原理
1、电解质溶液的电导率、摩尔电导率
①电导率
对于电解质溶液,常用电导G表示其导电能力的大小。电导G是电阻R的倒数,
电导的单位是西门子,常用S表示。
G =κA /l
κ为该溶液的电导率 l/A = Kcell,称为电导池常数。
其意义是电极面积为及1m2、电极间距为lm的立方体导体的电导,单位为S·m-1。
Kcell可通过测定已知电导率的电解质溶液的电导而求得。然后把欲测溶液放入该电导池测出
其电导值G,再得出κ
②摩尔电导率Λm
Λm=κ/ C
C为溶液浓度,单位mol.m-3
2、当溶液的浓度逐渐降低时,由于溶液中离子间的相互作用力减弱,所以摩尔电导
率逐渐增大。柯尔劳施根据实验得出强电解质稀溶液的摩尔电导率Λm与浓度有如下
关系:
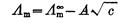
Λ∞m为无限稀释时的极限摩尔电导率 ,A视为常数可见,以Λm对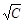 作图得一直线,其截距即为Λ∞m。
作图得一直线,其截距即为Λ∞m。
3、弱电解质溶液中,只有已电离部分才能承担传递电量的任务。在无限稀释的溶液中可认为弱电解质已全部电离。此时溶液的摩尔电导率为Λ∞m,可用离子极限摩尔电导率相加求得。
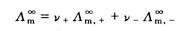
在弱电解质稀溶液中。离子的浓度很低,离子间的相互作用可以忽视,因此在浓度C时的解离度α等于他的摩尔电导率Λm与其极限摩尔电导率之比,即:
α=Λm/Λ∞m
对于HAc,在溶液中电离达到平衡时,电离平衡常数Kc与原始浓度C和解离度α有以下关系:
HAc====H+ + Ac-
t=0 C 0 0
t=t平衡 C(1-α) Cα Cα
K⊙=cα/c⊙(1-α)
在一点温度下K⊙是常数,因此可以通过测定Hac在不同浓度时的α代入上式求出K。
α=Λm/Λ∞m代入上式中得出:
K⊙=cΛm2/ [c⊙Λ∞m(Λ∞m-Λm)]
或者 cΛm=(Λ∞m)2 K⊙ c⊙(1/Λm )- Λ∞m K⊙c⊙
以cΛm对1/Λm作图,其直线斜率为(Λ∞m)2 K⊙ c⊙,因此可算出K⊙。
三、实验仪器、试剂
仪器:梅特勒326电导率仪1台、量杯(50ml)2只、移液管(25ml)3只、洗瓶1只、洗耳球1只
试剂:10.00(mol/m-3)KCl溶液、100.0(mol/m-3)HAc溶液、电导水
四、实验步骤
1、打开电导率仪开关,预热5min。
2、KCl溶液电导率的测定:
①用移液管准确移入10.00(mol/m-3)KCl溶液25.00ml。置于洁净,干燥的量杯中。测其电导率3次,去平均值。
②再用移液管准确移入25.00ml电导水,置于上述量杯中。搅拌均匀后,测其电导率3次,
取其平均值。
③用移液管准确移出25.00ml上述量杯中的溶液,弃去。再用移液管准确移入25.00ml点导水,置于上述量杯中。搅拌均匀后,测其电导率3次,取其平均值。
④重复③的步骤。
⑤重复③的步骤。
⑥倾去电导池中的KCl溶液,用电导水洗净量杯和电极。量杯放回烘箱,电极用滤纸吸干。
3、HAc溶液和电导水的电导率测定
①用移液管准确移入100.0(mol/m-3)HAc溶液25.00ml。置于洁净,干燥的量杯中。测其电导率3次,去平均值。
②再用移液管准确移入25.00ml已恒温的电导水,置于上述量杯中。搅拌均匀后,测其电
导率3次,取其平均值。
③用移液管准确移出25.00ml上述量杯中的溶液,弃去。再用移液管准确移入25.00ml电导水
置于上述量杯中。搅拌均匀后,测其电导率3次,取其平均值。
④再用移液管准确移入25.00ml电导水,置于上述量杯中。搅拌均匀后,测其电导率3次,
取其平均值。
⑤倾去电导池中的HAc溶液,用电导水洗净量杯和电极。然后注入电导水,测定电导水的电
导率3次,去平均值。
⑥倾去电导池中的电导水,量杯放回烘箱,电极用滤纸吸干。
五、数据记录与处理
室温: 24.7 ℃ 大气压: 100.24 Kpa 实验温度 23.8 ℃
已知数据:25℃下10.00(mol/m-3)KCl溶液电导率=0.4113S.m-1; 25℃下无限稀释的Hac水溶液的摩尔电导率=3.907*10-2S.m2.mol-1
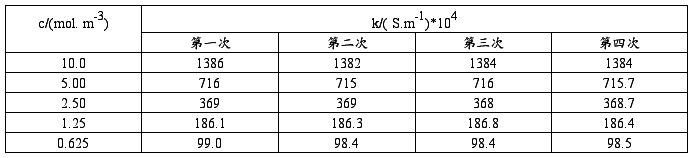
⑴测定KCl溶液的电导率
⑵测定HAc溶液的电导率
电导水的电导率k( H2O)/( S.m-1): 9.30*10-4 S.m-1
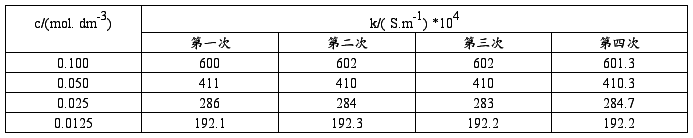
2、数据处理
⑴将KCl溶液的各组数据填入下表内:
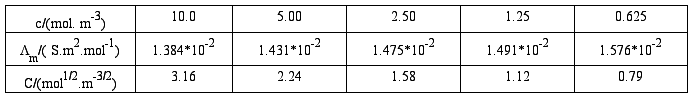
以KCl溶液的Λm对√c作图,

由图得该直线的斜率(1.475*10-2 -1.431*10-2)/(1.58-2.24)=-6.667*10-4 截距c=0.01537
因此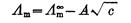 方程得出,KCl的Λ∞m=c=0.01537S.m2.mol-1
方程得出,KCl的Λ∞m=c=0.01537S.m2.mol-1
⑵HAc溶液的各组数据填入下表内:
HAc原始浓度:0.093 mol.dm-3
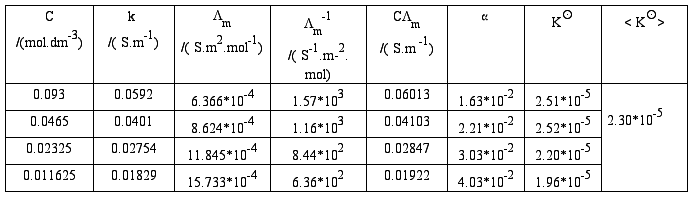
κ=κ′-κH2O
以CΛm对1/Λm作图得:
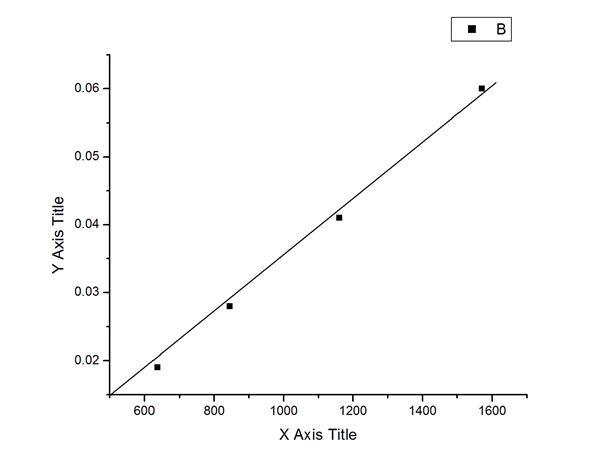 由图得出该直线的斜率k=(0.02847-0.01922) /(1.16*103-8.44*102)=2.93*10-5截距c=0.0148
由图得出该直线的斜率k=(0.02847-0.01922) /(1.16*103-8.44*102)=2.93*10-5截距c=0.0148
因此由cΛm=(Λ∞m)2 K⊙c⊙(1/Λm ) - Λ∞m K⊙c⊙方程得出
K⊙=k/(Λ∞m)2 c⊙=2.93*10-5/[(3.907*10-2)2*1000]=1.92*10-5
误差为(2.30*10-5-1.92*10-5)/2.30*10-5=0.1652
六、结果讨论
一、误差产生原因可能是配制溶液时浓度不是很准确,有点误差,还有就是操作过程中的误差。
主要误差原因:
1、溶液配制时的问题:溶液时由大浓度向小浓度一瓶一瓶稀释过来的。一旦某一瓶配制出现偏差,则将影响到后面的几瓶,因此在溶液配制的时候要及其小心,我认为这也是影响实验准确性的一个很重要的因素。
2、浓度较小时,信号不明显,即某个电阻改变一个大阻值,其示波器的变化不大,可能会导致大的偏差。
二、结果与讨论
1、电解质溶液导电主要与电解质的性质,溶剂的性质,测量环境的温度有关,所以测电导时要恒温。而电导池常数是一个不随温度变化的物理量,因此可以直接在不同的温度下使用。
2、电解质的摩尔电导率随浓度增加而降低,原因是:对强电解质而言,溶液浓度降低,摩尔电导率增大,这是因为随着溶液浓度的降低,离子间引力变小,粒子运动速度增加,故摩尔电导率增大。对弱电解质而言,溶液浓度降低时,摩尔电导率也增加。在溶液极稀时,随着溶液浓度的降低,摩尔电导率急剧增加
第二篇:实验五 电导的测定及其应用
 宁 波 工 程 学 院
宁 波 工 程 学 院
物理化学实验报告
专业班级 姓 名 序 号
同组姓名 指导老师 实验日期 2012.3.27
实验名称 实验五 电导的测定及其应用
一、实验目的
1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率;
2、用电导法测量醋酸在水溶液中的解离平衡常数;
3、掌握恒水温水槽及电导率仪的使用方法。
二、实验原理
1、电解质溶液的导电能力通常用电导G来表示,若将电解质溶液放入两平行电极之间,设电极的面积为A,两电极的间的距离为l,则溶液的电导G为:
G = к(A / l) (1)
式中к为改溶液的电导率,其单位是S.m-1;l/A为电导池常数,以Kcell来表示,它的单位为m-1。
由于电极的l和A不易精确测量,因此在实验中用一种已知电导率的溶液先求出电导池的常数Kcell,然后再把欲测的的溶液放入该电导池中测出其电导值,在根据上式求出其电导率。
在讨论电解质溶液的电导能力时常用摩尔电导率(Λm)这个物理量。摩尔电导率与电导率的关系:
Λm=K/C (2)
式中,C为该溶液的浓度,单位为mol.m-3;Λm的单位为S.m2.mol-1。
注意,当浓度C的单位是mol/L表示时,则要换算成mol/m3,后再计算。
2、Λm总是随着溶液的浓度的降低而增大的。对强电解质稀溶液而言,其变化规律可以用科尔劳施经验公式表示:
Λm=Λ∞m -A√C (3)
式中,Λm是溶液在无限稀释时的极限摩尔电导率。对特定的电解质和溶剂来说,在一定温度下,是一个常数。所以,将Λm对√C作图得到的直线外推至C=0处,可求得。
3、对于弱电解质溶液来说,其Λm无法利用上式通过实验直接测定。但是,在弱电解质的稀薄溶液中,离子的浓度很低,离子的浓度很低,离子间的相互作用可以忽略,也可以认为它在C浓度时的解离度等于它的摩尔电导率Λm与其无限稀释摩尔电导率之比,即:
α=Λm/Λ∞m (4)
对于HAc,在溶液中电离达到平衡时,电离平衡常数Kc与原始浓度C和电离度α有以下关系:
HAc H+ + Ac-
t=0 C 0 0
t=t平衡 C(1-α) Cα Cα
K0= Cα2/[C0(1-α)] (5)
在一定温度下K0是常数,因此可以通过测定HAc在不同浓度时的代入(5)式中求出Kc。
综合可得出关系:
K0= CΛ2m/ [C0Λ∞m(Λ∞m-Λm)]
或CΛm=(Λ∞m)2K0 C0(1/Λm)-Λ∞m K0 C0
以CΛm对1/Λm作图,其直线的斜率为(Λ∞m)2K0 C0,如知道Λ∞m值,就可算出K0。
三、实验仪器、试剂
仪器:梅特勒326电导率仪1台,电导电极1台,量杯(50ml)2只,移液管(25ml)3只,洗瓶1只,洗耳球1只。
试剂:10.00(mol·m-3)KCl溶液,100.0(mol·m-3)HAc溶液,电导水。
四、实验仪器装置图
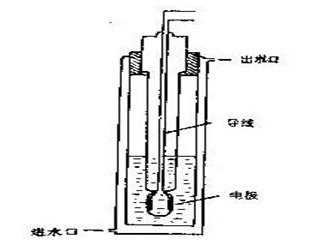
四、实验步骤
1、打开电导率仪开关,预热5min。
2、KCl溶液电导率测定:
⑴用移液管准确移取10.00(mol·m-3)KCl溶液25.00 ml于洁净、干燥的量杯中,测定其电导率3次,取平均值。
⑵再用移液管准确移取25.00 ml电导水,置于上述量杯中;搅拌均匀后,测定其电导率3次,取平均值。
⑶用移液管准确移出25.00 ml上述量杯中的溶液,弃去;再准确移入25.00 ml电导水,只于上述量杯中;搅拌均匀后,测定其电导率3次,取平均值。
⑷重复⑶的步骤2次。
⑸倾去电导池中的KCl溶液,用电导水洗净量杯和电极,量杯放回烘箱,电极用滤纸吸干
3、HAc溶液和电导水的电导率测定:
⑴用移液管准确移入100.0(mol·m-3)HAc溶液25.00 ml,置于洁净、干燥的量杯中,测定其电导率3次,取平均值。
⑵再用移液管移入25.00 ml已恒温的电导水,置于量杯中,搅拌均匀后,测定其电导率3次,取平均值。
⑶用移液管准确移出25.00 ml上述量杯中的溶液,弃去;再移入25.00 ml电导水,搅拌均匀,测定其电导率3次,取平均值。
⑷再用移液管准确移入25.00 ml电导水,置于量杯中,搅拌均匀,测定其电导率3次,取平均值。
⑸倾去电导池中的HAc溶液,用电导水洗净量杯和电极;然后注入电导水,测定电导水的电导率3次,取平均值。
⑹倾去电导池中的电导水,量杯放回烘箱,电极用滤纸吸干,关闭电源。
五、数据记录与处理
1、大气压:101.64kPa 室温:23.5℃
已知:25℃时10.00(mol·m-3)KCl溶液k=0.1413S·m-1;25℃时无限稀释的HAc水溶液的摩尔电导率=3.907*10-2(S·m2·m-1)
⑴测定KCl溶液的电导率:
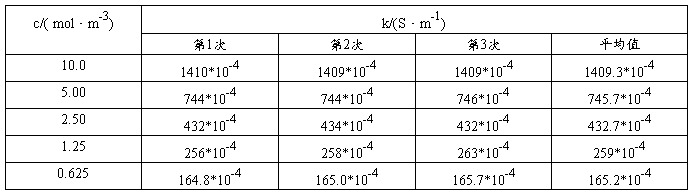
⑵测定HAc溶液的电导率:
电导水的电导率k(H2O)/ (S·m-1):7 *10-4S·m-1

2、数据处理
⑴将KCl溶液的各组数据填入下表内:

以KCl溶液的Λm对√C作图,由直线的截距求出KCl的Λ∞m。
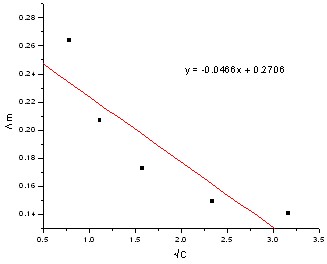
根据Λm=Λ∞m -A√C,截距即为Λ∞m,得Λ∞m =270.6*10-4 S·m2·mol-1
⑵HAc溶液的各组数据填入下表内:
HAc原始浓度:0.09509 mol·/L
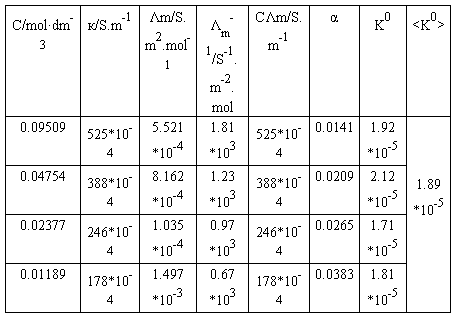
注:к=к-к(H2O)
以CΛm对1/Λm作图应得一直线,直线的斜率为(Λ∞m)2Kθ Cθ:

根据上图可知,该直线的斜率为3*10-5,截率为-0.0034;
即(Λ∞m)2Kθ Cθ=3*10-5。
已知Λ∞m =3.907*10-2S.m2.mol-1,
则Kθ=3*10-5/[(Λ∞m)2C0]= 3*10-5/[(3.907*10-2)2*1000]=1.965*10-5
将拟合获得的Kθ值,与表格计算的与<Kθ>=1.89*10-5作比较,
百分误差=(Kθ-<Kθ>)/<Kθ>*100%=(1.965*10-5-1.89*10-5)/(1.89*10-5)*100%=3.97%
六、结果与讨论
实验误差分析
1. 读数过程中,没有等到读数稳定就读数,导致 误差;
2. 测定HAc溶液时候,没有将电极洗净,导致测量误差;
3. 被测溶液可能含有部分杂质,使测得的电导率不是该纯物质的电导率。
对得出结果的讨论
1. 电解质溶液到点主要与电解质的性质,溶剂的性质,测量环境的温度有关,所以测电导时要恒温。而电导池常数是一个不随温度变化的物理量,因此可以直接在不同的温度下使用。
2. 电解质的摩尔电导率随浓度增加而降低,原因是:对强电解质而言,溶液浓度降低,摩尔电导率增大,这是因为随着溶液浓度的降低离子间引力变小,粒子运动速度增加,故摩尔电导率增大。对弱电解质而言,溶液浓度降低时,摩尔电导率也增加。在溶液极稀时,随着溶液浓度的降低,摩尔电导率急剧增加。
-
电导的测定及其应用实验报告
电导的测定及其应用一、实验目的1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。2、用电导法测量醋酸在水溶液中的解离平衡常…
-
电导的测定及应用实验报告
实验名称一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电…
-
电导的测定及其应用实验报告
001520015000148YAxisTitle00146001440014200140XAxisTitle根据截距即为得154…
-
电导的测定及其应用实验报告wqf
宁波工程学院物理化学实验报告专业班级姓名序号同组姓名指导老师实验日期3月31号实验名称实验五电导的测定及其应用一实验目的1测量KC…
-
电导的测定及其应用实验报告
电导的测定及其应用一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒…
-
电导的测定及应用实验报告
实验名称一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电…
-
电导的测定及其应用实验报告wqf
宁波工程学院物理化学实验报告专业班级姓名序号同组姓名指导老师实验日期3月31号实验名称实验五电导的测定及其应用一实验目的1测量KC…
-
电导的测定及其应用实验报告
电导的测定及其应用一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒…
-
物化实验报告5-电导的测定及其应用
一实验目的1测量KCl水溶液的电导率求它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电导率仪的使…
-
电导的测定及其应用实验报告
电导的测定及其应用一、实验目的1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。2、用电导法测量醋酸在水溶液中的解离平衡常…
-
物化实验报告7-电动势的测定及应用
一实验目的1通过实验加深对可逆电池可逆电极盐桥等概念的理解2掌握对消法测定电池电动势的原理及电位差计的使用方法3通过电池AgAgN…