贝诺酯的合成
实验一 阿司匹林的制备
一、实验目的
(1)掌握酯化反应和精制的原理;
(2)熟悉酯化反应和中和反应的注意事项;
(3)了解温度在反应中的重要性。
二、化学反应式
三、主要试剂及数量:

四、操作步骤:
(1)实验装置:在集热式磁力搅拌器水浴锅中,安装配有磁性搅拌子、温度计、回流冷凝管的250 mL三颈瓶;
(2)阿司匹林的制备:在三颈瓶中加入10 g水杨酸和14 mL乙酸酐,开动搅拌,逐滴加入1 mL硫酸,水浴加热到70℃,反应30分钟;冷却到室温,即有结晶析出(1);向反应混合物中慢慢加入200 mL水,使结晶完全;抽滤,冷水洗涤滤饼两次,抽干得粗品。
(3)阿司匹林的纯化:将粗品移至250 mL的烧杯中,搅拌下加入100mL饱和碳酸氢钠水溶液,加完后继续搅拌直至不再有气泡产生;抽滤,除去不溶性副产物,得滤液;将滤液倒入由20 mL盐酸与20 mL水配成的溶液中(2),析出大量沉淀;待其冷却至室温后,抽滤,水洗涤滤饼两次,抽干得产品;将产品转移至培养皿中,干燥后计算产量和产率。Mp.135-140℃。
五、注意事项
(1) 如不结晶,可用钢铲或玻璃棒摩擦瓶壁并将反应物置于冰水中冷却使结晶产生。
(2) 本项操作应慢,以免反应剧烈时,反应液从烧杯中溢出。
六、预习思考题
(1)反应液中加入少量浓硫酸的目的是什么?
(2)本反应可能产生的副反应有哪些?写出其化学反应式。
(3)本实验阿司匹林的精制方法与重结晶的精制方法在原理上有何不同?用粗产物纯化过程原理流程图说明其原理。
实验二 对乙酰氨基酚的制备
一、实验目的
(1)了解选择性乙酰化对氨基苯酚的氨基而保留酚羟基的方法;
(2)掌握易被氧化产品的重结晶精制方法。
二、化学反应式
三、主要试剂及数量:
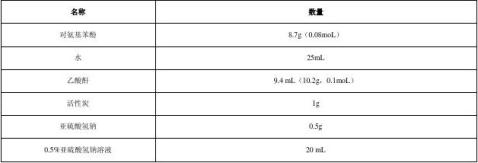
四、操作步骤:
(1)实验装置:在集热式磁力搅拌器水浴锅中,安装配有磁性搅拌子、温度计、回流冷凝管的250 mL三颈瓶。
(2)对乙酰氨基酚的制备:在三颈瓶中加入8.7 g对氨基苯酚和25mL水,开动搅拌,水浴加热到50℃;自滴液漏斗逐滴加入9.4 mL乙酸酐,控制滴加速度在30分钟完成;升温到80℃,保温120分钟;冷却到室温,即有结晶析出;抽滤,冷水洗涤滤饼两次,抽干得粗品。
(3)对乙酰氨基酚的纯化:将粗品移至250 mL三颈瓶中,加入50mL水,电热套加热使溶解;稍冷后加入1g活性碳,回流15分钟;在抽滤瓶(1)中先加入0.5g亚硫酸氢钠,趁热抽滤,滤液趁热转移至100mL烧杯中;放冷析晶,抽滤,滤饼以20mL0.5%亚硫酸氢钠溶液分2次洗涤,抽干得产品;将产品转移至培养皿中,干燥后计算产量和产率。Mp.168-170℃。
五、注意事项
(1) 该步骤用的布氏漏斗和抽滤瓶要在干燥箱中预热后使用。
六、预习思考题
(1)如果采用冰醋酸作酰化剂制备对乙酰氨基酚,其实验方案和反应装置如何?为什么?
(2)对乙酰氨基酚重结晶时加入亚硫酸氢钠的目的是什么?
(3)阿司匹林的制备和对乙酰氨基酚的制备这两个实验都是采用乙酸酐作酰化剂,但是乙酸酐的加入方法却不同,为什么?
(4)对乙酰氨基酚的精制方法和阿司匹林的精制方法在原理上有何不同?为什么?
实验三 贝诺酯的制备
一、实验目的
(1)通过乙酰水杨酰氯的制备,了解氯化试剂的选择及操作中的注意事项;
(2)了解前药原理和拼合原理在化学结构修饰方面的应用;
(3)了解肖特—鲍曼(Schotten-Baumann)酯化反应原理。
二、化学反应式
三、主要试剂及数量:
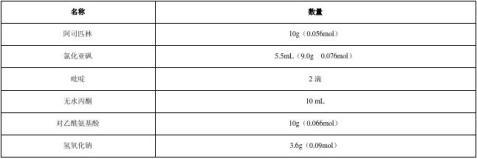
四、操作步骤:
(1)乙酰水杨酰氯的制备:在干燥的100 mL圆底烧瓶中,依次加入10g阿司匹林,5.5 mL氯化亚砜(1),2滴吡啶,迅速安装顶端带有氯化钙干燥管并连接气体吸收装置的球形冷凝管。集热式磁力搅拌器油浴锅加热至70℃,圆底烧瓶外油浴中置一支温度计,用于校正传感器的温度,维持该温度反应70分钟,冷却,加入10 mL无水丙酮,混合均匀,密闭备用。
(2)对乙酰氨基酚钠的制备:将250 mL三颈瓶安装到集热式磁力搅拌器水浴锅中,配置搅拌子、温度计及滴液漏斗,加入10g对乙酰氨基酚,50 mL水。冰水浴冷却至10℃左右时,搅拌下用滴管逐滴加入3.6g氢氧化钠与20mL水配制的氢氧化钠溶液。
(3)贝诺酯粗品的制备(2):在三颈瓶中口上安装顶端连接气体吸收装置的球形冷凝管,乙酰水杨酰氯丙酮溶液加入干燥的滴液漏斗中。在对乙酰氨基酚钠溶液8-12℃之间,于快速搅拌下,慢慢滴加乙酰水杨酰氯丙酮溶液。滴加完毕后,再滴加20%氢氧化钠溶液直至反应液pH≥10,依然控制温度在8-12℃之间,继续搅拌反应60分钟,抽滤,产物用水洗涤至中性,即得贝诺酯粗品。干燥,称重,计算收率。
(4)贝诺酯的纯化:在100mL圆底烧瓶中加入4g贝诺酯粗品,60mL95%乙醇。电热套加热回流,贝诺酯粗品全部溶解。而后移去电热套,冷却后加入0.3g活性炭,继续加热回流30分钟。趁热用已经预热的布氏漏斗和抽滤瓶过滤,滤毕,趁热转移至100mL烧杯中,冷却使结晶完全,抽滤,压干;用少量冷乙醇洗涤析出的结晶两次,抽干后将结晶移至培养皿中即得贝诺酯精品。红外灯下干燥、称重,计算回收率和总产率。Mp. 177-181℃。 本实验约需10学时。
五、注意事项
(1) 二氯亚砜是由羧酸制备酰氯最常用的氯化试剂,不仅价格便宜而且沸点低,生成的副产物均为挥发性气体,故所得酰氯产品易于纯化。二氯亚砜遇水可分解为二氧化硫和氯化氢,因此所用仪器均需干燥;加热时不能用水浴。反应用乙酰水杨酸需干燥。吡啶作为催化剂,用量不宜过多,否则影响产品的质量。制得的乙酰水杨酰氯不应久置。
(2) 贝诺酯制备采用Schotten-Baumann方法酯化,即乙酰水杨酰氯与对乙酰氨基酚钠缩合酯化。由于对乙酰氨基酚羟基与苯环共轭,加之苯环上又有吸电子的乙酰胺基,因此酚羟基上电子云密度较低,亲核反应性较弱;成盐后酚羟基氧原子电子云密度增高,有利于亲核反应;此外,酚钠成酯,还可避免生成氯化氢,使生成的酯键水解。
六、预习思考题
(1)在乙酰水杨酰氯的制备中,应注意哪些事项?为什么?
(2)贝诺酯的制备,为什么采用先制备对乙酰氨基酚钠,再与乙酰水杨酰氯进行酯化,而不直接酯化?
(3)通过本实验说明酯化反应在结构修饰中的意义。
第二篇:贝诺酯的相转移催化合成






-
企业公司扶贫工作总结1
企业公司扶贫工作总结自从20××年以来XX帮扶的农村工作联系点调整到XX村,在市农村小康建设工作领导小组的领导及共同努力下,我厂认…
-
20xx年上半年护理工作总结
20xx年上半年护理部工作总结20xx年上半年,护理部在医院领导的正确领导下,围绕医院20xx-20xx年四年规划,结合护理部的工…
-
3季度案件防范工作总结修改版Microsoft Word 文档
三季度案件防范分析汇报在市行的指导下,***支行认真按照上级部署,严格落实案防要求,切实履行案防职责,将责任细化到个人,有效地防范…
-
开展安全风险管理工作总结
和田电力有限责任公司供电公司根据上级公司新和电安〔20xx〕127号《关于印发公司开展安全风险管理工作实施意见的通知》文件要求和《…
-
社区20xx年退休职工认证工作总结
20xx年退休人员资格认证工作总结为最大限度杜绝冒领养老金现象,避免有限的社保基金流失,我社区于二0一二年四月份着手退休人员养老金…