蒸馏及沸点的测定2
蒸馏及沸点的测定
一、 实验目的
1. 了解蒸馏和沸点测定的用途
2. 掌握沸点测定的方法。
3. 掌握蒸馏烧瓶、冷凝管等的使用方 法,学会蒸馏装置的使用。
二、 实验原理
当液体饱和蒸汽压与外界压强相等时,液体开始沸腾汽化。蒸馏是将液体加热到沸腾状态,使之汽化,再将蒸汽冷凝为液体的两个联合操作。它是分离和提纯液体化合物最常用的一种方法,也是测定液体沸点的一种方法。
沸点是液体的饱和蒸汽压与外界压强相等时的温度。每个纯的有机化合物在一定的压力下均有恒定的沸点。液体沸点的测定可以用来鉴别有机化合物,也可以用之定性的鉴定化合物的纯度。
三、 实验仪器和药品
仪器:圆底烧瓶、直形冷凝管、接受器、
锥形瓶、蒸馏头、温度计等。
药品:工业酒精。
四、 实验装置
(在装置上讲解)
五、 实验步骤
(结合装置讲解)
六、 实验注意事项
1. 是否放了沸石,若已经开始热而发现忘了放沸石,那么应等液体冷却后在加沸石。
2. 温度计水银球的位置是否正确。
3. 先通水后加热,水应从冷凝管的下方进上方出。
第二篇:工业乙醇的蒸馏与沸点的测定
工业乙醇的蒸馏与沸点的测定
〖实验目的〗
(1)掌握简单蒸馏和分馏的操作技术。
(2)掌握微量法测定沸点的方法。
〖实验用品〗
仪器:250ml圆底烧瓶、接液管、温度计、接受器、直型冷凝管、酒精灯、铁架台、沸点管、韦氏分馏住。
材料:小橡皮圈、沸石。
药品: 40%酒精溶液(工业级)。
〖实验原理〗
(1)水和乙醇沸点不同,用蒸馏或分馏技术,可将乙醇溶液分离提纯。
(2)当溶液的蒸气压与外界压力相等时,液体开始沸腾。以此原理用微量法测定乙醇的沸点。
〖操作步骤〗
1.蒸馏与分馏
(1)取150ml40%的酒精样品注入250ml磨口圆底烧瓶中,放入2~3粒沸石。
(2)分别按照简单蒸馏(见图2.2.8)和分馏(见图2.2.11)装置图及注意事项安装好仪器。

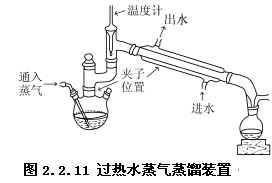
(3)用酒精灯在石棉网下加热,并调节加热速度使馏出液体的速度控制在每移秒1滴~2滴。记录温度刚开始恒定而馏出的一滴馏液时的温度和最后一滴馏液流出时的温度。当具有此沸点范围(沸程)的液体蒸完后,温度下降,此时可停止加热。同时收集好除去前馏分后的馏液。千万不可将蒸馏瓶里的液体蒸干,以免引起液体分解或发生爆炸。
(4)称量所收集馏分的质量或量其体积,并计算回收率。
2.微量法测乙醇沸点
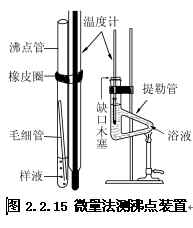
沸点测定有常量法和微量法两种,常量法可借助简单蒸馏或分馏进行。微量法测定沸点(装置见图2.2.15)是置1滴~2滴乙醇样品于沸点管中,再放入一根上端封闭的毛细管,然后将沸点管用小橡皮圈缚于温度计旁,放入热浴中进行缓慢加热。加热时,由于毛细管中的气体膨胀,会有小气泡缓缓逸出,在到达该液体的沸点时,将有一连串的小气泡快速地逸出。此时可停止加热,使浴温自行冷却,气泡逸出的速度即渐渐减慢。当气泡不再冒出而液体刚要进入毛细管的瞬间(即最后一个气泡缩 至毛细管中时),表示毛细管内的蒸气压与外界压力相等,此时的温度即为该液体的沸点。
-
常压蒸馏及沸点测定实验
新乡医学院医用化学实验课教案首页授课教师姓名及职称新乡医学院化学教研室年月日实验常压蒸馏及沸点测定一实验目的1了解沸点测定的原理及…
-
乙醇的蒸馏及沸点测定 实验报告
报告题目:乙醇的蒸馏及沸点测定实验报告报告题目:乙醇的蒸馏及沸点测定专业班级:生物工程指导老师:***学生姓名:**学号:**20…
-
有机化学实验-----蒸馏及沸点的测定技术
实验报告姓名班级同组人项目蒸馏及沸点的测定技术课程学号一实验目的1了解蒸馏和沸点测定的基本原理和意义2掌握蒸馏和沸点测定的操作技术…
-
实验二:乙醇的蒸馏及沸点的测定
实验二乙醇的蒸馏及沸点的测定一实验目的1了解蒸馏提纯液体有机物的原理用途2掌握蒸馏提纯液体有机物的操作步骤3了解沸点测定的方法4了…
-
熔点.沸点的测定实验报告
有机化学实验报告实验学专班姓指导日名称院业级名教师期熔点的测定沸点的测定化学工程与工艺化工133班王腾飞学号134020xx330…
-
有机化学实验-----蒸馏及沸点的测定技术
实验报告姓名班级同组人项目蒸馏及沸点的测定技术课程学号一实验目的1了解蒸馏和沸点测定的基本原理和意义2掌握蒸馏和沸点测定的操作技术…
-
乙醇的蒸馏及沸点的测定
大学化学基础实验II实验报告课程名称物理化学实验实验名称乙醇的蒸馏及沸点的测定姓名张玉学号1108110191专业化学工程与工艺班…
-
乙醇的蒸馏及沸点测定 实验报告
报告题目:乙醇的蒸馏及沸点测定实验报告报告题目:乙醇的蒸馏及沸点测定专业班级:生物工程指导老师:***学生姓名:**学号:**20…
-
熔点.沸点的测定实验报告
有机化学实验报告实验学专班姓指导日名称院业级名教师期熔点的测定沸点的测定化学工程与工艺化工133班王腾飞学号134020xx330…
-
实验二:乙醇的蒸馏及沸点的测定
实验二乙醇的蒸馏及沸点的测定一实验目的1了解蒸馏提纯液体有机物的原理用途2掌握蒸馏提纯液体有机物的操作步骤3了解沸点测定的方法4了…