酪蛋白的提取与测定
牛乳中酪蛋白的制备与浓度测定
一、实验目的
1、学习从牛乳中分离酪蛋白的原理和方法
2、掌握等电点沉淀法提取蛋白质的方法
3、了解紫外吸收法测定蛋白质浓度的原理,熟悉紫外分光光度计的使用
4、学会用考马斯亮蓝结合法测定蛋白质浓度
二、实验原理
1、准备酪蛋白原理:牛乳中主要含有酪蛋白和乳清蛋白两种蛋白质,其中酪蛋白占了牛乳蛋白质的80%。牛乳在PH4.7时酪蛋白等电聚沉后剩余的蛋白质统称为乳清蛋白。酪蛋白是白色、无味的物质,不溶于水、乙醇等有机溶剂,但溶于碱溶液。乳清蛋白不同于酪蛋白,其粒子的水和能力很强,分散性高,在乳中呈高分子状态。本法利用等电点时溶解度最低的原理,将牛乳的PH调至4.7时,酪蛋白就沉淀出来。用乙醇洗涤沉淀物,除去脂类杂质后便可得到纯的酪蛋白。
2、紫外吸收法测定蛋白质浓度的原理:大多数蛋白质由于有酷氨酸和色氨酸的存在,在紫外光280nm有吸收高峰,可以进行蛋白质含量的测定。但是核酸在280nm也有吸收,干扰测定,不过核酸的最大吸收峰在260nm,通过测定在280nm和260nm时A的比值,然后通过计算消除核酸存在的影响,可以求得有核酸存在时蛋白质的浓度。
3、考马斯亮蓝结合法测定蛋白质浓度原理:考马斯亮蓝能与蛋白质的疏水微区相结合,这种结合具有高敏感性。考马斯亮蓝G250的磷酸溶液呈棕红色,最大吸收峰在465nm。当它与蛋白质结合形成复合物时呈蓝色,其最大吸收峰改变为595nm,考马斯亮蓝G250—蛋白质复合物的高消光效应导致了蛋白质定量测定的高敏感度。
在一定范围内,考马斯亮蓝G250—蛋白质复合物呈色后,在595nm下,吸光度与蛋白质含量呈线性关系,故可以用于蛋白质浓度的测定。
三、实验器材与试剂
1、制备酪蛋白:
烧杯、玻璃棒、量筒、精密PH试纸、离心机、布氏漏斗、表面皿、恒温水浴锅
牛奶、醋酸缓冲液、冰醋酸、95%乙醇、无水乙醚
2、紫外光吸收法:
紫外可见光分光光度计、容量瓶50ml(×1)、石英比色皿
0.9%NaCl、1mol/LNaOH溶液、1mol/L乙酸溶液
3、考马斯亮蓝法:
紫外可见光分光光度计、试管1.5cm×15cm(×9)、玻璃比色皿
牛血清白蛋白(0.1mg/ml)、考马斯亮蓝、0.9%NaCl
四、实验步骤
制备酪蛋白
1、将20mL pH4.7的醋酸-醋酸钠缓冲液预热至40℃
2、将20mL牛奶加热至40℃,在搅拌下缓慢地加入20mL预热的pH4.7的醋酸-醋酸钠缓冲液
3、用精密pH试纸调pH至4.7,可见溶液变为乳白色悬浮液
4、待悬浮液冷却至室温,4000rpm离心5min,弃上清,得酪蛋白粗制品
5、用蒸馏水洗沉淀3次,3000rpm离心5min,弃上清
6、在沉淀中加入20mL95%乙醇,搅拌片刻,将全部悬浊液转移至布氏漏斗中抽滤
7、用乙醇-乙醚混合液洗涤沉淀2次(10ml/次),最后用乙醚洗涤沉淀2次(10ml/次),抽干
8、将沉淀摊开在表面皿上,风干,得酪蛋白纯品
9、准确称量,计算含量和得率
紫外光吸收法
1.取待测样品溶液置于的石英比色皿中,于分光光度计波长280nm和260nm,分别读取A280nm和A260nm,用生理盐水为比色空白对照。
2.若A280nm/A260nm>1.5,用公式:蛋白质含量(mg/ml)=A280nm/6.3*10 若A280nm/A260nm<1.5,用公式:蛋白质含量(mg/ml)=1.45A280nm—0.74A260nm
考马斯亮蓝法
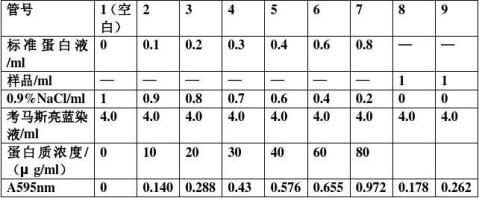
取9支干净试管,按表进行编号并加入试剂。
混匀,室温静置3min,以第1管为空白,于波长595nm处比色,读取吸光度,以吸光度为纵坐标,各标准液浓度(μg/ml)作为横坐标作图得标准曲线。
五、实验数据
酪蛋白质量:0.5421g
酪蛋白含量:2.71g/100ml牛乳
紫外光吸收法:A280nm 0.769A A260nm 0.959A
A280nm/A260nm<1.5,蛋白质含量(mg/ml)=1.45A280nm—0.74A260nm =0.405 mg/ml
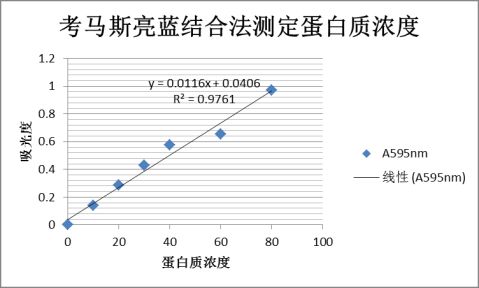
蛋白质浓度为
第二篇:牛奶中提取酪蛋白
牛奶中提取酪蛋白
[目的与要求]
1、了解等电点沉淀法
2、学习从牛奶中制备酪蛋白的方法
3、加深对蛋白质等电点性质的理解
[原理]
蛋白质是一种亲水胶体,在水溶液中蛋白质分子表面形成一个水化层。另外,蛋白质又是一种两性离子,在一定pH溶液能够维持一个稳定的状态。但是调节蛋白质溶液的pH值至等电点时,蛋白质会因失去电荷而变得不稳定,此时若再加脱水剂或加热,水化层被破坏,蛋白质分子就相互凝聚而析出。等电点沉淀法主要利用两性电解质分子在等电点时溶解度最低的原理,而多种两性电解质具有不同等电点而进行分离的一种方法。
牛乳中主要的蛋白质是酪蛋白含量约为35g/L。酪蛋白是一些含磷蛋白质的混合物,等电点为4.7。将牛乳的pH调至4.7时,酪蛋白就沉淀出来。用乙醇洗涤沉淀,除去脂类杂质后便可得到较纯的酪蛋白。
但单独利用等电点沉淀法来分离生化产品效果并不太理想,因为即使在等电点时,有些两性物质仍有一定的溶解度,并不是所有的蛋白质在等电点时都能沉淀下来,特别是同一类两性物质的等电点十分接近时。生产中常与有机溶剂沉淀法、盐析法并用,这样沉淀的效果较好。 本实验目的是使学生运用等电点沉淀法制备酪蛋白,从中加深对蛋白质等电点性质的理解。
[方法和步骤]
1、取预先放冰箱中冷却的消毒牛奶6mL,3 000r/min离心10min,除去脂肪层的乳液置50毫升烧杯内,加热至40℃左右,在搅拌下慢慢加入10mL左右预热的醋酸-醋酸钠缓冲液,此时混浊液中有大量絮状物沉下。冷至室温,3 000r/min离心10min,弃去上清液,得酪蛋白粗品。
2
5mL左右),3 000r/min离心10min,弃去上清液。
3、将沉淀置研钵中,研碎后,渐加5mL 95%乙醇,静置片刻,将全部悬浮液转移至布氏漏斗抽滤,抽干后的制品,用乙醇-乙醚混合液洗沉淀二次(每次5mL),最后用无水乙醚洗沉淀二次(每次5mL),抽干。
4、将沉淀摊开在表面皿上,风干,得酪蛋白制品(称重,记录)。
5、酪蛋白溶液的配制:称取酪蛋白0.1g,置10毫升烧杯中,加5mL 0.2mol/L氢氧化钠溶液,搅匀, 隔水加热,溶解后转移至10


[结果与计算]
计算酪蛋白含量和得率:
1、含量:酪蛋白克数/100mL牛奶 2、
式中理论含量3.5g/100mL牛奶
-
蛋白质的定量测定实验报告
显问题其次回顾全部过程的原理我们猜测可能存在的造成结果低的情况为在室温冷却后实验室没有空余的分光光度计排队时间应该是全部小组中最长…
-
蛋白质测定实验报告
蛋白质测定方法化学报告蛋白质的检测酚试剂法灵敏度较高20250mg费时蛋白质在碱性溶酚类柠檬液中其肽键与酸硫酸铵Cu2螯合形成tr…
-
蛋白质测定实验报告
生物化学实验报告姓名学号专业年级组别生物化学与分子生物学实验教学中心实验名称实验日期20xx1015合作者评分Folin酚试剂法测…
-
紫外分光光度法测定蛋白质含量实验报告
紫外分光光度法测定蛋白质含量一实验目的1学习紫外光度法测定蛋白质含量的原理2掌握紫外分光光度法测蛋白质含量的实验技术二实验原理1测…
-
分光法测蛋白质实验报告
紫外分光光度法测定蛋白质含量一实验目的1学习紫外分光光度法测定蛋白质含量的原理2掌握紫外分光光度法测定蛋白质含量的实验技术3掌握T…
-
20xx—20xx学年上期体育学院学生会学习部工作总结
重庆邮电大学体育学院学生会学习部20xx—20xx学年度上期工作总结在体育学院团总支、学生会的领导和校学生会学习部的引导下,体育学…
-
中职专业教师暑期企业实践活动总结
中职专业教师暑期企业实践活动为了加强职业教育与行业的联系,提高专业教师实践水平,培养“双师”型专业骨干教师,学校安排专业教师暑期到…
-
班主任德育工作经验总结 金丝峡镇中心小学 邓萍
德育论文用爱搭建爱的桥梁金丝峡镇中心小学邓萍“捧着一颗心来,不带半根草去。”从教以来我一直以陶行知的这句话勉励自己。在学校领导的统…
-
办公室9月份工作总结
办公室九月份工作总结九月份,办公室严格按照领导的工作部署,继续贯彻落实精细化管理要务,抓好全局人事、报账、后勤等行政管理工作,为厂…
-
个人年终总结 2
年终个人总结20xx在一场寒流中就这样离去,回顾半年来的工作历程,在公司领导及各位同事的大力支持与帮助下,无论在思想意识、还是业务…