醋酸乙烯酯的溶液聚合
高分子化学实验
醋酸乙烯酯的溶液聚合
一、目的要求
1、 通过本实验掌握溶液聚合的实验方法和溶液聚合的特点。
2、 掌握醋酸乙烯酯聚合原理及溶剂对醋酸乙烯酯溶液聚合的影响。
二、实验基本原理
1、单体的性质
醋酸乙烯酯的分子量为86.09。纯的醋酸乙烯酯的聚合能力很强,在常温下能缓慢聚合,在光和引发剂的作用下聚合的速度显著提高。聚合过程为放热反应,故聚合开始后即能自行加快聚合速度。
醋酸乙烯醋在无机酸或碱的作用下易发生水解,生成乙醛和乙酸。受热的稳定温度可达到400℃。
醋酸乙烯酯(VAC)的物化常数
凝固点(℃) -84
沸点(℃) 73
密度 0.9342
折光率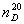 1.3958
1.3958
膨胀系数(5-250)(l/℃) 0.00155
粘度(20℃)厘泊 0.432
燃烧热(kJ/mol) 2072.07
生成热(kJ/mol) 118.46
蒸馏潜热(kJ/mol) 32.65
闪点(℃) -5—8
水中溶解度(20℃)% 2.5
水在VAC中溶解度(20℃)% 0.1
2、聚合反应机理
醋酸乙烯酯的聚合方式按自由基型链式反应进行。常用的引发剂是过氧化物体系和偶氮双腈体系、反应过程中除链引发、链增长、链终止三个分数外还有链转移反应,反应机理如下:
(1) 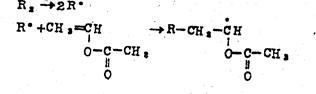 链引发
链引发
(2)链增长
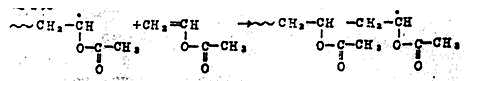
(3)链转移
在醋酸乙烯酯聚合反应中,由于RCH2CHOCOCH3的活性大,增长的活性链容易向溶剂,向单体以及向已生成的聚合物大分子转移。
① 向溶剂转移
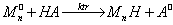
如果A·不活泼,不与单体发反,或反应速度很小HA就称为阻聚剂或缓聚剂。如A·很活泼,易与单体发生反应,重新引起聚合反应,HA就称为链转移剂。
有溶剂情况下平均聚合度

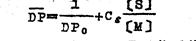
式中:DP0—无溶剂存在条件下时聚合物平均聚合度。
[S] —溶剂浓度
[M]—单体浓度
Cs—链转移常数
② 向单体转移,可形成支链聚合物
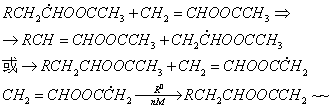
③ 向大分子转移,也可形成支链聚合物
(4)终止链
链终止一般按偶合终止和歧化终止两种方式进行。
偶合终止:
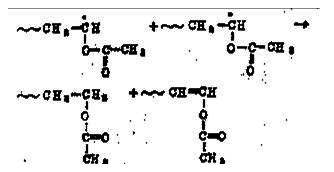
醋酸乙烯酯的聚合实施方法也有本体、悬浮、乳液和溶液聚合四种方法。溶液聚合是最广泛的一种方法。所得到的聚醋酸乙烯酯溶液可以加工成聚乙烯醇,可纺丝作纺织物,也可作粘合剂和清漆等。本实验采用溶液聚合来制备聚醋酸乙烯酯。
三、实验配方与仪器
1、试剂与配方
醋酸乙烯酯(新蒸馏) 40克
乙醇(或甲醇、或丙酮) 40克
过氧化苯甲酰 0.4克(0.5%)
2、实验仪器
实验用仪器与实验5相同。
四、实验操作步骤
将醋酸乙烯酯40克、过氧化苯甲酰0.2克、乙醇溶剂20克等加入三颈瓶中,搅拌、加热,使引发剂过氧化苯甲酰溶解。升温至70-73℃在此温度下反应1小时,然后加入10克乙醇溶剂。又在70-73℃下反应1小时后将剩余的10克乙醇溶剂全部加入,继续在此温度下反应。一般反应时间为4小时左右。可参看反应体系粘度增加,并结合反应时间来确定反应终点。
在反应过程中测不同时间的转化率,做出转化率随时间变化曲线。反应进行30分钟测一个值,反应结束时测最后一个值,共测4-6个值。测转化率的方法是:取一块铝箔,摺成一小方盒(带有盖)、并称重。用吸管取样1克快速称重,然后在空气中使溶剂挥发30分钟后再放入100℃烘箱中烘12小时,称重恒重,即可算出转化率。
转化率%=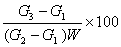
式中:G1 ——小盒重量
G2 ——干燥前(小盒重量 + 样品重量)
G3 ——干燥后(小盒重量 + 样品重量)
W——单体质量%
此实验可以用不同的溶剂(如甲醇、丙酮)进行聚合反应,观察溶剂对反应速率的影响和对转化率的影响。(反应条件有所变动)
五、影响聚合反应的主要因素
醋酸乙烯酯溶液聚合的关键问题就是链转移。单体、溶剂和杂质都有个链转移问题。所以影响因素主要考虑与链转移有关的因素。
1、溶剂的选择与用量
在溶液聚合中,溶剂的选择和用量对聚合反应速率和聚合物的分子结构、分子量大小及分布都有重要的影响。溶剂不直接参加聚合反应。但溶剂对过氧化物体系的引发剂有诱导分解作用,而诱导分解虽然使引发剂效率降低,但使引发速率增加。各类溶剂对过氧化物类引发剂的分解速率按如下次序依次增加:芳烃、烷烃、醇类、胺类。
溶剂能控制生长着的链分子的分散状态和构型。溶剂能降低向大分子进行转移反应的几率;从而减少聚合物的支化和交联。
溶剂对聚合物分子量大小有影响。即大分子活性链与单体的加成能力应远远大于分子活性链与溶剂的链作用能力,否则溶剂发生链转移,既影响了聚合速率又使分子量降低,因而选择溶剂,首先看其链转移常数Cs。选择链转移常数小的溶剂一般可制备高分子量的聚合物。
另外要得到聚合的溶液,可选择聚合物的良溶剂,而要使聚合物沉淀出来,就要选择聚合物的非溶剂。下面列出一些溶剂的链转移常数。
溶剂的链转移常数Cs
(VAC,60C,AIBN引发剂)
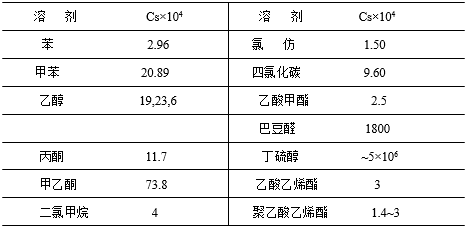
溶剂的用量由[AB]/[M]的比值决定,根据公式 可以看出聚合度首先决定于溶剂的Cs,但也决定于所用溶剂的量。如果要达到某一聚合度,即可知道溶剂在反应体系中的用量。
可以看出聚合度首先决定于溶剂的Cs,但也决定于所用溶剂的量。如果要达到某一聚合度,即可知道溶剂在反应体系中的用量。
2、单体
前面已述,增长的活性链容易向单体发生链转移,其如形成支链聚合物,一般控制到聚合反应的转化率在50~60%时停止反应,这样就可以避免支化反应。
3、杂质
在聚合反应中,如果存在醛和巴豆醛,就很难聚合。因为它们的链转移常数非常大,聚合度一般小时10。醛可以作分子量调节剂,当需要的产物的聚合度不是太大时,可在能得到聚合度较大的溶剂中加入少量的乙醛,即可使聚合度适当降低。
此外,聚合温度的影响是温度升高,聚合度相应降低,温度降低,所得出的聚醋酸乙烯酯形成的聚乙烯醇的结晶度高,生产的维尼龙纤维耐热水性好,但反应热移出困难。氧对醋酸乙烯酯的聚合反应有双重作用。吸氧量多时起阻聚作用;吸氧量少时起引发聚合作用。
六、 结果处理
绘出时间——转化率曲线。
七、思考题
1、溶液聚合的特点是什么?为什么说醋酸乙烯酯溶液聚合的关键问题是链转移?
2、比较不同的溶剂对醋酸乙烯酯溶液聚合反应的影响?
注:本文引用于成都科技大学编的《高分子合成专业实验教材》(1983年6月)。
第二篇:实验04 醋酸乙烯酯溶液聚合及聚醋酸乙烯酯的醇解
实验五 醋酸乙烯酯的溶液聚合及聚醋酸乙烯酯的醇解
聚乙烯醇是制备维纶的原材料。由于乙烯醇很不稳定,极易异构化成乙醛。所以聚乙烯醇通常都是通过醋酸乙烯溶液聚合以及聚醋酸乙烯酯的醇解这两个步骤来制得的。
本实验是以偶氮二异丁腈为引发剂;甲醇为溶剂的醋酸乙烯酯的溶液聚合。这是个自由基聚合反应。
一、实验目的
1、通过实验掌握醋酸乙烯酯溶液聚合的方法以及聚醋酸乙烯酯醇解的方法。
2、进一步掌握溶液聚合原理及高分子侧基反应原理。
3、掌握醇解度测定方法。
二、实验原理
本实验采用溶液聚合的自由基聚合原理。
选用甲醇作溶剂是由于聚醋酸乙烯酯(PVAc)能溶于甲醇,而且聚合反应中活性链对甲醇的链转移常数较小。且在醇解制取聚乙烯醇(PVA)时,加入催化剂后在甲醇中即可直接进行醇解。
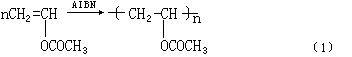 醋酸乙烯(VAc)在聚合过程中,容易发生向聚合物链的链转移反应。聚合物浓度越大,支化越容易发生。聚合物活性自由基链除了向聚醋酸乙烯酯(PVAc)主链上的α、β氢处链转移,形成水解不掉的支链,还会向乙酰基上活泼氢原子转移,在乙酰基上形成支链。这部分支链容易水解脱掉,导致聚合度降低。
醋酸乙烯(VAc)在聚合过程中,容易发生向聚合物链的链转移反应。聚合物浓度越大,支化越容易发生。聚合物活性自由基链除了向聚醋酸乙烯酯(PVAc)主链上的α、β氢处链转移,形成水解不掉的支链,还会向乙酰基上活泼氢原子转移,在乙酰基上形成支链。这部分支链容易水解脱掉,导致聚合度降低。
在聚合反应的同时,可能存在副反应:
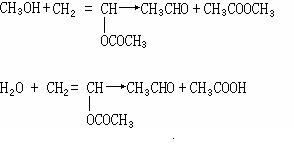
(2)
在单体浓度为85%时聚合得聚醋酸乙烯酯(PVAc),醇解后聚合度下降38.15%。单体浓度为67%时醇解后只降低了6.89%。因此,要降低溶液中单体浓度。但单体浓度过低,会影响产物的最终聚合度。
表1 60℃甲醇中不同单体浓度溶液聚合得到PVAc和PVA的聚合度
|
单体浓度/% |
聚合时间/h |
转化率/% |
PVAc聚合度 |
PVA聚合度 |
聚合度降低/% |
|
85 |
16 |
96.2 |
1903 |
1177 |
38.15 |
|
67 |
17 |
96.6 |
668 |
622 |
6.89 |
聚醋酸乙烯酯(PVAc)的醇解可以在酸性或碱性的催化下进行,用酸性醇解时,由于痕量级的酸很难从PVA中除去,而残留的酸可加速PVA的脱水作用,使产物变黄或不溶于水,所以一般均采用碱性醇解法。另外,甲醇中的水对醇解会产生阻碍作用。因为水的存在使反应体系内产生CH3COONa,消耗了NaOH,而NaOH在此起的是催化作用。因此,一定要严格控制甲醇中的水的含量。
聚醋酸乙烯酯(PVAc)的醇解过程是在碱的催化下聚醋酸乙烯酯(PVAc)在甲醇溶液进行的醇解反应。其反应方程式为:
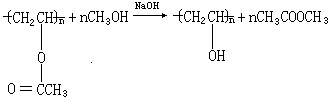
(3)
本实验先制备聚醋酸乙烯酯(PVAc),然后再进行碱性醇解,由于产物PVA不溶于甲醇,所以,醇解到一定程度时会观察到明显的相转变,此时,大约有60%的乙酰基已被羟基取代。
三、实验仪器和试剂
(1)实验仪器
电动搅拌器、恒温水浴锅、水泵减压装置 电炉子、三口烧瓶、直形冷凝管、球形冷凝管、恒压滴液漏斗、布氏漏斗、烧杯(50ml)、量筒(50ml、100ml)、温度计(100℃)、表面皿。
 实验试剂和药品:醋酸乙烯酯(VAC)(重蒸)、甲醇、偶氮二异丁腈(AIBN)、NaOH。
实验试剂和药品:醋酸乙烯酯(VAC)(重蒸)、甲醇、偶氮二异丁腈(AIBN)、NaOH。
四、实验方法及步骤
1、醋酸乙烯酯的聚合
(1)称量三口烧瓶。
(2)按图1组装好实验仪器。
(3)将20克醋酸乙烯酯(换算成体积;比重0.93)加入到三口烧瓶中,将0.1克偶氮二异丁腈(AIBN)放入一个烧杯中;加入20克甲醇,充分溶解后加入到三口烧瓶中。
(4)开始升温,温度升到60℃时,开始记录反应时间。
(4)控制水浴温度在61—63℃,温度偏差不应超过2℃,保持温度,注意观察反应物溶液的粘度,持续反应三小时。
(5)反应三小时后停止加热,冷却至室温。将实验装置改装成减压蒸馏装置如图2所示。将产物中的溶剂以及未聚合的单体蒸出(馏液回收)。留在烧瓶中的产物是无色的玻璃状聚合物,取下烧瓶,连瓶一块称重,并计算产率。
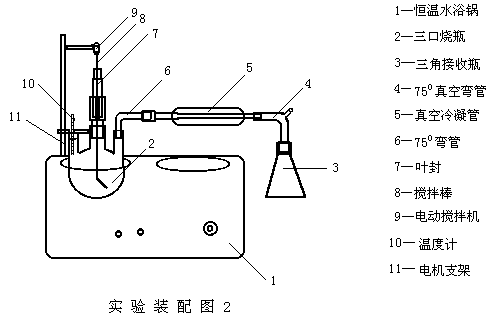
 2、聚醋酸乙烯酯的醇解
2、聚醋酸乙烯酯的醇解
(1)将所制得的聚醋酸乙烯酯留8克于三口烧瓶中。
(2)向三口烧瓶中加入50ml甲醇,加热回流,使之完全溶解,冷却后倒入滴液漏斗中。
(3)向三口烧瓶中加入0.5克NaOH,用甲醇溶液溶解至100ml。
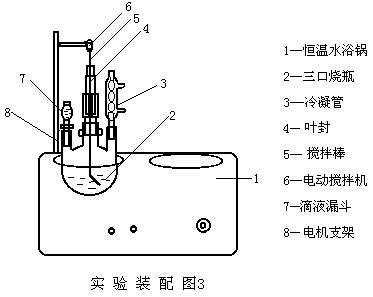
(4)按图3所示组装好实验仪器。将装有聚醋酸乙烯-甲醇溶液的滴液漏斗装于三口烧瓶的一个侧口上;另一侧口装冷凝器,上回流水。
(5)启动搅拌器快速搅拌,将水浴锅温度上升至65~70℃。
(6)慢慢地打开滴液漏斗阀门,缓慢地滴加聚醋酸乙烯-甲醇溶液,滴加溶液完成时间大约为30~40分钟。
注意:滴加溶液的速度不要太快,太快容易生成冻胶,不利于醇解及产物的洗涤。
(7)滴加溶液完毕后,应继续反应回流40~60分钟。大约1小时后停止加热,冷却。
(8)将三口烧瓶取下,将物料用布氏漏斗过滤,用10ml甲醇溶液洗涤,重复洗涤三次。滤液回收。
(9)将所得产物盛于表面皿上,放入烘箱中烘干,烘箱温度应保持在50~60℃。干后称重,并计算转化率。
五、实验数据的整理
将实验记录的数据整理成表。
表2 制备聚醋酸乙烯酯和聚乙烯醇的原料加入量
|
试 剂 名 称 |
VAC |
CH3OH |
AIBN |
NaOH |
PVAc |
|
|
聚合反应试剂用量 |
重量/g |
|||||
|
体积/ml |
||||||
|
醇解反应试剂用量 |
重量/g |
|||||
|
体积/ml |
||||||
表3 产物的转化率
|
聚合反应 |
三口烧瓶重量/g |
瓶+PVAc重量/g |
产物PVAc重量/g |
转化率/% |
|
醇解反应 |
PVAc加入量/g |
产物聚乙烯醇重量/g |
转化率/% |
|
六、思考题
1、影响聚合速度、醇解反应以及产物的转化率的主要因素是什么?如何控制这些不利因素?
2、参加反应的各组份的作用是什么?
3、你对本实验有何改进建议?
-
实验三 醋酸乙烯酯的溶液聚合
高分实验三子化学实验报告醋酸乙烯酯的溶液聚合醋酸乙烯酯的溶液聚合一实验目的1学习水溶液的聚合方法制备醋酸乙烯酯溶液2了解水溶液聚合…
-
实验五 醋酸乙烯酯的溶液聚合
高分子化学实验报告08高分子材料与工程1班刘奕杉0814121024刘莹0814121025醋酸乙烯酯的溶液聚合实验目的1通过聚醋…
-
实验三:醋酸乙烯酯的溶液聚合
高分子实验三醋酸乙烯酯的溶液聚合化学实验报告一实验目的通过聚醋酸乙烯酯的制备掌握溶液聚合的一般方法和基本实验技巧二实验原理通过实验…
-
实验四:醋酸乙烯酯的乳液聚合
高分子化学实验指导河西学院化学化工学院金淑萍博士教授20xx0301目录实验一单体引发剂的纯化3实验二甲基丙酸烯甲酯的本体聚合有机…
-
实验五_醋酸乙烯酯的溶液聚合
高分子化学实验报告08高分子材料与工程1班刘奕杉0814121024刘莹0814121025醋酸乙烯酯的溶液聚合实验目的1通过聚醋…
-
醋酸乙烯酯乳液聚合-白乳胶的制备实验报告
广东工业大学学院专业班组学号姓名协作者教师评定实验题目醋酸乙烯酯乳液聚合白乳胶的制备一实验目的学习聚醋酸乙烯酯白乳胶的合成原理和方…
-
聚醋酸乙烯酯乳胶的合成和乳胶漆的制备预习报告 (2)
实验四聚醋酸乙烯酯乳胶的合成和乳胶漆的制备乳胶漆是一种用途广泛的新型涂料具有价格低廉使用简便耐水性好绿色环保安全无毒等优点其中内墙…
- 醋酸乙烯酯的乳液聚合 实验报告
-
实验3_醋酸乙烯酯的溶液聚合
高分子化学实验报告10高二醋酸乙烯酯的溶液聚合实验三危平福10141220xx丁胜10141220xx20xx58溶液聚合是将单体…
-
实验三 醋酸乙烯酯的溶液聚合
高分实验三子化学实验报告醋酸乙烯酯的溶液聚合醋酸乙烯酯的溶液聚合一实验目的1学习水溶液的聚合方法制备醋酸乙烯酯溶液2了解水溶液聚合…