邻二氮菲分光光度法测定微量铁
邻二氮菲分光光度法测定微量
一、 实验目的:
1、学习确定实验条件的方法,掌握邻二氮菲分光光度法测定微量铁的方法原理;
2、掌握721型分光光度计的使用方法,并了解此仪器的主要构造。
二、 实验原理:
1、在可见分光光度测定中,通常是将被测物质与显色剂反应,使之生成有色物质,然后测其吸光度,进而求得被测物质的含量。因此,显色反应的完全程度和吸光度的测量条件都会影响到测量结果的准确性。通常所研究的显色反应条件有显色温度和时间、显色剂用量、显色剂酸度、干扰物质的影响及消除等。条件试验的一般步骤为改变其中一个因素(比如介质的pH值),暂时固定其他因素,显色后测定相应溶液的吸光度,通过吸光度-pH曲线确定显色反应的适宜酸度范围。
2、根据朗伯-比耳定律:A=εbc,当入射光波长λ及光程b一定时,在一定浓度范围内,有色物质的吸光度A与该物质的浓度c成正比。只要绘出以吸光度A为纵坐标,浓度c为横坐标的标准曲线,测出试液的吸光度,就可以由标准曲线查得对应的浓度值,即未知样的含量。
3、本实验以邻二氮菲为显色剂,选择测定微量铁的适宜显色条件和测量条件,并用于工业盐酸中全铁的测定。邻二氮菲亦称邻菲咯啉(简称phen),是光度法测定铁的优良试剂,在pH 2-9范围内(一般控制在5—6间)邻二氮菲与二价铁生成稳定的红色配合物:
Fe +3 phen = [Fe(Phen)3] 其lgK稳=21.3,最大吸收波长在510nm处,其摩尔吸光系数为
1.1×104L/moL.cm。Fe3+与邻二氮菲作用生成蓝色配合物,lgK稳=14.1,稳
定性较差,因此在实际应用中常加入还原剂盐酸羟胺,使Fe3+还原为Fe2+。其反应式如下:
2 Fe+2 NH2OH·HCl → 2Fe + N2 + H2O + 4H + 2Cl 本方法的选择性很高。相当于含铁量40倍的Sn、AI、Ca、Mg、Zn、Si;20倍的Cr、Mn、V、P和5倍的Co、Ni、Cu不干扰测定。
三、 实验仪器与试剂:
仪器:TU-1901双光束紫外可见分光光度计、1cm玻璃比色皿2个、2mL 吸量
管3个、1mL 吸量管2个、5mL 吸量管1个、50mL 比色管9个 试剂:1.0×10-3 mol·L-1 铁标准溶液、100μg·mL-1铁标准溶液、0.15%邻二氮菲3+2++-2+2+
水溶液(新配)、10% 盐酸羟胺溶液(新配)、1mol·L-1乙酸钠溶液、6 mol·L-1 HCl(工业盐酸试样)
四、 实验步骤:
1、准备工作
打开仪器电源开关,预热,调解仪器。
2、测量工作
(1) 吸收曲线的绘制和测量波长的选择
用吸量管吸取2.00 mL 1.0×10-3mol·L-1铁标准溶液,注入50mL比色管中,加入1.00mL 10%盐酸羟胺溶液,摇匀,加入2.00 mL 0.15%邻二氮菲溶液,5.0 mLNaAc溶液,以水稀释至刻度。在光度计上用1 cm比色皿,采用试剂溶液(去离子水)为参比溶液,在440~560 nm间,每隔10 nm测量一次吸光度(在最大吸收波长处,每隔2nm),以波长为横坐标,吸光度为纵坐标,绘制吸收曲线,选择测量的适宜波长。
(2) 显色剂条件的选择
① 显色剂用量
在6支比色管中,各加入2.00mL 1.0×10-3mol·L-1铁标准溶液和1.00mL 10%盐酸羟胺溶液,摇匀。分别加入0.10、0.50、1.00、2.00 、3.00及4.00mL 0.15%邻二氮菲溶液,5.0 mL NaAc溶液,以水稀释至刻度,摇匀。在光度计上用1cm比色皿,采用去离子水溶液为参比溶液,测吸光度。以邻二氮菲体积为横坐标,吸光度为纵坐标,绘制吸光度-试剂用量曲线,从而确定最佳显色剂用量。
② 溶液pH值
取8支50mL比色管,每只加入2.00mL 1.0×10-3mol·L-1铁标准溶液和1.00mL 10%盐酸羟胺溶液,摇匀。再加入2mL 0.15%邻二氮菲溶液,摇匀。用吸量管分别加入0.0、0.2、0.5、1.0、1.5、2.0、2.5、3.0 mL NaAc溶液,以水稀释至刻度,摇匀。在光度计上用1cm比色皿,采用去离子水为参比溶液,测定吸光度。以NaAc溶液体积为横坐标,吸光度为纵坐标,绘制吸光度-试剂用量曲线,从而确定最佳NaAc溶液用量。
③ 显色时间及有色溶液的稳定性
在50mL比色管中,加入2.00mL 1.0×10-3mol·L-1铁标准溶液和1.00mL 10%盐酸羟胺溶液,2mL 0.15%邻二氮菲溶液和1.5 mL NaAc溶液,以水稀释至刻度,摇匀。立刻在所选择的波长下,用1cm比色皿,采用去离子水溶液为参比溶液,测吸光度。然后放置2、4、6、8min测定其相应的吸光度。绘制吸光度-时间曲线,从曲线确定显色时间。
(3) 工业盐酸中铁含量的测定
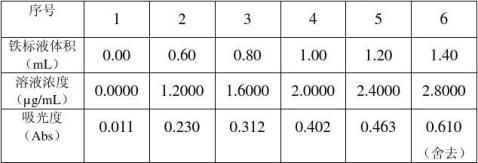
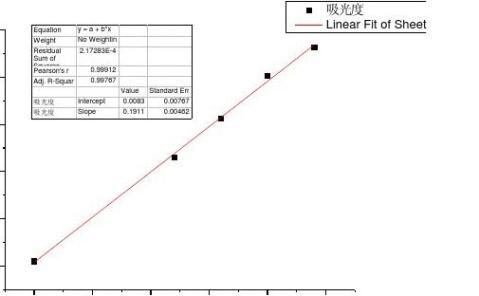
① 标准曲线的制作
在6支50mL比色管中,分别加入0.00、0.60、0.80、1.00、1.20、1.40mL 100μg/mL铁标准溶液,再加入1.00mL 10%盐酸羟胺溶液,2.00mL 0.15%邻二氮菲溶液和1.5 mL NaAc溶液,以水稀释至刻度,摇匀。在510nm处,用1cm比色皿,采用去离子水溶液为参比溶液,测吸光度A。
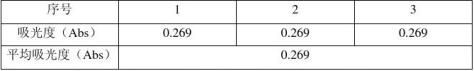
② 试样测定
准确吸取2.0 mL工业盐酸三份,按标准曲线的操作步骤,测定其吸光
度。
五、 数据处理:
1、吸收曲线的绘制和测量波长的选择

0.50
0.45
0.40
0.35
吸光度 (Abs)0.30
0.25
0.20
0.15
0.10
0.05
44046xxxxxxxxxxxx560
波长 (nm)
由图可知,最大吸收波长为510 nm,因此测量的最适宜波长为510nm
2、显色剂用量的选择
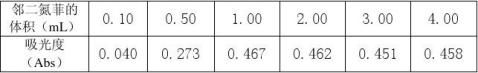
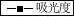
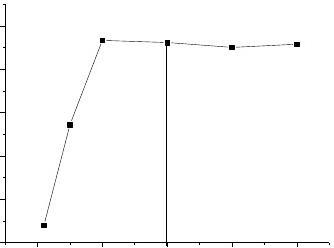
吸光度 (Abs)邻二氮菲的体积 (mL)
由图可知,显色剂邻二氮菲的最佳用量为2mL
3、溶液pH值的选择
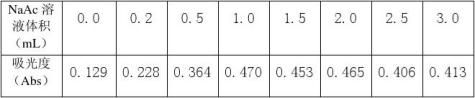

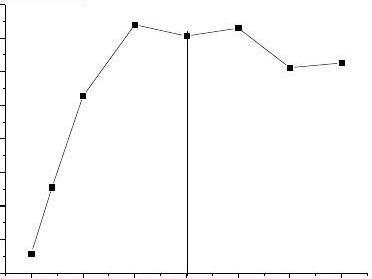
0.500.45

0.400.35
吸光度 (Abs)
0.300.250.200.150.10
NaAc溶液的体积 (mL)
由图可知,加入NaAc的最佳体积为1.5mL
4、显色时间及有色溶液的稳定 确定最佳显色时间为6min 5、标准曲线的绘制
0.50.4
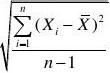
0.3
吸光度 (Abs)0.2
0.1
0.0
溶液浓度 (μg/mL)
标准曲线方程为A=0.19118C+0.0083
相关系数R=0.9991
6、试样测定
即稀释后工业盐酸中铁的含量为1.3640?g/mL
由2×Cx÷50=1.3640,得Cx=34.10?g/mL
误差:S??0
S0?100%??100%?0 A0.269相对误差: RSD?
实验结论:由实验数据可知,最适宜波长为λ=510nm;0.15%邻二氮菲的适宜用
量为2mL;加入乙酸钠的最佳体积为1.5mL;最佳显色时间为6min,
最终由标准曲线求得工业盐酸中铁的含量为:34.10μg/mL。
六、 实验讨论及反思:
讨论:
1、不能颠倒各种试剂的加入顺序;
2、比色皿在换装不同浓度的溶液时,必须用待测的溶液润洗;
3、比色皿放入分光光度计样品室前,必须用滤纸将表面擦拭干净;
4、影响实验成败的关键可能有:样品液的配置不准、分光光度计使用不当。 反思:
每次移液前都应认真读取移液管的量程,以防移取错误;加入试剂要按照顺序,配制溶液一定要标准,不然会产生很大的误差;每次的比色管都应清洗干净。
第二篇:邻二氮氮菲分光光度法测定试样中的微量铁








-
综合实验报告 邻二氮菲分光光度法测定微量铁
邻二氮菲分光光度法测定微量铁一实验目的学习确定实验条件的方法掌握邻二氮菲分光光度法测定微量铁的方法原理掌握721型分光光度计的使用…
-
邻二氮菲分光光度法测定微量铁实验报告
邻二氮菲分光光度法测定微量铁课程名称仪器分析指导教师李志红实验员张丽辉李国跃崔凤琼刘金旖普杰飞赵宇时间20xx年5月12日一实验目…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁20xx级医学检验3组吴茳铃20xx221885实验目的和要求1掌握紫外可见分光光度计的基本操作…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁一实验目的和要求1掌握紫外可见分光光度计的基本操作2掌握邻二氮菲分光光度法测定微量铁的原理和方法…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁实验目的和要求1掌握紫外可见分光光度计的基本操作2掌握邻二氮菲分光光度法测定微量铁的原理和方法3…
-
邻二氮菲分光光度法测定微量铁实验报告
邻二氮菲分光光度法测定微量铁课程名称仪器分析指导教师李志红实验员张丽辉李国跃崔凤琼刘金旖普杰飞赵宇时间20xx年5月12日一实验目…
-
综合实验报告 邻二氮菲分光光度法测定微量铁
邻二氮菲分光光度法测定微量铁一实验目的学习确定实验条件的方法掌握邻二氮菲分光光度法测定微量铁的方法原理掌握721型分光光度计的使用…
-
邻二氮菲分光光度法测定微量铁实验报告
实验一邻二氮菲分光光度法测定微量铁实验目的和要求1掌握紫外可见分光光度计的基本操作2掌握邻二氮菲分光光度法测定微量铁的原理和方法3…
-
邻二氮菲分光光度法测定微量铁
邻二氮菲分光光度法测定微量铁一实验目的1学习确定实验条件的方法掌握邻二氮菲分光光度法测定微量铁的方法原理2掌握TU19xx分光光度…
-
邻二氮菲分光光度法测定水中微量铁
邻二氮菲分光光度法测定微量铁一实验目的1学会吸收曲线及标准曲线的绘制了解分光光度法的基本原理2掌握用邻二氮菲分光光度法测定微量铁的…