医疗器械二类备案注册表附件4
附件4
第二类医疗器械经营备案表
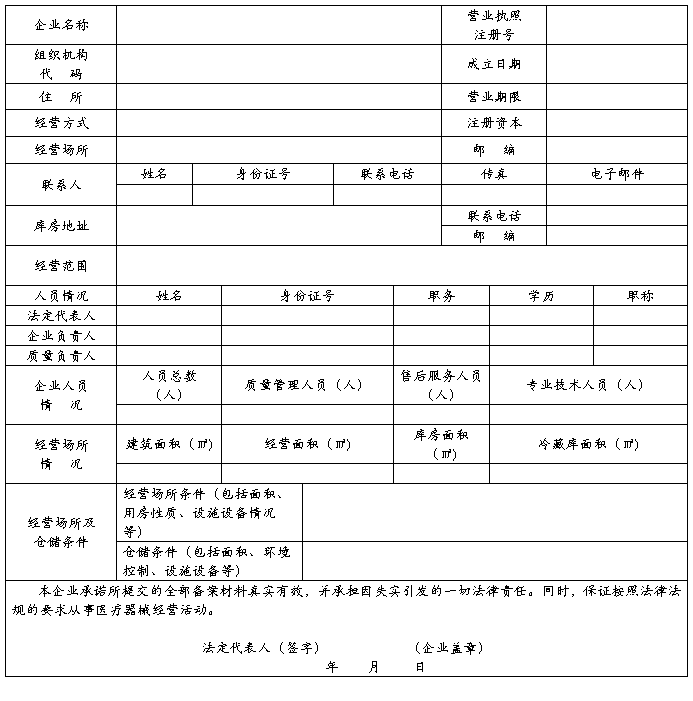
填 表 说 明
一、本表按照实际内容填写,不涉及的可缺项。其中,企业名称、营业执照注册号、住所、法定代表人、注册资本、成立日期、营业期限等按照营业执照内容填写。
二、本表经营范围应当按照国家食品药品监督管理总局颁布的医疗器械分类目录中规定的管理类别、分类目录类代号和类代号名称填写。
三、本表经营方式指批发、零售、批零兼营。
四、本表应使用A4纸双面打印,不得手写。
附件5
第二类医疗器械经营备案材料要求
1.第二类医疗器械经营备案表;
2.企业营业执照复印件;
3.企业法定代表人或者负责人、质量负责人的身份、学历、职称证明复印件;
4.企业组织机构与部门设置说明;
5.企业经营地址、库房地址的地理位置图、平面图(注明实际使用面积)、房屋产权证明文件或者租赁协议(附房屋产权证明文件)复印件;
6.企业经营设施和设备目录;
7.企业经营质量管理制度、工作程序等文件目录;
8.经办人授权证明;
9.其他证明材料。
备案材料应完整、清晰,使用A4纸打印装订并附有目录,复印件加盖公章后与电子版一并提交。
第二篇:第一类医疗器械产品备案和二类经营备案的相关措施
第一类医疗器械产品备案和二类经营备案的相关措施
摘要:新《医疗器械监督管理条例》分别对第1类医疗器械产品备案、生产备案和第2类医疗器械经营备案的具体要求和操作规范做了明确的规定,区别于与旧法规276号令中规定的1类产品注册、1类生产备案和2类经营许可。
新《医疗器械监督管理条例》已于20xx年6月1日正式实施,按照医疗器械产品的风险放宽了一类产品,为此国家食品药品监督管理总局20xx年05月30日先后发布了20xx年第26号、第25号公告,分别对第1类医疗器械产品备案、生产备案和第2类医疗器械经营备案的具体要求和操作规范做了明确的规定,区别于与旧法规276号令中规定的1类产品注册、1类生产备案和2类经营许可。
针对国家局发布的公告,各省市也在近期陆续出台了相关措施。从新法规了解到,一类医疗器械注册审评阶段的30个工作日缩短为只要资料合格可以当场备案,缩短了办理时间、简化了产品备案的程序。
国家局发布的26号公告,1类产品备案需要增加的资料:风险分析报告、临床评价资料、最小销售单元标签设计样稿、生产制造信息,从需要递交资料的内容和数量上都可见备案的难度在增加。从各市局发布的办事指南也了解到,1类医疗器械备案需要递交的资料要求更为明确,操作规范更为详细,甚至细致到每份文件需要包含的内容、格式和填写要求。
在国家局发布公告后,江苏省最先于20xx年6月9号发布了“关于实施第一类医疗器械生产备案和第二类医疗器械经营备案有关事宜的通知”,对已有资质的一类生产企业换发《生产备案凭证》、二类经营企业换发《第二类医疗器械经营备案凭证》做出了规定,原则上自20xx年6月1日起所有第一类医疗器械生产企业和第二类经营企业均应凭有效《生产备案凭证》和《经营许可备案凭证》开展第一类医疗器械生产活动和第二类医疗器械经营活动。但对新企业的开办并无具体的办事指南。同时,南京市局在6月9号宣布暂停办理一类产品备案,并申明会在近期出台具体的办理程序,截止目前并未见公布。其他市级药监局也在长达20多天的磨合期和商讨后陆续出台了新的办事指南,有上海市、东莞市、珠海市、中山市、深圳市、杭州市、佛山市一类生产和产品备案,二类经营备案。其中上海市对一类产品备案的申报材料的内容要求和格式进行了详细规定。其余各市食药监管局仍在制订中,从多个食药监局了解到,对于新的细则的出台,市食药监管局经过了多次会议的研讨,对新的细则的制订给予了高度重视,新的办事指南也将更加规范。
-
第二类医疗器械经营备案表
第二类医疗器械经营备案表填表说明一本表按照实际内容填写不涉及的可缺项其中企业名称营业执照注册号住所法定代表人注册资本成立日期营业期…
-
第二类医疗器械经营备案申报资料模板
申办第二类医疗器械经营备案申请材料XXXXXXXXXXXX企业名称XXXX年XX月XX日联系电话XXXXXXXXXXX目录1第二类…
-
二类医疗器械备案申请资料模板
申办二类医疗器械经营企业备案申请材料有限公司年月日联系电话申请材料目录1医疗器械经营企业备案申请表2营业执照副本复印件3公司章程4…
-
第二类医疗器械备案表
附件4第二类医疗器械经营备案表4填表说明一本表按照实际内容填写不涉及的可缺项其中企业名称营业执照注册号住所法定代表人注册资本成立日…
-
第二类医疗器械经营备案表20xx0425
枣庄浩翔医疗器械有限公司医疗器械经营许可证申报材料目录1医疗器械经营经营许可申请表一份2企业营业执照正副本和企业组织机构代码证正副…
-
二类医疗器械备案材料示范文本
示范文本说明本示范文本内容请根据市级情况填写不可生搬硬套不适用或无相应内容请填医疗器械经营企业许可证备案材料市健康医疗器械有限公司…
-
第二类医疗器械经营备案申报资料模板
申办第二类医疗器械经营备案申请材料XXXXXXXXXXXX企业名称XXXX年XX月XX日联系电话XXXXXXXXXXX目录1第二类…
-
二类医疗器械备案申请资料模板
申办二类医疗器械经营企业备案申请材料有限公司年月日联系电话申请材料目录1医疗器械经营企业备案申请表2营业执照副本复印件3公司章程4…
-
第二类医疗器械经营备案表
第二类医疗器械经营备案表填表说明一本表按照实际内容填写不涉及的可缺项其中企业名称营业执照注册号住所法定代表人注册资本成立日期营业期…
-
第二类医疗器械经营备案表20xx0425
枣庄浩翔医疗器械有限公司医疗器械经营许可证申报材料目录1医疗器械经营经营许可申请表一份2企业营业执照正副本和企业组织机构代码证正副…