篇一 :《分析化学实验》总结
定量分析是一门实验性课程,通过分析化学实验可以是我们对分析学化学基本理论进一步加深理解,并能够熟练地掌握定量分析的基本操作技能,为我们将来参加工业生产和科学研究打下良好的基础,为我们以后的社会工作和社会实践做准备。
分析化学实验是分析化学课的重要组成部分,其目的在于加强学生对分析化学基本概念、基本理论的理解,训练学生分析化学的基本操作技能,掌握基础和现代分析化学技术,为后继学习及将来工作打下坚实基础。因此,分析化学实验的教学十分重要,必须予以重视。分析化学是一门非常注重学生动手能力的学科,它异于其他实践课程的要求就决定了我们对待它不同于别的科目。它要求我们在试验中要有认真、仔细、严谨的态度。
分析化学是基础化学实验的一部分,分析化学在整个分析化学教学环节中占有重要的地位,不仅要使学生加深对基本理论和概念的理解,训练学生熟练的实验技能,更重要的是培养学生的创新素质和创新能力。但是在实验教学中任然存在着许多弊端。诸如:验证性的实验较多,而研究性的实验较少;学生仅满足于按照实验指导书按部就班的进行实验;实验考试只限于实验报告的优劣,实验技能的好坏以及实验理论的考试。这些问题已经制约着学生创新意识和创新能力的培养和优秀人才的脱颖而出,迫切需要改变。
…… …… 余下全文
篇二 :分析化学(第六版)总结
分析化学(第六版)总结
第一章 绪论
第一节 分析化学及其任务和作用
定义:研究物质的组成、含量、结构和形态等化学信息的分析方法及理 论的科学,是化学学科的一个重要分支,是一门实验性、应用性很强的学科
第二节 分析方法的分类
一、按任务分类
定性分析:鉴定物质化学组成(化合物、元素、离子、基团)
定量分析:测定各组分相对含量或纯度
结构分析:确定物质化学结构(价态、晶态、平面与立体结构)
二、按对象分类:无机分析,有机分析
三、按测定原理分类
(一)化学分析
定义:以化学反应为为基础的分析方法,称为化学分析 法.
 分类: 定性分析
分类: 定性分析
 重量分析:用称量方法求得生成物W重量
重量分析:用称量方法求得生成物W重量
定量分析
…… …… 余下全文
篇三 :分析化学总结
第一章
系统误差的性质:由固定原因造成的,有单向性特征,通过数理统计的方法不能除去。
系统误差的来源:仪器、试剂、实验方法、实验操作
系统误差的解决办法:针对仪器的要校准仪器;针对试剂的要做空白试验,因实验方法而带来系统误差的要改进实验方法或重新选定实验方法。
随机误差具有偶然性,随机性,也是必然存在的,随机误差只能通过多次平行实验来减小随机误差
在没有系统误差的情况下,无限次平行测定结果的平均值等于真值。
在没有系统误差的情况下,无限次平行测定结果的随机误差遵循正态分布规律,有限次的采用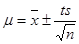 来处理。
来处理。
为了检验两组数据之间的精密度是否有显著性差异,用F检验
为了检验平均值和真值或标准值之间是否显著性差异,用t检验。
为了考察两组数据之间显著性差异,先用F检验,后用t检验。F检验不合格就不用t检验,只有F检验合格了才可以进行t检验。
处理数据要注意四舍六入五成双
计算平均值时要注意可疑值的取舍,取舍有两种方法,Q值检验法和4d法。会计算标准偏差以及置信区间。
第二章 酸碱滴定法
…… …… 余下全文
篇四 :分析化学实验思考题总结
实验一 煤气灯的使用和玻璃工操作
1. 正常的煤气灯火焰,各焰层的大概温度为多少?被加热的物体应放在哪一层?(题目加黑)
答:焰心(内层)温度约573K左右;还原焰(中层)温度较焰心高;氧化焰(外层)温度最高,约1073~1173K。实验时,被加热物体一般都用氧化焰来加热,根据需要可调节火焰的大小。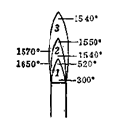
(留一个空)
2.使用煤气灯时,什么情况下会出现临空火焰和侵入火焰?出现这种情况如何处理?
答:如果煤气和空气的进入量都调节得很大,则点燃煤气后火焰在灯管的上空燃烧,移去点燃所用的火柴时,火焰也自行熄灭,这样的火焰称为“临空火焰”。 如果煤气的进入量很小,而空气的进入量很大时,煤气将在灯管内燃烧,管口会出现一缕细细的呈青色或绿色的火焰,同时有特色的“嘘嘘”声响发出,这样的火焰称为“侵入火焰”。 遇到这些不正常的火焰,应立即关闭煤气开关,重新调节和点燃煤气。
3.选择瓶塞有什么要求?试比较玻璃磨口塞、橡皮塞和软木塞各有哪些优缺点。
答:塞子的大小应与仪器的口径相适合,塞子塞进瓶口或仪器口的部分不能少于塞子本身高度的1/2,也不能多于2/3。瓶塞的种类应根据所装化学品的化学性质来选择。软木塞易被酸、碱所损坏,但与有机物作用较小。橡皮塞可以把瓶子塞得很严密,并可以耐强碱性物质的侵蚀,但容易被强酸和某些有机物质(如汽油、苯、氯仿、丙酮、二硫化碳等)所侵蚀。玻璃磨口塞子把瓶子也塞得很严,它适用于除碱和氢氟酸以外的一切盛放液体或固体物质的瓶子。
…… …… 余下全文
篇五 :《化学分析技术实训》
目 录
实验一 不同成分混合碱含量的测定…………………………… 3
实验二 不同品牌矿泉水中钙镁含量的测定…………………… 5
实验三 不同品牌维生素中维C含量的测定……………………7
实验一 不同成分混合碱含量的测定
一、实验目的
1、了解双指示剂法测定混合碱成分的原理;
2、了解双指示剂的使用及其优点;
3、掌握双指示剂法操作方法。
二、实验原理
混合碱系是指Na2CO3、NaOH、NaHCO3的各自混合物及类似的混合物。但不存在NaOH和NaHCO3的混合物。
0.1mol/L的NaOH、Na2CO3、NaHCO3溶液的pH分别为:13.0、11.6、8.3,用0.1mol/L HCl分别滴定0.1mol/L NaOH、Na2CO3、NaHCO3溶液时,如果以酚酞为指示剂,酚酞的变色范围为8~10,因此,NaOH、Na2CO3可以被滴定,NaOH转化为NaCl,Na2CO3转化为NaHCO3,为第一终点;而NaHCO3不被滴定,当以甲基橙(3.1~4.3)为指示剂时,NaHCO3被滴定转化为NaCl为第二终点。
…… …… 余下全文
篇六 :分析化学(第六版)总结
分析化学(第六版)总结
第一章 绪论
第一节 分析化学及其任务和作用
定义:研究物质的组成、含量、结构和形态等化学信息的分析方法及理 论的科学,是化学学科的一个重要分支,是一门实验性、应用性很强的学科
第二节 分析方法的分类
一、按任务分类
定性分析:鉴定物质化学组成(化合物、元素、离子、基团)
定量分析:测定各组分相对含量或纯度
结构分析:确定物质化学结构(价态、晶态、平面与立体结构)
二、按对象分类:无机分析,有机分析
三、按测定原理分类
(一)化学分析
定义:以化学反应为为基础的分析方法,称为化学分析 法.
 分类: 定性分析
分类: 定性分析
 重量分析:用称量方法求得生成物W重量
重量分析:用称量方法求得生成物W重量
定量分析
…… …… 余下全文
篇七 :分析化学实验的总结 填空题
1.测定一物质中某组分的含量,测定结果为(%):59.82,60.06,59.86,60.24。则平均偏差为 0.16 % ;相对平均偏差为 0.26% ;标准偏差为0.20%;相对标准偏差为 0.33% ;置信区间为 (60.00±0.32)% ( )
3.滴定管的读数常有±0.01mL的误差,则在一次滴定中的绝对误差可能为 ±2 mL。常量滴定分析的相对误差一般要求应≤0.1%,因此,滴定时消耗标准溶液的体积必须控制在 20 mL以上。
4.从误差的基本性质来分,可以将它分为 随机误差 、 系统误差、 过失量误差 。
5.NH4CN质子条件为 [HCN]+[H+]=[OH—]+NH3
7.六次甲基四胺的pKb=8.85,用它配制缓冲溶液时的pH范围是 5.15±1
9.在含有Ca2+、Ag2+混合溶液中,在pH=12条件下,用EDTA标准溶液滴定其中的Ca2+。加入三乙醇胺的作用是 掩蔽Fe3+、Al3+,加入NaOH的作用是掩蔽Mg2+,使之形成Mg(OH)2
…… …… 余下全文
篇八 :无机与分析化学实验课总结
无机与分析化学实验总结
转眼间,一个学期的实验课已经结束了。现在回想起来,在化学实验课上,真的收获了很多。这些收获也不仅仅是学会了一些化学实验的操作,对很多元素的性质有了更深的理解,更重要的是学会了严谨,学会了提前准备,学会了合作,学会了思考,学会了自己探究……这些都将在我以后的学习和生活中有很重要的意义。
最重要的一点是严谨,做实验时要做到一丝不苟。还记得第一次进入实验室看到的情景,整齐的仪器、药品摆放,一尘不染的桌面,各种事故处理的器材……我深深意识在这个实验室里是不容许有一点马虎的。这一点尤其体现在做分析实验上,做分析实验是要严格按照标准操作来的。称量、滴定、移液、定容……每一个地方都要足够细心,足够严谨,很多时候会做得慢,如果有时候追求速度,就很容易出现实验数据不准确或者几次数据的偏差很大的情况。还记得第一次做滴定实验时,由于在终点附近对液滴控制不够熟悉,也有想快一点完成实验的想法,导致前两次滴定都滴过了终点,只能重新滴定。后来虽然终点可以控制的很好,结果也很准确,但由于怕滴过了所以整个过程特别慢。在熟练了几次后,心中就有了正确判断滴定快到终点的那种感觉,整个过程就变得流畅多了。我深深体会到了做分析实验时是一点也马虎不得的。分析实验的任何一个失误都有可能导致结果与正确结果相差很多。也许我们当时偷懒了,也许我们当时走神了,如果我们带着这样的失误走向了结果,那么等待我们的很可能就是误差很大的实验结果,或者是要重新完成实验操作内容。
…… …… 余下全文