电导的测定及应用实验报告
实验名称 电导的测定及其应用
一、实验目的
1.测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率;
2.用电导法测量醋酸在水溶液中的解离平衡常数;
3.掌握恒温水槽及电导率仪的使用方法。
二、实验原理
 1、电导G:对于电解质溶液,常用电导表示其导电能力的大小。电导G是电阻R的倒数,即 G=1/R。电导的单位是西门子,常用S表示。1S=1Ω-1
1、电导G:对于电解质溶液,常用电导表示其导电能力的大小。电导G是电阻R的倒数,即 G=1/R。电导的单位是西门子,常用S表示。1S=1Ω-1
2、电导率或比电导:κ=Gl/A (2.5.1)
其意义是电极面积为及1m2、电极间距为lm的立方体导体的电导,单位为S·m-1。
对电解质溶液而言,令l/A = Kcell,Kcell称为电导池常数。
所以 κ=G l/A =G Kcell
3、摩尔电导率:Λm=κ/ C (2.5.2)
强电解质稀溶液的摩尔电导率Λm与浓度有如下关系:
Λm= Λ∞m- A (2.5.3)
(2.5.3)
Λ∞m为无限稀释摩尔电导率。可见,以Λm对 作图得一直线,其截距即为Λ∞m。
作图得一直线,其截距即为Λ∞m。
弱电解质溶液中。在无限稀释的溶液中可认为弱电解质已全部电离。此时溶液的摩尔电导率为 Λ∞m =V+ Λm ,+ + V- Λm ,- (2.5.4)
根据电离学说,可以认为,弱电解质的电离度α等于在浓度时的摩尔电导Λ与溶液在无限稀释时的电导Λ∞m之比,即:α=Λm/Λ∞m (2.5.5)
4、弱电解质电离平衡常数:弱电解质AB型的电离平衡常数:Kθ=(Cα2)/Cθ(1-α) (2.5.6)
所以,通过实验测得α即可得Kθ值。
把(2.5.4)代入(2.5.6)式可得
Kθ=(CΛ∞m2)/ Λ∞mCθ(Λ∞m-Λm) (2.5.7)
或 CΛm=(Λ∞m2) KθCθ1/Λm -Λ∞mKθCθ
以CΛm对1/Λm作图,其直线的斜率为(Λ∞m2) KθCθ,如知道Λ∞m值,就可算出Kθ。
三、实验仪器、试剂
仪器:梅特勒326电导率仪1台;电导电极一只,量杯(50mL)2个;移液管(25mL)3只;
洗瓶一只;洗耳球一只。
药品:10.00(mol/m3)KCl溶液;0.093mol/dm3)HAc溶液;电导水。
四、实验步骤
1.打开电导率仪开关,预热5min。
2.KCl溶液电导率的测定:
(1)用移液管准确移入10.00(mol/m3)KCl溶液25.00mL,至于洁净、干燥的量杯中;测定
其电导率3次,取平均值。
(2)再用移液管准确移入25.00mL电导水,置于上述量杯中;搅拌均匀后,测定其电导率3
次,取平均值。
(3)再用移液管准确移出25.00mL上述量杯中的溶液,弃去;再用移液管准确移入25.00mL
电导水,置于上述量杯中;搅拌均匀后,测定其电导率3次,取平均值。
(4)重复(3)的步骤。
(5)重复(3)的步骤。
(6)倾去电导池中的KCl溶液,用电导水洗净量杯和电极;量杯放回烘箱;电极用滤纸吸干。
3.HAc溶液和电导水的电导率的测定:
(1)用移液管准确移入0.093(mol/dm3)KCl溶液25.00mL,至于洁净、干燥的量杯中;测定
其电导率3次,取平均值。
(2)再用移液管准确移入25.00mL已恒温的电导水,置于上述量杯中;搅拌均匀后,测定其
电导率3次,取平均值。
(3)再用移液管准确移出25.00mL上述量杯中的溶液,弃去;再用移液管准确移入25.00mL
电导水,置于上述量杯中;搅拌均匀后,测定其电导率3次,取平均值。
(4)再用移液管准确移出25.00mL上述量杯中的溶液,弃去;再用移液管准确移入25.00mL
电导水,置于上述量杯中;搅拌均匀后,测定其电导率3次,取平均值。
(5)倾去电导池中的HAc溶液,用电导水洗净量杯和电极;然后注入电导水,测定其电导率
3次,取平均值。
(6)倾去电导池中的电导水,用电导水洗净量杯和电极;量杯放回烘箱;电极用滤纸吸干。
五、数据记录与处理
1.数据记录
大气压:101.10KPa 室温:25.2℃ 实验温度:25.2℃
已知数据:25℃下10.00(mol/m3)KCl溶液电导率=0.1413S·m-1;25℃时无限稀释的HAc水溶液的摩尔电导率=3.907×10-2(S·m2·mol-1)。
(1)测定KCl溶液的电导率:
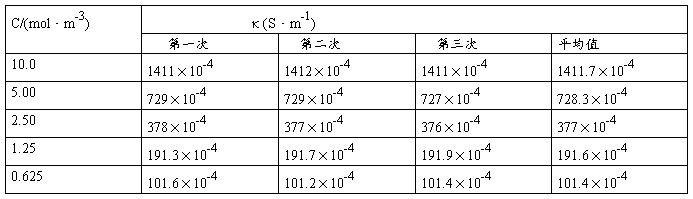
(2)测定HAc水溶液的电导率:
电导水的电导率κ=(H2O)/(S·m-1)=8.90×10-4

2.数据处理
(1)KCl溶液的各组数据
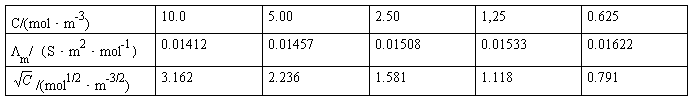
以KCl溶液的Λm对 作图得一直线,其截距即为KCl的Λ∞m。
作图得一直线,其截距即为KCl的Λ∞m。
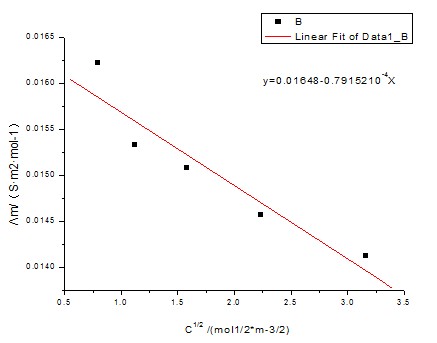
由图可知斜率为-7.98152×10-4,截距为0.01648
由Λm= Λ∞m- A 得出Λ∞m= 0.01648S·m2·mol-1
得出Λ∞m= 0.01648S·m2·mol-1
(2)HAc溶液的各组数据
HAc原始浓度:0.093mol/L
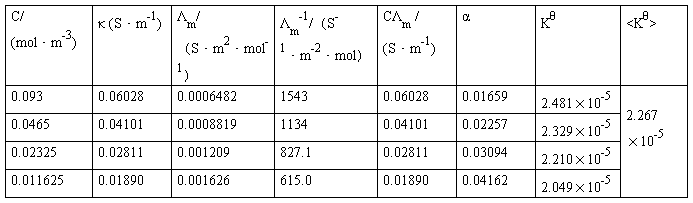
κ = κ′-κH2O
以CΛm对1/Λm作图,其直线的斜率为(Λ∞m2) KθCθ,如知道Λ∞m值,就可算出Kθ,并与上述结果进行比较。
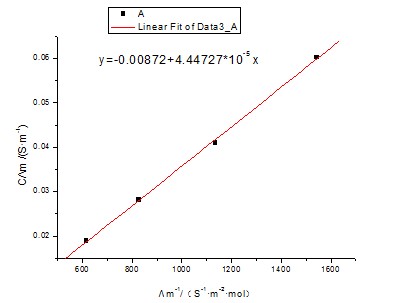
由图可知此直线的斜率为4.44727×10-5,所以(Λ∞m)2 KθCθ=4.44727×10-5,
又因为Λ∞m=3.907×10-2(S·m2·mol-1),Cθ=1mol/L;
所以Kθ=4.1963×10-5/((3.907×10-2)2×1×1000)=2.749×10-5
实验计算所得结果相对图得到的结果的相对误差=(2.749×10-5-2.267×10-5)×100%=17.5%
六、结果与讨论
误差分析:
1、 移液管使用时存在误差,使得溶液浓度非理想浓度;
2、 更换待测液时,电导率仪的电极与未洗干净或未擦干,导致误差;
3、 电导水的电导率的测定误差;
4、 移液管操作时没有进行搅拌。
有关已知数据:25℃下0.01000mol/L KCl溶液电导率К =0.1413 S·m-1 无限稀的HAc水溶液的摩尔电导率(25℃)∧∞m=3.907×10-2S·m2·mol-1
第二篇:实验报告 电导法测定乙酸乙酯皂化反应的速率常数
电导法测定乙酸乙酯皂化反应的速率常数实验目的1.掌握电导法测定反应速率常数的原理和方法2.了解二级反应的特点,学会用图解计算法求取二级反应的速率常数3.用电导法测定乙酸乙酯皂化反应的速率常数,了解反应活化能的测定方法实验原理乙酸乙酯皂化是一个二级反应,其反应式为:反应速率方程为:在反应过程中,各物质的浓度随时间而变。测定该反应体系组分浓度的方法很多,例如,可用标准酸滴定测出不同时刻OH-离子的浓度。本实验使用电导率仪测量皂化反应进程中体系电导值G随时间的变化,可以监测反应的进程,进而可求算反应的速率常数。二级反应的速率与反应物的浓度有关。若反应物和的初始浓度相同(均设为c),设反应时间为t时,反应所产生的和的浓度为x,若逆反应可忽略,则反应物和产物的浓度时间的关系为:t=0: c c o ot=t: c-x c-x x x上述二级反应的速率方程可表示为:..........(1)作积分得:或 .........(2)显然,只要测出反应进程中任意时刻t时的x值,再将已知浓度c代入上式,即可得到反应的速率常数k值.因反应物是稀水溶液,故可假定全部电离.则溶液中参与导电的离子有Na+、OH-和等,Na+在反应前后浓度不变,OH-的迁移率比的大得多.随着反应时间的增加,OH-不断减少,而不断增加,所以体系的电导值不断下降.在一定范围内,可以认为体系电导值的减少量与的浓度x的增加量成正比,即:…….(3)…….(4)式中, 和分别是溶液起始和t时的电导值, G∞为反应终了时的电导值,β是比例系数.将(3)、(4)代入(2)得:.........( 5)或写从直线方程式可知,只要测出G0、G∞和一组值,据(11.5)式,由对t作图,应得一直线,从其斜率即可求得速率常数k值.实验仪器与试剂DDS-307型数字电导率仪 1台 双管电导池 1个移液管(10 mL) 2支 DJS-1型铂黑电极 1支洗耳球 1只 (0.0100、0.0200 mol/L) 一瓶CH3COONa(0.0100 mol/L) 一瓶 CH3COOC2H5(0.0200 mol/L) 一瓶实验步骤本实验用烧杯作电导池,如下:1. G0的测定(1)洗净烧杯并烘干,倒入适量0.0100 mol/L溶液(以能浸没铂黑电极并高出1cm为宜)。(2)用电导水洗涤铂黑电极,再用0.0100 mol/L 溶液淋洗,然后置入烧杯中。(3)测量溶液的电导(率)值,每隔2 min测量一次,共3次。2.G∞的测定 实验测定过程不可能进行到t=∞,且反应也并不完全可逆,故通常以0.0100 mol/L 的溶液的电导(率)值作为G∞,测量方法与G0的测量方法相同。
但必须注意,每次更换测量溶液时,须用电导水淋洗电极和烧杯,再用被测溶液淋洗三次。3.Gt的测定(1)电导池和电极的处理方法与上述相同,装后置烧杯中.(2)用移液管量准确取10 mL 0.0200 mol/L 溶液放入洗净并干燥的烧杯, 用另一支移液管吸取10 mL 0.0200 mol/L 溶液注入烧杯中。(3)将CH3COOC2H5溶液快速倒入烧杯中,溶液倒入一半时,开始记时,并继续倒完,使溶液混合均匀,并立即测量溶液的电导(率)值.注意不要使溶液逸出!(4)每隔2 min测量一次,直至电导(率)值基本不变为止。除记录第一个数据的外,其它各数据在测量时,应该尽量保持在整数分钟时测定,以便于进行数据处理。整个反应约需时45 min~1 h。(5)反应结束后,倒掉反应液,洗净烧杯和电导电极.实验数据记录及处理表一:t/min246/ 1948194619411945表二:t/min2461312131713181315.67表三:t/min246810121416177917401697165816321583155115210.35830.48310.65040.83840.98951.35411.67422.0697t/min1820222xxxxxxxxxxxx14851455144614301418139913822.43282.71663.51683.82814.50455.15006.55238.4879根据测试结果,以对t作图:直线的斜率0.1756,则k=17.56所以反应速率常数实验小结1 .本实验要在恒温条件下进行,且和溶液在混合前还要预先恒温是因为温度对反应速率常数K影响很大,故反应过程应在恒温条件下进行,本实验是在室温下下进行。2.反应分子数与反应级数是两个完全不同的概念,反应级数只能通过实验来确定。试问如何从实验结果来验证乙酸乙酯皂化反应为二级反应?答:利用不同浓度下的乙酸乙酯和氢氧化钠,来测定相同反应条件下的不同浓度的反应物的反应速率。3.乙酸乙酯的皂化反应为吸热反应,试问在实验过程中如何处置这一影响而是使实验得到较好的结果?答:采用稀溶液控制反应速率,并适当搅拌。4.如果和溶液均为浓溶液,试问能否用此方法求得K值?为什么?答:不能。因为影响因素太多,实验结果更差。5.为什么两溶液混合一半是就开始计时?答:因为溶液要尽快混合,而且反应速率较快,电导率也下降较快,所以加入一半时,就开始计时。
-
电导的测定及其应用实验报告
电导的测定及其应用一、实验目的1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。2、用电导法测量醋酸在水溶液中的解离平衡常…
-
电导的测定及应用实验报告
实验名称一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电…
-
电导的测定及其应用实验报告
电导的测定及其应用一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒…
-
电导的测定及其应用实验报告wqf
宁波工程学院物理化学实验报告专业班级姓名序号同组姓名指导老师实验日期3月31号实验名称实验五电导的测定及其应用一实验目的1测量KC…
-
电导的测定及其应用实验报告
001520015000148YAxisTitle00146001440014200140XAxisTitle根据截距即为得154…
-
电导的测定及其应用实验报告wqf
宁波工程学院物理化学实验报告专业班级姓名序号同组姓名指导老师实验日期3月31号实验名称实验五电导的测定及其应用一实验目的1测量KC…
-
电导的测定及其应用实验报告
电导的测定及其应用一实验目的1测量KCl水溶液的电导率求算它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒…
-
物化实验报告5-电导的测定及其应用
一实验目的1测量KCl水溶液的电导率求它的无限稀释摩尔电导率2用电导法测量醋酸在水溶液中的解离平衡常数3掌握恒温水槽及电导率仪的使…
-
电导的测定及其应用实验报告
电导的测定及其应用一、实验目的1、测量KCl水溶液的电导率,求算它的无限稀释摩尔电导率。2、用电导法测量醋酸在水溶液中的解离平衡常…
-
实验五:电导率的测定及其应用
宁波工程学院物理化学实验报告专业班级化本092姓名周培实验日期20xx年4月14日同组姓名徐浩郑志浩指导老师刘旭峰王婷婷实验名称实…
-
物化实验报告7-电动势的测定及应用
一实验目的1通过实验加深对可逆电池可逆电极盐桥等概念的理解2掌握对消法测定电池电动势的原理及电位差计的使用方法3通过电池AgAgN…