制备环己酮肟的实验
50.设计合成实验的原理和步骤。
一、以环已酮和盐酸羟胺为主要原料
【实验原理】
2 NH2OH·HCl (盐酸羟胺) + Na2CO3→NH2OH+2NaCl+ H2O +CO2

本实验以环已酮和盐酸羟胺为主要原料来制备环己酮肟。羟胺在酸性条件下稳定,因此常常做成稳定的盐酸羟胺。但是本反应中制得的环己酮肟酸性条件下不稳定易分解,在碱性环境下稳定,所以本实验的反应环境是碱性环境。
本实验中碳酸钠要过量,原因是:(1)提供碱性环境,使生成物环己酮肟稳定(2)碳酸钠弱碱性,起中和作用,使羟胺从盐酸羟胺中游离出来,与环己酮进行反应。
本实验中盐酸羟胺过量要过量,原因是:若环己酮过量,环己酮和环己酮肟的后处理比较复杂,难以提纯目的产物。
【实验步骤】
1、先在锥形瓶中加水溶解适量盐酸羟胺,再加入环己酮肟混合均匀,后将碳酸钠碱液缓慢滴加到混合液中反应,直至溶液显碱性为止。观察并记录实验现象。
2.不断搅拌,反应过程中会产生大量的CO2产生并伴有白色固体析出。用TLC跟踪反应进程,直至反应完全。
3.间歇振荡15min后用冰水浴冷却。有更多白色固体析出。
4、把产物抽滤称重并记录实验数据,后把粗产物反复洗涤、过滤2-3次后再用乙醇重结晶可得纯品环己酮肟。
5、计算理论值和收率。对本次实验进行理论分析和数据分析,得出结论。
二、环已酮和氨水、双氧水为主要原料
【实验原理】
C6H5O(环己酮)+NH3.H2O+H2O2→2H2O +C6H5=NOH(环己酮肟)
本实验以环已酮和和氨水、双氧水为主要原料来制备环己酮肟。羟胺在酸性条件下稳定,因此常常做成稳定的盐酸羟胺。但是本反应中制得的环己酮肟酸性条件下不稳定易分解,在碱性环境下稳定,所以本实验的反应环境是碱性环境,要加入氨水。
NH3.H2O、H2O2过量理由:1、提供碱性环境 2、NH3.H2O、H2O2过量,产物容易分离。若环己酮过量,若环己酮过量,环己酮和环己酮肟的后处理比较复杂,难以提纯目的产物。
【实验步骤】
1、先搭好回流装置,取一定量的环己酮、氨水、双氧水加入单口烧瓶中,混合均匀后在一定温度下反应,观察并记录实验现象。
2、不断搅拌,反应过程中会产生大量的CO2产生并伴有白色固体析出。用TLC跟踪反应进程,直至反应完全。
3.间歇振荡15min后用冰水浴冷却。有更多白色固体析出。
4、把产物抽滤称重并记录实验数据,后把粗产物反复洗涤、过滤2-3次后再用乙醇重结晶可得纯品环己酮肟。
5、计算理论值和收率。对本次实验进行理论分析和数据分析,得出结论。
TLC指薄层色谱法,也就是我们平常所说的点板。
第二篇:实验10_环己酮的制备
酒泉职业技术学院《工科化学实验技术》学习领域教案
NO:10

环己酮的制备
一、教学要求:
学习铬酸氧化法制环己酮的原理和方法。进一步了解醇和酮之间的联系和区别。
二、预习内容:
1.实验原理2.抽虑操作3.盐析
三、实验原理:
实验室制备脂肪或脂环醛酮,最常用的方法是将伯醇和仲醇用铬酸氧化。铬酸是重要的铬酸盐和40-50%硫酸的混合物。仲醇用铬酸氧化是制备酮的最常用的方法。酮对氧化剂比较稳定,不易进一步氧化。铬酸氧化醇是一个放热反应,必须严格控制反应的温度,以免反应过于激烈。环己酮主要用于合成尼龙-6或尼龙-66,还广泛用作溶剂,它尤其因对许多高聚物(如树脂、橡胶、涂料)的溶解性能优异而得到广泛的应用。在皮革工业中还用作脱脂剂和洗涤剂。
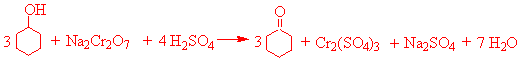
四、仪器与药品
仪器: 250ml圆底烧瓶、温度计、蒸馏装置、分液漏斗。
药品: 浓硫酸、环己醇、重铬酸钠、草酸、食盐、无水碳酸钠。
四、实验步骤:
1.铬酸溶液的配制
在250mL烧杯中加入30mL水和5.5g重铬酸钠,搅拌使之全部溶解。然后在搅拌下慢慢加入4.5mL浓硫酸,将所得橙红色溶液冷却至30℃以下备用。
2. 氧化反应  在250mL圆底烧瓶中加入5.5mL环己醇,然后取此铬酸溶液lml加入圆底烧瓶中,充分振摇,这时可观察到反应温度上升和反应液由橙红色变为墨绿色,表明氧化反应已经发生。继续向圆底烧瓶中滴加剩余的重铬酸钠(或重铬酸钾)溶液,同时不断振摇烧瓶,控制滴加速度,保持烧瓶内反应液温度在60~65℃之间。若超过此温度时立即在冰水浴中冷却。在圆底挠瓶中插入一支温度计,并继续振摇反应瓶。这时温度徐徐上升,当温度上升到55℃时,用水浴冷却,并维持反应温度在60~65℃。大约0.5h左右,当温度开始下降时移去冷水浴,室温下放置20分钟左右,其间仍要间歇振摇反应瓶几次,最后反应液呈墨绿色。如果反应液不能完全变成墨绿色,则应加入少量草酸(0.5~1.0g或甲醇1mL)以还原过量的氧化剂。
在250mL圆底烧瓶中加入5.5mL环己醇,然后取此铬酸溶液lml加入圆底烧瓶中,充分振摇,这时可观察到反应温度上升和反应液由橙红色变为墨绿色,表明氧化反应已经发生。继续向圆底烧瓶中滴加剩余的重铬酸钠(或重铬酸钾)溶液,同时不断振摇烧瓶,控制滴加速度,保持烧瓶内反应液温度在60~65℃之间。若超过此温度时立即在冰水浴中冷却。在圆底挠瓶中插入一支温度计,并继续振摇反应瓶。这时温度徐徐上升,当温度上升到55℃时,用水浴冷却,并维持反应温度在60~65℃。大约0.5h左右,当温度开始下降时移去冷水浴,室温下放置20分钟左右,其间仍要间歇振摇反应瓶几次,最后反应液呈墨绿色。如果反应液不能完全变成墨绿色,则应加入少量草酸(0.5~1.0g或甲醇1mL)以还原过量的氧化剂。
3. 在反应瓶中加入30mL水,如图1装置仪器(改用锥形瓶作接受器)进行蒸馏,收集约50mL馏出液。这一步蒸馏操作实际上是一种简化了的水蒸气蒸馏。环已酮与水形成沸点为95℃的恒沸混合物(含环已酮38.4%)。应注意馏出液的量不能太多,因为馏出液中含水较多,而环已酮在水中的溶解度较大 (31℃时为2.4g);否则,即使利用盐析效应,也有少量环已酮溶于水而损失掉。
4. 把馏出液用食盐水饱和,并将馏出液移至分液漏斗中,静止,分出有机相。水相用15mL乙醚提取一次,将乙醚提取液与有机相合并,用无水硫酸镁干燥。
5. 按图1装置仪器,在水浴上蒸出乙醚(在接液管的尾部接一通住水槽或室外的橡皮管,以便把易挥发、易燃的乙醚蒸气通入水槽的下水管内或引出室外),然后改用空气冷接管和接受器(如图2装置)继续蒸馏,收集150~155℃的馏分,产量3~4g。(产率66-72%)。
纯粹环己酮为无色透明液体,沸点155.7℃,相对密度d=0.9478,折光率1.4507。
乙醚的凝固点-116.2℃,沸点34.5℃,相对密度0.7138(20/4℃)。
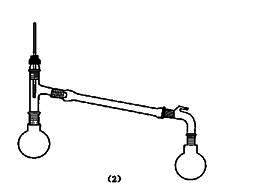
图2 空气冷凝蒸馏装置
五、存在的问题与注意事项:
1.本实验是一个放热反应,必须严格控制温度。
2.本实验使用大量乙醚作溶剂和萃取剂,故在操作时应特别小心,以免出现意外。
3.环己酮在31℃水解度为2.4g /100ml水中。加入粗盐的目的是为了降低溶解度,有利于分层。
4.反应容器外要用冰水浴冷却。
5.反应完全后反应液呈墨绿色,如果反应液不能完全变成墨绿色,则应加入少量草酸或甲醇以还原过量的氧化剂;
6. 加水蒸馏时,水的馏出量不宜过多,否则即使使用盐析,仍不可避免有少量环己酮溶于水中而损失。
六、深入讨论:
1.盐析的作用是什么?
答:盐析的作用:
氯化钠是离子子型晶体,溶于水中可增大水的介电常数,使极性小的有机物在水中的溶解度进一步降低,达到萃取分离的目的。
2.能否用铬酸氧化法把2-丁醇和2-甲基-2-丙醇区别开来?说明原因,并写出有关反应式。
答:能用铬酸氧化法把2-丁醇和2-甲基-2-丙醇区别开来。2-丁醇被氧化为2-丁酮,反应液变绿;2-甲基-2-丙醇不被氧化,反应液无颜色变化。
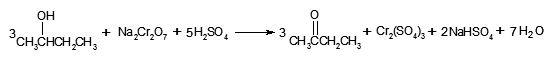
3.用铬酸氧化法环己酮的制备实验,为什么要严格控制反应温在55~60℃之间,温度过高或过低有什么不好?
答:本反应是一个放热反应,温度高反应过于激烈,不易控制,易冲出,温度过低反应不易进行,导致反应不完全。
4. 制备环己酮时,在加重铬酸钾(钠)溶液过程中,为什么要待反应物的橙红色完全消失后,方能加入下一批重铬酸钾(钠)?
答:重铬酸钾(钠)的氧化性比较强,如果一次加入很大量的话,会将环己醇氧化到环己酮,再继续氧化开环生成己二酸,所以加入重铬酸钾(钠)时要分批加入,防止过度氧化。而橙红色消失就是重铬酸钾(钠)反应完全的标志。
-
环己酮的制备实验报告
20xx年11月19日姓名系年级20xx级应用化学系组别30同组者科目有机化学题目环己酮的制备仪器编号一实验目的1学习铬酸氧化法制…
-
制备环己酮肟的实验
50设计合成实验的原理和步骤一以环已酮和盐酸羟胺为主要原料实验原理2NH2OHHCl盐酸羟胺Na2CO3NH2OH2NaClH2O…
-
有机化学实验报告:环己酮的制备
环己酮的制备华南师范cai前言环己酮无色透明液体分子量9814密度09478gmL熔点164C沸点15565C在水中微溶在乙醇中混…
-
环己酮的制备实验报告
实验学专班姓指导日机化学实验报告名称环己酮的制备院化学工程学院业化学工程与工艺级化工106班名严晓晓学号104020xx602教师…
-
环己酮的制备实验报告
实验学专班姓指导日机化学实验报告名称环己酮的制备院化学工程学院业化学工程与工艺级化工124班名王伟杰学号124020xx414教师…
-
环己酮的制有机化学实验报告
实验学专班姓指导日机化学实验报告名称环己酮的制备业化学工程与工艺级名学号教师房江华李颖期有一实验目的1学习次氯酸氧化法制环己酮的原…
-
有机化学实验报告:环己酮的制备
环己酮的制备华南师范cai前言环己酮无色透明液体分子量9814密度09478gmL熔点164C沸点15565C在水中微溶在乙醇中混…
-
聚己内酰胺的制备实验报告
聚己内酰胺的制备三主要试剂和产物的物理常数四实验装置图五实验步骤和现象六实验结果七注意事项八问题与讨论1因为环己酮肟的纯度对反应有…
-
环己酮的制备实验报告
20xx年11月19日姓名系年级20xx级应用化学系组别30同组者科目有机化学题目环己酮的制备仪器编号一实验目的1学习铬酸氧化法制…
-
环己酮的制备实验报告
实验学专班姓指导日机化学实验报告名称环己酮的制备院化学工程学院业化学工程与工艺级化工124班名王伟杰学号124020xx414教师…
-
环己酮的制备实验报告(4)沈杰
实验学专班姓指导日机化学实验报告名称院化学工程学院业化学工程与工艺级化工114班名沈杰学号114020xx417教师肖勋文何炎军期…