实验九 氧化还原与电化学
无机实验报告
实验九 氧化还原与电化学
一、电极电势与氧化还原反应方向

结论: (MnO4/ Mn2+)
(MnO4/ Mn2+)  (Fe3/Fe2+)
(Fe3/Fe2+)  (I2/I-)
(I2/I-)  (Sn4+/ Sn2+)
(Sn4+/ Sn2+)
查表:
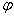 °(MnO4/Mn2+)= ,
°(MnO4/Mn2+)= , °(Fe3+/Fe2+)= ,
°(Fe3+/Fe2+)= , °(I2/I-) ,
°(I2/I-) ,
 °(Sn4+/Sn2+)= 。与上述实验所得 ,所以氧还方向为 。
°(Sn4+/Sn2+)= 。与上述实验所得 ,所以氧还方向为 。
二酸度对氧化还原反应的影响

结论:(1)C[H+]增大, (MnO2/Mn2+)及
(MnO2/Mn2+)及 (Cr2O72-/Cr3+)值 。
(Cr2O72-/Cr3+)值 。
(2)C[HCl]增大, (C12/C1-)值 ,所以,反应 。
(C12/C1-)值 ,所以,反应 。
三、影响氧化还原反应的其它因素
1、浓度的影响
FeC13+FeSO4+K1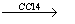 (CC14层 色)
(CC14层 色)
FeC13+K1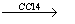 (CC14层 色)
(CC14层 色)
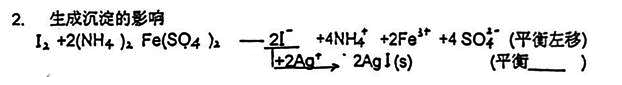
3、生成配合物的影响
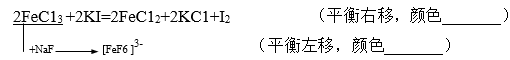
结论:
(1)反应1(稀释),3(生成配合物),使电对Fe3+/Fe2+中[Fe3+]降低,从而使反应难进行,即 (Fe3/Fe2+)下降了,Fe3+氧化性减弱。
(Fe3/Fe2+)下降了,Fe3+氧化性减弱。
(2)反应2(生成沉淀),使电对I2/I-中[I-]降低,  (I2/I-)值升高。
(I2/I-)值升高。
四、介值(碱)度对氧化还原反应的影响

五、酸度对氧-还反应速率的影响

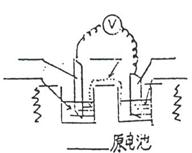
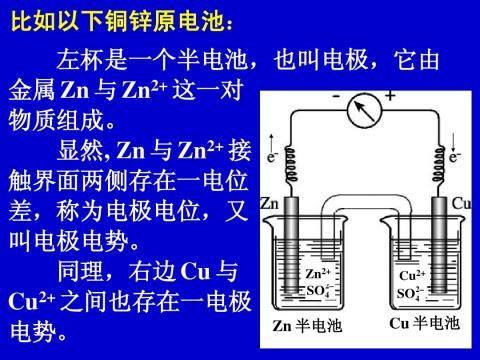
六、原电池
1、简易原电池的构成和电极电势的比较
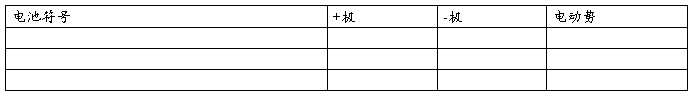
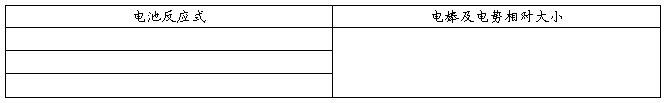
上述原电池中,各电极的反应式为:
原电池:负极反应 。
正极反应 。
原电池:负极反应 。
正极反应 。
原电池:负极反应 。
正极反应 。
2、浓度对电极电势的影响
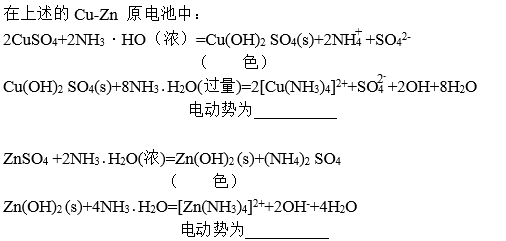
结论:电极电势随离子浓度改变而 ,在原电池中,正极离子浓度降低,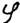 值 ,负极离子浓度降低,其
值 ,负极离子浓度降低,其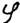 值 ,前者使电动势 ,后者使电动势 。
值 ,前者使电动势 ,后者使电动势 。
3、介质酸(碱)度对电极电势的影响
电池反应:

七、电解

专业 班,姓名 学号 评分
第二篇:实验十三 氧化还原反应与电化学







-
氧化还原反应实验报告
实验十二氧化还原反应一实验目的1理解电极电势与氧化还原反应的关系和介质浓度对氧化还原反应的影响2加深理解氧化态或还原态物质浓度变化…
-
实验九 氧化还原与电化学
无机实验报告实验九氧化还原与电化学一、电极电势与氧化还原反应方向结论:(MnO4/Mn2+)(Fe3/Fe2+)(I2/I-)(S…
-
实验17 氧化还原反应和电化学
实验17氧化还原反应和电化学一实验目的1了解电极电势与氧化还原反应的关系2试验并掌握浓度和酸度对电极电势的影响二实验原理原电池是将…
-
实验四氧化还原与电化学
实验四氧化还原与电化学一实验目的1了解原电池的电动势和电极电势的测定方法2掌握电极电势和氧化还原反应的关系3掌握反应物浓度介质对氧…
-
氧化还原与电化学实验
氧化还原与电化学实验Oxidationreductionreaction实验学时3实验类型验证性实验所属实验课程名称大学基础化学实…
-
氧化还原反应实验报告
实验十二氧化还原反应一实验目的1理解电极电势与氧化还原反应的关系和介质浓度对氧化还原反应的影响2加深理解氧化态或还原态物质浓度变化…
-
课题_氧化还原反应实验报告
一实验目的1理解电极电势与氧化还原反应的关系和介质浓度对氧化还原反应的影响2加深理解氧化态或还原态物质浓度变化对电极电势的影响3进…
-
实验九 氧化还原与电化学
氧化还原与电化学三(一)、电极电势与氧化还原反应方向结论:(MnO4/Mn2+)(Fe3/Fe2+)(I2/I-)(Sn4+/Sn…
-
实验17 氧化还原反应和电化学
实验17氧化还原反应和电化学一实验目的1了解电极电势与氧化还原反应的关系2试验并掌握浓度和酸度对电极电势的影响二实验原理原电池是将…
-
氧化还原反应和电化学的实验步骤
步骤1原电池的组成和电动势的粗略测定在一只井穴皿的123位置分别倒入约12容积的01MolL现象解释结论及方程式21CuCu22C…
-
电化学分析实验报告
电化学分析实验报告姓名:XXX专业:有机化学学号:时间:20XX.12.12一、实验目的1、了解电化学工作站的结构并熟悉其操作流程…