纳米二氧化硅的制备及其对有机物
纳米二氧化硅的制备及其对Cu2+、Ag+的吸附性能研究
一、实验目的:
(1)掌握纳米二氧化硅的制备方法;
(2)考察制备纳米SiO2的影响因素(温度、搅拌时间等);
(3)考察温度对纳米SiO2吸附蔗糖溶液的影响;
(4)考察温度对纳米SiO2吸附蔗糖溶液的影响;
(5)比较纳米SiO2对蔗糖、
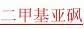
、DMF(二甲基甲酰胺)的吸附能力;
(6)掌握阿贝折射仪的使用方法;
二、实验原理:
纳米二氧化硅是一种无毒、无味、无污染的非金属材料,其平均粒径在1~100nm之间,呈絮状和网状的准颗粒结构,为球形状[1]。 由于纳米二氧化硅比表面大、表面能量高、化学反应活性大,可与聚合物基体发生界面反应,因此纳米二氧化硅作为工业填料能对聚合物起到增强、增韧的作用 [2]. 随着研究的深入,纳米二氧化硅在军事、通讯、电子、激光、生物学等领域都得到了广泛的应用。故本实验研究纳米二氧化硅对有机物的吸附性能和影响纳米二氧化硅吸附能里的因素。
负载能力定义为每100gSiO2负载银的克数。SiO2 对被吸附质有较强的吸附作用。本实验通过用一定量的SiO2吸附有机物,测量吸附前后有机物的浓度差,计算纳米二氧化硅的负载能力。
3、负载能力S定义为每1gSiO2可以吸附多少被吸附物质的能力。SiO2
对有机物有较强的吸附作用,用一定量的SiO2吸附一定量已浓度的有机物溶液,就可以用充分吸附后的滤液中的有机物量来确定SiO2的负载能力。
1、纳米二氧化硅的制备
本研究采用醇盐水解沉淀法制备二氧化硅纳米粉,并以SiO2为载体研究蔗糖浓度、吸附温度及吸附时间对负载能力的影响。
2、标准曲线法
折射率是物质物理材料属性之一,其受浓度、温度、压强、波长等因素影响。本研究利用浓度对物质折射率的影响,在一定条件下测出物资的折射率,从而确定物资的浓度。
标准曲线法是制定一系列标准浓度的有机物(如蔗糖),由低浓度到高浓度,利用阿贝折光仪分别测定不同标准浓度的折射率,以浓度为横坐标,折射率n为纵坐标,绘制n-c曲线,该曲线称为标准曲线。在相同条件下,测定试样的折射率,在标准曲线上求出试样的浓度。
三、实验仪器与试剂:
1、仪器:
阿贝折光仪,电子天平、容量瓶、烧杯、电子天平、滴管、玻璃棒、移液管。
2、试剂:
正硅酸乙酯、无水乙醇、浓氨水、蒸馏水、蔗糖(固体)、DMSO(二甲基亚砜)试剂、DMF(N-N-二甲基甲酰胺)试剂。
四、实验步骤
1、纳米二氧化硅的制备
将一定量的水和乙醇混合搅拌,滴入正硅酸乙酯和氨水,搅拌30min,静置一段时间即分层得二氧化硅沉淀。将二氧化硅沉淀洗涤,抽滤,100℃干燥得到白色轻质的SiO2粉末。(氨水1.2mol/L,乙醇2.5 mol/L,正硅酸乙酯100mL)。
2、蔗糖标准溶液的配制
称取一定量蔗糖固体溶解于蒸馏水中,在100ml容量瓶定容成浓度为500mg/l的蔗糖溶液,依次取一定量500mg/l的蔗糖稀释成浓度分别为400mg/l、300mg/l、200mg/l、100mg/l的蔗糖溶液。
3、研究浓度对纳米二氧化硅的负载能力s影响
量取分别量取20ml一系列标准蔗糖溶液于烧杯,在相同环境条件下,加入1g纳米二氧化硅,搅拌一定时间,静置混合液一段时间,取上层清液,用阿贝折光仪测定相应的折射率,在蔗糖标准曲线找出相应的浓度,整理数据,以蔗糖浓度c为横坐标,纳米二氧化硅的负载能力s为纵坐标,绘制s-c曲线。
4、研究温度对纳米二氧化硅的负载能力影响
取五份1.0 g纳米SiO2分别加入到五份50mL浓度为500mg/L蔗糖溶液,分别在20℃、30℃、40℃、50℃、60℃吸附1h,静置,去上层清液,用阿贝折光仪测定对应的折射率n,在蔗糖标准曲线求出相应的浓度c,整理数据,以吸附温度T为横坐标,纳米二氧化硅负载能
力s为纵坐标,绘制s-t曲线。
5、研究吸附时间对纳米二氧化硅的负载能力影响
取五份1.0 g纳米SiO2分别加入到五份50mL浓度为500mg/L蔗糖溶液,搅拌,静置一定时间,分别吸附1h,2h,3h,4h,5h,分别取上层清液,测定相应的折射率n,在蔗糖标准曲线求出相应的浓度c,整理数据,以吸附时间t为横坐标,纳米二氧化硅负载能力s为纵坐标,绘制s-t曲线。
6、研究纳米二氧化硅对哪种物质(DMSO、DMF)的吸附性能最好
(1)配制100mL浓度为5moL/L的DMSO溶液,稀释成五份100ml浓度分别为1moL/L、2moL/L、3moL/L、4moL/L的DMSO溶液,测定相应的折射率,绘制n-c曲线。
(2)配制100mL浓度为5moL/L的DMF溶液,稀释成五份100ml浓度分别为1moL/L、2moL/L、3moL/L、4moL/L的DMF溶液,测定相应的折射率,绘制n-c曲线。
(3)取五份1.0 g纳米SiO2分别加入到五份50mL浓度为5mol/L的DMSO溶液,搅拌,静置一定时间,在30℃下,分别吸附1h,2h,3h,4h,5h,分别取上层清液,测定相应的折射率n,在其标准曲线求出相应的浓度c,整理数据,以吸附时间t为横坐标,纳米二氧化硅负载能力s为纵坐标,绘制s-t曲线。
(4)取五份1.0 g纳米SiO2分别加入到五份50mL浓度为5mol/L的DMF溶液,搅拌,静置一定时间,在30℃下,分别吸附1h,2h,3h,4h,5h,分别取上层清液,测定相应的折射率n,在其标准曲线求出
相应的浓度c,整理数据,以吸附时间t为横坐标,纳米二氧化硅负载能力s为纵坐标,绘制s-t曲线。
(5)取五份1.0 g纳米SiO2分别加入到五份50mL浓度为5mol/L的DMSO溶液,分别在20℃、30℃、40℃、50℃、60℃吸附1h,静置,去上层清液,用阿贝折光仪测定对应的折射率n,在蔗糖标准曲线求出相应的浓度c,整理数据,以吸附温度T为横坐标,纳米二氧化硅负载能力s为纵坐标,绘制s-t曲线。
(6)取五份1.0 g纳米SiO2分别加入到五份50mL浓度为5mol/L的DMF溶液,分别在20℃、30℃、40℃、50℃、60℃吸附1h,静置,去上层清液,用阿贝折光仪测定对应的折射率n,在蔗糖标准曲线求出相应的浓度c,整理数据,以吸附温度T为横坐标,纳米二氧化硅负载能力s为纵坐标,绘制s-t曲线。
五、实验数据与处理:
1、计算各实验条件下的SiO2负载能力,绘制SiO2吸附能力与蔗糖原始浓度的关系曲线、SiO2吸附量与吸附温度的关系曲线及SiO2吸附量与吸附时间的关系曲线。
蔗糖的负载能力计算:
负载能力s(mg/g) =(吸附前浓度—吸附后浓度)*50ml/1.0g
2、分析蔗糖浓度、吸附温度及吸附时间对负载能力的影响,得出SiO2获得较大的载糖量的实验条件。
3、计算各实验条件下的SiO2负载能力,绘制SiO2吸附能力与DMSO原始浓度的关系曲线、SiO2吸附量与吸附温度的关系曲线及SiO2吸附量与吸附时间的关系曲线。
DMSO的负载能力计算:
负载能力s(mol/g) =(吸附前浓度—吸附后浓度)*50ml/1.0g
4、分析DMSO浓度、吸附温度及吸附时间对负载能力的影响,得出SiO2获得较大的载DMSO量的实验条件。
5、计算各实验条件下的SiO2负载能力,绘制SiO2吸附能力与DMF原始浓度的关系曲线、SiO2吸附量与吸附温度的关系曲线及SiO2吸附量与吸附时间的关系曲线。
DMF的负载能力计算:
负载能力s(mol/g) =(吸附前浓度—吸附后浓度)*50ml/1.0g
6、分析DMF浓度、吸附温度及吸附时间对负载能力的影响,得出SiO2获得较大的载DMF量的实验条件。
7、比较蔗糖溶液、DMSO溶液和DMF溶液的SiO2吸附能力与DMF原始浓度的关系曲线、SiO2吸附量与吸附温度的关系曲线及SiO2吸附量与吸附时间的关系曲线,分析纳米二氧化硅对哪种物质的吸附能力强,分别找出三者的最佳吸附时间、最佳吸附温度。
六、注意事项:
1、实验发现在溶液体积近似不变的情况下,氨水浓度在本实验范围内对二氧化硅粉体的粒度影响不大。平均粒径为 40nm
2 、分别用乙醇和水洗涤二氧化硅沉淀,直到流出液显中性。发现
用乙醇洗的粉体比用水洗的粉体团聚小、易分散。这是由于在用水洗涤后,残留在颗粒间的微量水会通过氢键而使颗粒团聚在一起。而用乙醇可以减少这种液桥作用,从而获得团聚少的粉体 。
七、参考文献:
[1] 霍玉秋,霍玉春.醇盐水解沉淀法制备二氧化硅纳米粉[J].微纳米电子技术,2003,15(9):12-15
[2] 张霞, 高大明. 二氧化硅纳米粒子制备的工艺参数研究. 安徽师范大学学报(自然科学版)第31卷3期2 0 0 8年5月
[3] 张国范,陈启元,冯其明等.温度对油酸在一水硬质铝石矿物表面吸附的影响[J].中国有色金属学报,2004,14(6):1042-1045
[4] 廖辉伟,车明霞.载银纳米SiO2制备与抗菌性研究[J].稀有金属,2006,30(4):570-573
第二篇:纳米二氧化硅的制备研究
2066
功能材料
20xx年增刊(38)卷
纳米二氧化硅的制备研究*
解小玲,张跃东,许并社
(太原理工大学材料科学与工程学院,山西太原030024)
摘
要:采用溶胶-凝胶法制备纳米SiO2。以正硅酸乙
匀,且在搅拌作用下,粒核增多,以致水解聚合的粒径减小,大约为23nm,pH值为9时颗粒增大,粒径为96nm,为了使其凝化时间缩短而粒径符合要求,最终选择水解时pH=3.0~3.5,凝胶时pH=8~9。
当溶胶的pH值较大时,颗粒表面电位减小,表面排斥能也减小,这样,将使得颗粒间的双电层排斥力小于静电引力和范德华力等的合力,使颗粒间易团聚,二次颗粒增大
[2,11]
酯为原料,氯化铵为催化剂,以乙醇水溶液为溶剂,制备SiO2超细粉体,还对影响生成的原料浓度、pH值、反应温度、反应时间及焙烧温度对产物的影响进行了研究,找到了最佳的反应条件。通过控制参数,可使沉淀的后续处理简化、时间缩短。该法制得的SiO2粉体颗粒均匀,平均粒径为63.5nm左右。关键词:纳米SiO2;制备;溶胶-凝胶法中图分类号:TQ127.2;TQ131.12
文献标识码:A
文章编号:1001-9731(2007)增刊-2066-03
。而当pH值过大时,由于溶液中配位
羟基数目较少,水解不充分,聚合反应发生后,沉淀物结构中含有较多的结构水,其多余的自由水将与胶体颗粒表面的自由羟基—OH以氢键相互作用。当颗粒接触时,颗粒间由这种水分子和相邻两个颗粒表面上的羟基氢键发生作用而产生桥接,更易产生团聚。
1引言
由于纳米SiO2的量子尺寸、量子隧道效应和它的特殊光、电特性、高磁阻现象、非线性电阻现象以及高温下仍具有的高强、高韧、稳定性好等特性,使纳米SiO2可广泛应用于许多领域[1~3]。
由于纳米SiO2的团聚现象,不能均匀地与基体材
,
料混合[45],使其应用受到很大限制,因此如何制备粒径分布均匀、分散均匀的纳米SiO2,并使其与基体材料更好的相容成为应用领域中的一个焦点问题。前人已对此进行了很多研究,但效果仍不理想,大部分研究中制备时间过长,粒径分布宽,且改性效果不佳
[9,10][6~8]
。
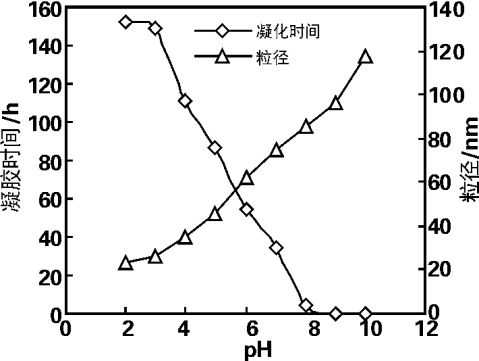
图1
3.2
pH对凝胶时间和粒径的影响
2实验
Fig1EffectofpHvalueongeiationtimeandparticlesize
水解度的影响
水解度用水和正硅酸乙酯的摩尔比n表示,水解度对凝胶时间和粒径的影响如图2所示。
首先将正硅酸乙酯、无水乙醇和蒸馏水按一定比例
混合,搅拌成均匀的混合溶液,加入少量氯化铵调节溶液pH值,调节体系温度为60℃,反应30min后,滴入氨水,调节pH值,生成凝胶,对不同凝胶产物用Zetasizer-Nano-Zs90型粒度分析仪进行粒径及粒径分布测试。所得纳米凝胶产物,研磨过筛,放入马弗炉中在不同温度下焙烧制得所需SiO2粉末样品。
3
3.1
实验结果
pH值的影响
图1为pH值对凝胶化时间和晶粒大小的影响。从图中可知,pH值对凝胶化的时间的影响很大,凝胶时间随pH值的增加而减小。在3.5左右时,反应很慢;当溶胶的pH>9时,在几秒中内可以完成凝胶化。同时pH值也严重影响了粒径,pH值为3时,粒度大小均
*基金项目:国家自然科学基金资助项目(50311140138)
n
图2n

对凝胶时间和粒径的影响
Fig2Effectofnongeiationtimeandparticlesize实验表明,不同的用水量对凝胶时间影响很大。由于在水解反应中,Si(OC2H5)4中的一个—OC2H5基因首
收到稿件日期:2007-04-27通讯作者:解小玲作者简介:解小玲(1969-),女,山西平遥人,硕士,讲师,主要从事高分子材料的研究。
解小玲等:纳米二氧化硅的制备研究先被—OH取代,剩余的—OC2H5基因反应活性低于开始时被取代的那个—OC2H5基因,因此,在水量不足的情况下,生成水解度最低的水解产物(C2H5O)3Si-OH,然后聚合成(C2H5O)3Si—O—Si(C2H5O)3,如果水量继续增加可导致上述部分进一步水解而得到链状聚合物。
n=7左右时凝胶化时间最短,随加水量增多,过量的水使得缩聚物的浓度降低,溶胶粘度下降,凝胶化时间延长。
在n值较小时,体系中乙醇分子含量较低,其阻碍顶氧形成硅-氧联结的作用不明显,硅酸根浓度迅速降低,而硅酸根浓度降低后,又易于交联形成凝胶,造成抽滤困难,干燥过程中出现团聚,使颗粒直径增大
[12]
;
在n值较大时,整个溶液中硅酸钠溶解度小,硅酸根彼此分离,易于形成凝胶,不利于生成沉淀,最终导致颗粒粒径增大。当n=6.5左右时,如图所示,粒径最小,约为63.5nm。3.3
温度的影响
如图3所示,水解温度越高,凝胶化时间越短。这
是因为升高反应温度,一方面使乙酸乙酯水解反应常数增大,反应速率加快,体系pH值降低加快;另一方面使聚合态硅酸根离子和胶体布朗运动加速,从而使质点间碰撞的频率增大。
图3温度对凝胶时间和粒径的影响
Fig3Effectoftemperatureongeiationtimeandparticlesize
对硅酸盐聚合形成溶胶的过程来说,pH值的影响是主要的,pH值降低速度加快导致聚合反应加速,表现为成胶时间缩短。但是,随着温度升高,溶胶越不稳定。水解温度在常温下时,凝胶时间较长,而温度在60℃附近时,凝胶化时间急剧的缩短,如图中所示,此温度下的凝胶较稳定,且最终粒径较小。3.4
溶胶凝胶形态
正硅酸乙酯作为特定的前驱体在一定条件下水解,形成溶胶,经溶剂挥发及加热等处理,使溶胶转变成网状结构纳米SiO2的凝胶[5]。凝胶焙烧得到SiO2粉末。焙烧温度影响SiO2粒径,焙烧温度越高,则粒径越大,但焙烧温度低于250℃时,得到的粉末不纯,因此选择焙烧温度为250℃,焙烧时间为1h,所得的SiO2凝胶经Zetasizer-Zano-ZS90型粒度分析仪检测,结果如图4所示,溶胶的平均粒径为63.5nm。
由于TEOS分子中的硅原子周围有4个烷氧基
2067
—OR(—OC2H5)与之键合,在碱性催化剂(NH4OH)参与下,OH-
对硅原子核发动亲核进攻,使硅原子核带负电,并导致电子云向另一侧的OR-
基团偏移,使该基团的Si—O键被削弱而断裂,发生水解。水解单体Si—OH基之间,以及Si—OH基与Si—OR基发生脱水或脱醇聚合反应,形成Si—O—Si链。Si—O—Si链之间不断交联,最终形成颗粒状聚集体。
图4纳米SiO2粒径分布
Fig4ParticlesizedistributionofSiO2powder
SiO2在成核过程中带负电,而NH4Cl可以作为阳离子表面活性剂它能在溶液中形成胶束,覆盖在微粒上,抑制粒子的快速长大,最终得到纳米SiO2凝胶。
4结论
(1)由于溶胶-凝胶过程中,溶胶由溶液制得,胶粒内和胶粒间化学成分完全一致。因此所制得的纳米SiO2粉体材料化学均匀性好。
(2)工艺条件:最终选择水解时pH=3.0~3.5,凝胶时pH=8~9。H2O/TEOS≈10,体系温度为60℃左右。
(3)颗粒细小,粒径为63.5nm,且均匀性好。(4)烘干后的球形颗粒自身烧结温度低,约250℃。(5)此工艺制备SiO2粉末时间短,只用大约2h。
参考文献:
[1]李凤生.超细粉体技术[M].北京:国防工业出版社,2000.[2]
徐国财,张立德.纳米复合材料[M].北京:化学工业出版社,2002.
[3]曹淑超,伍林,易德莲,等.[J].化学与生物工程,2005,
9:1-3.
[4]张宁,熊裕华.[J].南昌大学学报,2003,27(3):267-269.[5]Kyeong,YpulJung,SeungBinPark.[J].AppliedCatalysis
B,Environmental,2000,25(2):249-256.
[6]沈新璋,金名惠,孟厦兰,等.[J].涂料工业,2002,
9:15-18.
[7]HeleyJR,JacksonD,JamesPF.[J].Non-Solids,1995,
186:30-36.
[8]WardDA.[J].IndustrialEngineeringChemicalResearch,
1995,34(2):421-426.
[9]ChecmanowskiJG,GluszekJ,MasalskiJ.[J].Ochrona
PrzedKorozja,2002,11:214-218.
[10]李中军,刘长让,王雪清.[J].应用化学,1998,15(3):
79-81.
[11]秦晓东,蒋晓明,陈月珠.[J].石油大学学报,2001,25:
36-38.
[12]王子忱,王利玮.[J].无机材料学报,1997,12(3):
391-395.
2068功能材料20xx年增刊(38)卷
Studyonpreparationofnano-scalesilica
XIExiao-ling,ZHANGYue-dong,XuBing-she
(CollegeofMaterialsScienceandEngineeringofTaiyuanUniversityofTechnology,Taiyuan030024,China)
Abstract:Nano-silicawaspreparedbysol-gelmethod,usinglow-pricedtetraethylorthosilicateasrawmaterial,ammoniumchlorideascatalystandethanolassolvent.Influenceofpreparedparametersontheproducts,includingconcentrationofrawmaterial,pH,reactiontemperatureandtime,androasttemperature,wasstudied.Throughcontrollingappropriateparameter,followingtreatmentwassimplifiedandtimewasshortened.Theresultsshowedthatas-preparednano-silicawasuniformandtheaverageparticlesizewas63.5nm.
Keywords:nano-silica;preparation;sol-gelmethod
-
52硅及其重要化合物的相互转化
个性化教学辅导教案天津学大教育信息咨询有限公司个性化教学辅导教案学科化学任课教师庞向阳授课时间20xx年月日个性化教学辅导教案天津…
-
六、有关硅及其重要化合物化学方程式小结
六有关硅及其重要化合物化学方程式小结1Si1与氧气反应2与氯气反应3与氟气反应4与氢氟酸反应5与氢氧化钠溶液反应2SiO21与氧化…
- 鲁科版高一化学方程式总结-硅及其化合物
-
高一化学必修一第四章 非金属及其化合物(硅、氯)知识点总结
非金属及其化合物一一硅Si1硅单质存在结构化合态自然界在地壳中的含量第二仅次于氧物理性质灰黑色金属光泽硬度大有脆性熔沸点高的固体是…
-
硅及其化合物
教师寄语鲜花与荆棘同路泪水伴欢笑齐飞高三化学一轮复习导学案1迎着朝阳自我激励一天努力沐着晚霞自我反馈一天无悔2迎着朝阳自我激励一天…
-
三年级思品工作总结
三年级上册品德与社会教学工作总结本学期,我承担三年级《品德与社会》课的教学。一学期来,按照课程特点,在学期初制定了教学计划,并对学…
-
工作总结1
拥有着多年的工作经验,全身心的精力投入在工作中的电气工程师一职,年底的工作总结同时也是他们多年来的工作总结。以下是详细的电气工程师…
-
高一数学知识点归纳总结
高中高一数学必修1各章知识点总结第一章集合与函数概念一、集合有关概念1、集合的含义:某些指定的对象集在一起就成为一个集合,其中每一…
-
20xx年春小学三年级下学期品德与社会教学工作总结
一、学期目标本人承担了三年级品德与社会的教育教学工作。一学期来,按照课程特点制定实施了教育教学工作计划,对学生进行了一系列的教育。…
-
生产线线长个人工作总结
很快到公司已经半年多了,在这半年时间里,我受益匪浅,首先要感谢领导的鼓励与支持,同事的帮助与积极配合,使我对自己的工作不断的检讨和…