篇一 :原电池化学实验报告2
总实验目的:
研究原电池中各种因素对电池产生的电压、电流大小的影响
总实验用品:碳棒、铜棒、万用表(自备)、烧杯、导线(带夹子)
稀硫酸2mol/L、5mol/L、10 mol/L(递增即可,或者现配,则需配溶液用具),钠块、镁片(一卷,放心,用不完)、铜片、铝片、锌片、铁片
实验一
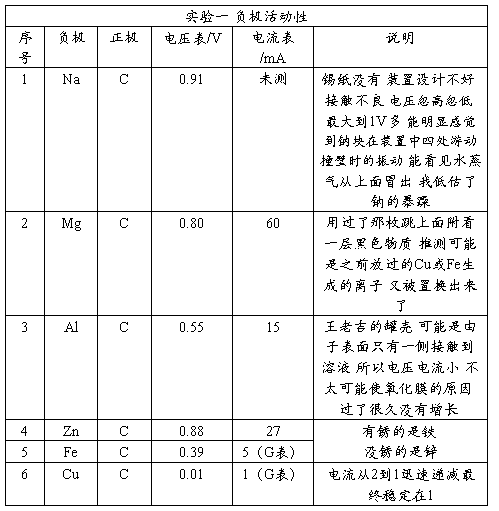
实验目的:探究负极金属活泼性对电压、电流的影响。
实验器材:碳棒、万用表(自备)、烧杯、导线(带夹子)
实验药品:稀硫酸2mol/L,钠块、镁片、铝片、锌片、铁片
实验二
实验目的:探究正极活泼性对电压、电流的影响
实验器材:碳棒、万用表(自备)、烧杯、导线(带夹子)
实验药品:稀硫酸2mol/L,碳棒、镁片、铜片、铜棒、铁片、锌片
实验三
实验目的:探究负极金属表面积大小对电压、电流的影响
实验器材:碳棒、万用表(自备)、烧杯、导线(带夹子)
实验药品:稀硫酸2mol/L,镁片(多个)
实验四(合在实验一中)
实验目的:研究钠作负极的原电池
实验用品:碳棒、导线(带夹子)、稀硫酸2mol/L、钠块、锡纸(被乌鸡白凤丸的药丸壳所替代)、万用表(自备)、烧杯
…… …… 余下全文
篇三 :原电池实验报告
贵阳十四中20##届高中毕业实验会考
(化学)
班级: 姓名:
一、实验考查内容:自制原电池
二、实验方案设计:(20分)
三、器材和用品准备:(10分)

四、实验操作:(60分)
五、桌面卫生(10分):
得分:( )
…… …… 余下全文
篇五 :原电池电动势的测定与应用物化实验报告
原电池电动势的测定及热力学函数的测定
一、实验目的
1) 掌握电位差计的测量原理和测量电池电动势的方法;
2) 掌握电动势法测定化学反应热力学函数变化值的有关原理和方法;
3) 加深对可逆电池,可逆电极、盐桥等概念的理解;
4) 了解可逆电池电动势测定的应用;
5) 根据可逆热力学体系的要求设计可逆电池,测定其在不同温度下的电动势值,计算电池反应的热力学函数△G、△S、△H。
二、实验原理
1.用对消法测定原电池电动势:
原电池电动势不能能用伏特计直接测量,因为电池与伏特计连接后有电流通过,就会在电极上发生生极化,结果使电极偏离平衡状态。另外,电池本身有内阻,所以伏特计测得的只是不可逆电池的端电压。而测量可逆电池的电动势,只能在无电流通过电池的情况下进行,因此,采用对消法。对消法是在待测电池上并联一个大小相等、方向相反的外加电源,这样待测电池中没有电流通过,外加电源的大小即等于待测电池的电动势。
2.电池电动势测定原理:
…… …… 余下全文
篇七 :化学选修4原电池实验报告
实验一:探究铁的腐蚀
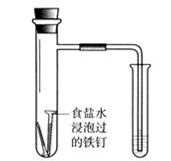 【实验目的】探究铁在中性环境中的腐蚀
【实验目的】探究铁在中性环境中的腐蚀
【实验原理】铁生锈时消耗了氧气,使具支试管中压强减小,因此导管中的水柱高度有变化
【实验仪器】具支试管,小试管,经过酸洗除锈的铁钉,塞子
【实验药品】饱和食盐水,蒸馏水
【实验步骤】将经过酸洗除锈的铁钉,用饱和食盐水浸泡一下,放入具支试管中。几分钟后,观察导管中水柱的变化。
【实验现象】(观察铁是否生锈,右边试管中导管内的水柱有什么变化)
实验二:金属的保护方法
【实验目的】用实验验证牺牲阳极的阴极保护法
【实验仪器】烧杯,铁片,锌片,导线,电压表
【实验药品】经过酸化的3﹪NaCl溶液
【实验步骤】将铁片和锌片放入盛有经过酸化的3﹪NaCl溶液的烧杯中,用导线连接并串联一个电压表。观察现象。
【实验现象】
实验三:原电池
【实验原理】Zn-2e- =Zn2+, Cu2+ +2e- =Cu
【实验仪器】烧杯2个,铜片,锌片,导线,电流表
【实验药品】CuSO4溶液
【实验步骤】将锌片和铜片用导线连接起来插入CuSO4溶液,并在中间串联一个电流表,观察现象;
【实验现象】锌片
…… …… 余下全文
篇八 :原电池电动势的测定实验报告
实验九 原电池电动势的测定及应用

一、实验目的
1.测定Cu-Zn电池的电动势和Cu、Zn电极的电极电势。
2.学会几种电极的制备和处理方法。
3.掌握数字电位差计的测量原理和正确的使用方法。
二、实验原理
电池由正、负两极组成。电池在放电过程中,正极起还原反应,负极起氧化反应,电池内部还可以发生其它反应,电池反应是电池中所有反应的总和。
电池除可用来提供电能外,还可用它来研究构成此电池的化学反应的热力学性质。从化学热力学知道,在恒温、恒压、可逆条件下,电池反应有以下关系:
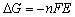 (9-1)
(9-1)
式中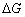 是电池反应的吉布斯自由能增量;n为电极反应中得失电子的数目;F为法拉第常数(其数值为96500
是电池反应的吉布斯自由能增量;n为电极反应中得失电子的数目;F为法拉第常数(其数值为96500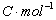 );E为电池的电动势。所以测出该电池的电动势E后,进而又可求出其它热力学函数。但必须注意,测定电池电动势时,首先要求电池反应本身是可逆的,可逆电池应满足如下条件:
);E为电池的电动势。所以测出该电池的电动势E后,进而又可求出其它热力学函数。但必须注意,测定电池电动势时,首先要求电池反应本身是可逆的,可逆电池应满足如下条件:
…… …… 余下全文

 实验报告
实验报告

