篇一 :人教版化学必修二第一章知识点总结
第一章 物质结构 元素周期表
第一节 元素周期表
一、周期表
原子序数 = 核电荷数 = 质子数 = 核外电子数
1、依据
横行:电子层数相同元素按原子序数递增从左到右排列
纵行:最外层电子数相同的元素按电子层数递增从上向下排列
2、结构
周期序数=核外电子层数 主族序数=最外层电子数
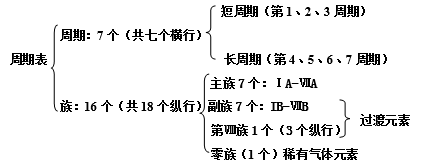
二.元素的性质和原子结构
(一)碱金属元素:
1、原子结构 相似性:最外层电子数相同,都为1个
递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径增大
2、物理性质的相似性和递变性:
(1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。
…… …… 余下全文
篇二 :高一化学必修2第一章知识点总结
第一章知识点复习及强化训练
一、元素周期表的结构
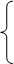 1、周期 第一周期____种元素 包括 元素
1、周期 第一周期____种元素 包括 元素
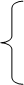 短周期 第二周期_____种元素 包括 元素
短周期 第二周期_____种元素 包括 元素
第三周期_____种元素 包括 元素
…… …… 余下全文
篇三 :人教版化学必修二第一章 知识点总结提高篇
夯实基础 提高能力 满分答卷 持之以恒
嘉祥一中高一化学 系列之知识清单
第一章 物质结构 元素周期表
提高篇:
一、周期表中特殊的周期和族
1、没有金属元素的周期是第一周期;含金属元素最多的族是ⅢB族;
2、非金属元素种类最多的.族是 0族。非金属元素种类最多的周期是第二周期。
3、全为金属元素的主族是第ⅡA族;
4、全为非金属元素的主族是第ⅦA族;
5、在常温时,全为气态的族是 0族。
6、形成化合物种类最多的族是ⅣA族;形成化合物种类最多的周期是第二周期。
7、最外层有3个电子的原子一定位于ⅢA族,最外层电子数为2个的原子可能位于
ⅡA,0族(He)、过渡元素区。
二、碱金属元素性质的特殊性
1、Na、K需保存于煤油中,但Li的密度比煤油小,所以Li必须保存在密度更小的石蜡油中或密封于石蜡
2、碱金属中,从Li?Cs,密度呈增大的趋势,但ρ(K)=0.862g/cm3<p(Na)=0.971e/cm3。
3、碱金属单质熔点都较低,只有Li高于100℃。
4、氧化产物的特殊性。碱金属在空气中燃烧,只有Li氧化成Li2O;其余的生成过氧化物(如Na2O2)或更复杂的氧化物(如K2O)。
…… …… 余下全文
篇四 :人教版化学必修二第一章知识点总结
第三节 化学键
知识点一.离子键
1.离子键:阴阳离子之间强烈的相互作用叫做离子键。 相互作用:静电作用(包含吸引和排斥)
注:(1)成键微粒: 阴阳离子间 (2)成键本质: 阴、阳离子间的静性作用
(3)成键原因:电子得失 (4)形成规律: 活泼金属和活泼非金属化合时形成离子键
离子化合物:像NaCl这种由离子构成的化合物叫做离子化合物。(1)活泼金属与活泼非金属形成的化合物。如NaCl、Na2O、K2S等
(2)强碱:如NaOH、KOH、Ba(OH)2、Ca(OH)2等 (3)大多数盐:如Na2CO3、BaSO4 (4)铵盐:如NH4Cl
小结:一般含金属元素的物质(化合物)+铵盐。(一般规律)
…… …… 余下全文
篇五 :高一化学必修2第一章知识点总结 2
第一章知识点复习及强化训练
一、元素周期表的结构
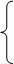 1、周期 第一周期____种元素 包括 元素
1、周期 第一周期____种元素 包括 元素
 短周期 第二周期_____种元素 包括 元素
短周期 第二周期_____种元素 包括 元素
第三周期_____种元素 包括 元素
…… …… 余下全文
篇六 :高中化学必修2知识点归纳总结第一章
第一章 物质结构 元素周期律
一、原子结构
 _______(Z个)
_______(Z个)
 原子核 注意:
原子核 注意:
_______(N个) 质量数(A)=_______ (Z)+_______ (N)
 1.原子(
A X ) 原子序数=_______=质子数=_______
1.原子(
A X ) 原子序数=_______=质子数=_______
核外电子(Z个)
★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
…… …… 余下全文
篇七 :人教版化学必修二第一章知识点总结
第一章 物质结构 元素周期表
第一节 元素周期表
一、周期表
原子序数 = 核电荷数 = 质子数 = 核外电子数
1、依据
横行:电子层数相同元素按原子序数递增从左到右排列
纵行:最外层电子数相同的元素按电子层数递增从上向下排列
2、结构
周期序数=核外电子层数 主族序数=最外层电子数

二.元素的性质和原子结构
(一)碱金属元素:
1、原子结构 相似性:最外层电子数相同,都为1个
递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径增大
2、物理性质的相似性和递变性:
(1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。
…… …… 余下全文
篇八 :人教版化学必修二第一章知识点总结
第一章 物质结构 元素周期表
第一节 元素周期表
一、周期表
原子序数 = 核电荷数 = 质子数 = 核外电子数
1、依据
横行:电子层数相同元素按原子序数递增从左到右排列
纵行:最外层电子数相同的元素按电子层数递增从上向下排列
2、结构
周期序数=核外电子层数 主族序数=最外层电子数

二.元素的性质和原子结构
(一)碱金属元素:
1、原子结构 相似性:最外层电子数相同,都为1个
递变性:从上到下,随着核电核数的增大,电子层数增多,原子半径增大
2、物理性质的相似性和递变性:
(1)相似性:银白色固体、硬度小、密度小(轻金属)、熔点低、易导热、导电、有展性。
…… …… 余下全文