ƪһ ����������Ĵ��ֽ�ʵ�鱨��
��������Ĵ��ֽ�
һ��ʵ��Ŀ�ģ�
1���þ�̬���ⶨH2O2�ֽⷴӦ���ٶȳ����Ͱ�˥�ڡ�
2����Ϥһ����Ӧ�ص㣬�˽ⷴӦ��Ũ�ȡ��¶ȡ����������ض�һ����Ӧ�ٶȵ�Ӱ�졣
3�������������������У����ѧ����ͼ����㷨���һ����Ӧ���ٶȳ�����
����ʵ��ԭ����
1. ����Ӧ�ٶ�ֻ�뷴Ӧ��Ũ�ȵ�һ�η������ȵķ�Ӧ����Ϊһ����Ӧ��ʵ��֤��H2O2�ķֽⷴӦ���£�

2 H 2O 2 �� 2 H 2O + O 2 ��1��

2. ���÷�Ӧ����һ����Ӧ�������ٶȷ���Ӧ�ǣ�
ʽ�У�CH2O2��ʱ��tʱ��H2O2Ũ�ȣ� k����Ӧ�ٶȳ�����
���� ���� ����ȫ��
ƪ�� ��ʵ��14 ����������ֽⷴӦ���ʳ����IJⶨ
�� �ο� 4 ѧʱ







ʵ��14 ����������ֽⷴӦ���ʳ����IJⶨ
һ��ʵ��Ŀ��
1. �ⶨ����������ֽⷴӦ���ʳ�����
2. ����ͨ��������Ӧϵͳ��������ٷ�ӦϵͳŨ�ȴӶ��о���Ӧ���ʵķ�����
����ʵ��ԭ��
����������û�д�������ʱ���ֽⷴӦ���еĺ�������������ܹ���߷ֽ����ʡ���������ֽⷴӦ�Ļ�ѧ����ʽ���£�
H2O2(l) = H2O(l) + 1/2O2(g)
����KIΪ��������KI�����´��ֽⲽ��Ϊ��
KI(l) + H2O2(l) = KIO + H2O(l) ������
���� ���� ����ȫ��
ƪ�� ����������������о� ʵ�鱨��
��������������о�
ժ Ҫ������������Ŀǰʵ������ȡ������ȫ�����۵��Լ������ڹ��������������ʣ��и��ָ����Ĵ����ɹ�ѡ���ľ������������ѡ�����̽����
�ؼ��ʣ��������� ���� ����
�����ڻ�ѧʵ����ʮ����Ҫ�����пα����Ʊ�������;��֮һ�ǹ���������ֽ⡣���Ź��յĸĽ�����������ijɱ����Ͻ��ͣ���һ�ֺ���ǰ;���Ʊ�������;��������������й�������-O-O-��O�����������̬���ʲ��ȶ������Ͽ��������²���Ϊ320��380nm�Ĺ����䣬���Ǽ��ȣ�ʹ�ô��������Լ��ٹ�������ķֽ⡣�����ٶ�̫���������˷���Դ�����ֽ����ʲ��ȶ�������Ѱ��һ�ֺ��ʵĴ����������Ҫ����������Ĵ�ԭ����Ҫ�����¼��֣�
1. �����ؽ��������������Σ����ɵ��������̷ֽ�ų�������
����H2O2+MnO2=H2MnO4
H2MnO4+H2O2=MnO2+O2��+2H2O
2. ���������ڼ������������ֽ�Ϊ������ˮ��������ʹ��Һ�Լ��ԣ����ڹ�������ķֽ⡣
���� ���� ����ȫ��
ƪ�� ����������Ĵ��ֽ�ʵ��
��������Ĵ��ֽ�
һ ʵ��Ŀ��
1. ��Ϥһ����Ӧ�ص㣬�˽ⷴӦŨ�ȡ��¶Ⱥʹ��������ض�һ����Ӧ�ٶȵ�Ӱ��;
2. �þ�̬����H2O2�ֽⷴӦ�ķ�Ӧ�ٶȳ����Ͱ�˥��.����Ӧ���;
3. ѧ����ͼ�ⷨ���һ����Ӧ�ķ�Ӧ�ٶȳ���.
�� ʵ��ԭ��
���Ƿ�Ӧ�ٶ�ֻ�뷴ӦŨ�ȵ�һ�η������ȵķ�Ӧ��Ϊһ����Ӧ��ʵ��֤������������ķ�Ӧ����Ϊһ����Ӧ.��ѧ��Ӧ�ٶ�ȡ���ڷ�Ӧ���Ũ�ȡ��¶ȡ���Ӧѹ���������������ٶȵ��������ء����������Pt��Ag��MnO2��FeCl3�⻯��ȶ��ܼ���H2O2�ֽ⡣�ڴ���KI�����µķֽⷴӦ����Ӧ�������£�
H2O2+I����IO��+H2O
H2O2+ IO����H2O+O2+I��
�������̣����Ƶ����ܷ�Ӧ���ٶȹ�ʽ��
-=K�@[H2O2][ I��]
���� ���� ����ȫ��
ƪ�� ����������Ĵ��ֽ�
��������ֽ�����
��Ա������ࡢ��誡����������ޡ����ڡ�����
һ�� ʵ��Ŀ��
1�� ����ʵ������˫��ˮ�Ʊ�������ԭ����װ�úͲ�����
2�� �˽�Ӱ��˫��ˮ�Ʊ�������Ӧ���ʵ����ء�
3�� ����ʶ�����ڻ�ѧ��Ӧ�е����ü���ѧ��Ӧǰ�������ı仯��
���� ʵ��ԭ��
�������ⲻ�ȶ����ڳ����¾��ܻ����ֽ�ų����������ٶȽ��������ײ�����ڹ���������Һ�м��������������̺�������������Ѹ�ٷų����ڴ˷�Ӧ�У����������Ǵ������ܼ��ٸ÷�Ӧ�ķ�����

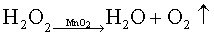
���� ʵ��ҩƷ������
ʵ��ҩƷ��5%��30%��˫��ˮ���������̡�����ͭ��
�� ����ע������20ml������ƿ�����ܡ���ľ��������ˮԡ��������ƿ����Ƥ�ܡ�Կ�ס�
�ġ� ʵ�鲽��
1��ʵ�����Ʊ�����
���������������װ�õ������ԣ�
������ƿ�м��������������̷�ĩ��������ľ������ע������˫��ˮƿ����ȡ10ml 5%˫��ˮ����עˮ�����˫��ˮ����Ҫ��������ע�����װ�������������̷�ĩ����ƿ�У�
���� ���� ����ȫ��
ƪ�� ��ʵ��ʮ�� ����������ֽ�
2.3 ����ѧ����
ʵ��ʮ�� ����������ֽ⪤
1 Ŀ��Ҫ��
(1) �ⶨ��������ֽ�ķ�Ӧ�ٶȳ����� ��
(2) �˽���������о�����ѧ�Ļ���ԭ������
(3) �˽�ʵ��ⶨ���E��ԭ���ͷ�������
2 ����ԭ����
����������û�д���ʱ���ֽⷴӦ���еú������������ʱ�ܴٽ���ֽ⡣��������ֽ�Ļ�ѧ����ʽ���£�
H2O2��H2O+1/2O2��
�ܶ����ʶ��ܶ���һ��Ӧ������ã��粬������Ǧ���������̡����Ȼ����Լ����Ȼ������Ȼ�ͭ�Ļ����ȡ���ʵ���������Ȼ������Ȼ�ͭ��������������о�H2O2�ֽⷴӦ�Ķ���ѧ������CuCl2��������������ʹ�����������ܴ��÷�Ӧ��
�ڱ�ʵ�������£���������ķֽ���һ����Ӧ���� �� a ��ʾH2O2����ʼŨ�ȣ�x��ʾ��ʱ�� t ʱ�Ѿ��ֽ����H2O2��Ũ�ȣ�����ʣ���H2O2��Ũ��Ϊ(a-x)�������У�
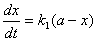
������ʽ���� ln(a-x)= -k1t + lna
���� ���� ����ȫ��
ƪ�� ������������ֽⷴӦ���ʳ����IJⶨ
����������ֽⷴӦ���ʳ����IJⶨ

һ��ʵ��Ŀ��
��1���˽����������ֽⷴӦ���ʳ����IJⶨ������
��2����Ϥһ����Ӧ���ص㣬�˽�����Է�ӳ���ʵ�Ӱ�졣
��3��������ͼ����㷨��Ӧ���ʳ�����
����ʵ����Ʒ
1������
������Ӧ����1����ˮƿ1����50mL������1�����������²�1�ס���ͨ����1�������1�顢10mL��Ͳ1����5mL������2֧������3m��
2��ҩƷ
��������Ϊ2%��H2O2��Һ���������ƣ���0.1mol·L-1KI��Һ��
����ʵ��ԭ���뼼��
��������ܲ��ȶ����ڳ����µķֽⷴӦʽΪ��
H2O2��H2O+1/2O2 ����
��KI�����µķֽⷴӦ����Ϊ��
H2O2+KI��KIO+ H2O ������ ����
KIO��KI+1/2O2 ���죩 ����
����ʽ��H2O2�ֽ���ٿز��裬H2O2�ֽⷴӦ�ķ�Ӧ���ʷ���Ϊ��
��dcH2O2/dt=k´cH2O2·cKI ������
���� ���� ����ȫ��
ƪ�� ��ʵ���� ����������ֽ�
ʵ���� ����������ֽ�
Catalyzed Decomposition of Hydrogen Peroxide
ʵ�����ͣ�������
ʵ��ѧʱ��5
��ѧ�����ٴ�ҩѧרҵ
һ��ʵ��Ŀ��
1. ��Ϥһ����Ӧ���ص㣬�˽�Ũ�ȡ��¶ȡ����������ضԷ�Ӧ���ʵ�Ӱ�졣
2. ���������ⶨ��������ֽⷴӦ�����ʳ����ͻ�ܡ�
����ʵ��ԭ��
��������Ĵ��ֽ���һ����Ӧ��
H2O2 �� H2O + 1 / 2 O2
ln  =�Ckt ��3-1��
=�Ckt ��3-1��
�ڷֽ�����У��ų��������������ֽ��˵�H2O2Ũ�ȳ����ȣ�
C0�� V��
Ct �أ�V���CVt��
����ʽ��3-1����������ɵã�
ln��V���CVt��=�Ckt + ln V��
��ln��V���CVt����t��ͼ����ֱ�ߵ�б�ʿ�������ʳ���k����������ͬ�¶ȵ�kֵ����������Ea��
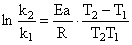
��. ʵ����
1. �� �������²ۣ�������װ�ã���ƿ����Һ�ܣ������
2. ҩ Ʒ��3%H2O2��Һ��KI��Һ��0.1mol·mol�C3����
�ģ�������װҪ��
������¼�� ��װ������װ��
���� ���� ����ȫ��