篇一 :现代实验分析报告
.水泥中MgO、CaO、Al2O3、Fe2O3含量的测定
一、实验目的
1、学习复杂物质分析的方法。
2、掌握尿素均匀沉淀法。
二、实验原理
本实验采用硅酸盐水泥,一般较易为酸所分解。
试样经 HCl 溶液分解、HNO3 氧化后,用均匀沉淀法使 Fe(OH)3,Al(OH)3 与 Ca2+,Mg2+分离。以磺基水杨酸为指示剂,用 EDTA 络合滴定 Fe3+;以 PAN 为指示剂,用 ZnSO4 标准溶液返滴定法测定Al。Fe、Al 含量高时, 对 Ca2+,Mg2+测定有干扰。可以用尿素分离 Fe,Al 后,再用钙指示剂或铬黑T通过络合滴定来测定 Ca2+,Mg2+含量。
三、主要实验试剂和仪器
试剂:EDTA溶液 铜标准溶液(0.02mol/L) 盐酸 浓硝酸 NH4Cl氨水 尿素
指示剂:磺基水杨酸(100g/L) 溴甲酚绿 PAN 铬黑T GBHA
缓冲溶液:氨水—NH4Cl缓冲溶液(PH=10)
六次甲基四胺缓冲溶液(PH=4~5)
仪器:容量瓶 烧杯 锥形瓶 酸性滴定管
四、实验步骤
1、EDTA溶液的标定
移取 10.00ml Cu2+ 标准溶液于250mL锥形瓶中,加入5mLPH为3.5的缓冲溶液和35mL蒸馏水,加热至80℃,加入4滴PAN指示剂,趁热用待标定的EDTA溶液滴定至溶液由红色变为绿色,即为终点,记下消耗EDTA溶液的体积。平行滴定3次,计算 EDTA 的准确浓度。
…… …… 余下全文
篇二 :实验结果分析报告
1、亚硝酸钠测定结果:
①标准液质量与吸光度表
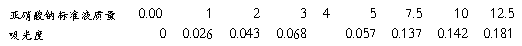
②工作曲线(标准液浓度与吸光度回归直线示意图,散点图用excel制作)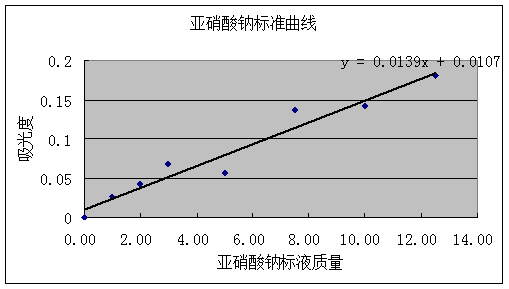
回归方程:【A】=0.0139m+0.0107
【A】表示吸光度; m表示质量
③结果计算
实验测得双汇1、2样品吸光度分别为:0.017、0.018
金锣1、2样品吸光度分别为:0.017、0.017
代入回归方程:【A】=0.0139m+0.0107,计算结果如下表:

2、亚硝酸盐含量计算
亚硝酸盐(以亚硝酸钠计)的含量按式(3)进行计算。

………一(3)
式中:
X1——试样中亚硝酸钠的含量,单位为毫克每千克(mg/kg);
A1——测定用样液中亚硝酸钠的质量,单位为微克(μg)
…… …… 余下全文
篇三 :实验报告 范本

研究生实验报告(范本)
实验课程: 新型传感器技术
实验名称: 聚苯胺复合薄膜气体传感器的制备与测试
实验地点: 光电420
学生姓名: (范本)
学 号: (范本)
指导教师: (范本)
实验时间: 年 月 日
一、实验目的
熟悉电阻型气体传感器结构及工作原理,进行基于聚苯胺敏感薄膜的气体传感器的结构设计、材料制作、材料表征、探测单元制作与测试、实验结果分析,通过该实验获得气体传感器从设计到性能测试完整的实验流程,锻炼同学学习能力、动手能力和分析问题能力。
二、实验内容
1、理解电阻式气体传感器工作原理
2、进行传感器结构设计
3、进行敏感材料的合成与测试
4、开展气体传感器制作
5、器件性能测试与分析讨论
三、实验原理
气体传感器是化学传感器的一大门类,是气体检测系统的核心,通常安装在探测头内。从本质上讲,气体传感器是一种将某种气体体积分数转化成对应电信号的转换器。根据气敏特性来分类,主要分为半导体气体传感器、固体电解质气体传感器、接触燃烧式气体传感器、光学式气体传感器、石英谐振式气体传感器、表面声波气体传感器等。
…… …… 余下全文
篇四 :程序分析实验报告
程序分析第二次实验报告
13091372 代树理
开发环境:
语言:java
编译器:myeclipse
操作系统:windows XP
另外使用的ANTLR语言包
实验要求:
用ANTLR构造所需的词法分析器、语法分析器、抽象语法树的遍历器。并在树的遍历器文法中,进行相关的语义处理(包括表达式求值、保存绘图参数等)。
…… …… 余下全文
篇五 :实验报告(相关分析)
《经济分析方法与手段》实验分析报告
附件一、
1 陶瓷产量与城镇住宅建筑面积的相关分析
散点图



2 与新增医疗卫生机构面积的关系
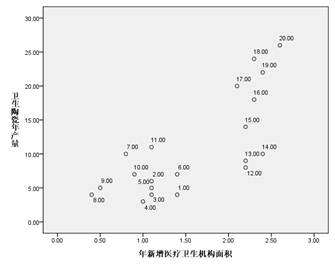
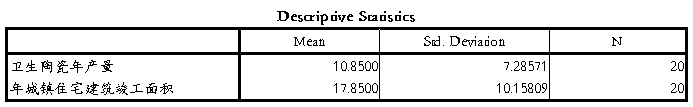
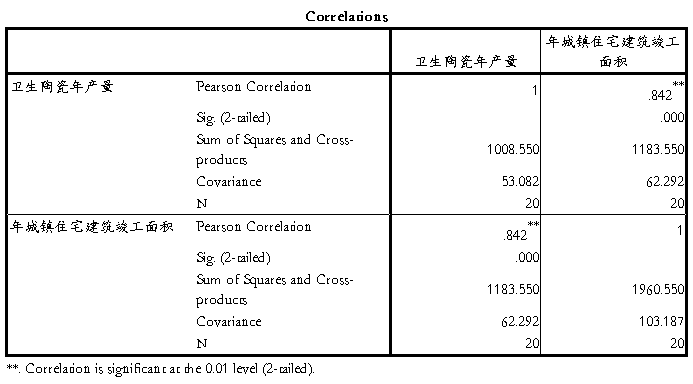
3 与新增办公楼面积的关系
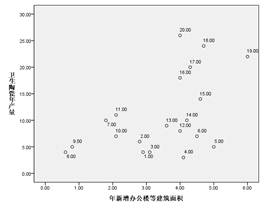
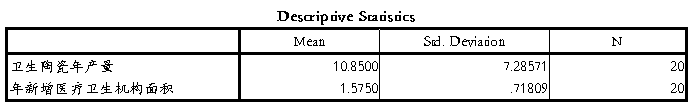
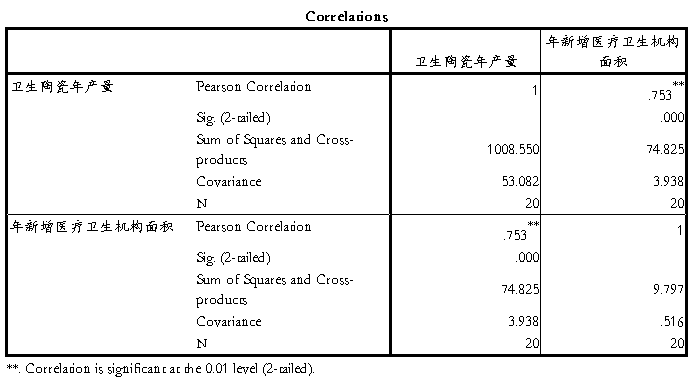
附件二、
说明:如果实验分析需要用到SPSS的图表,依次在附件中列出,并在“实验结果及分析”中相应说明。
…… …… 余下全文
篇六 :数据整理与分析实验报告
浙江万里学院实验报告

课程名称:2014/2015学年第一学期统计实验
实验名称: 数据整理与数据分析

专业班级: 姓名: 学号 实验日期:
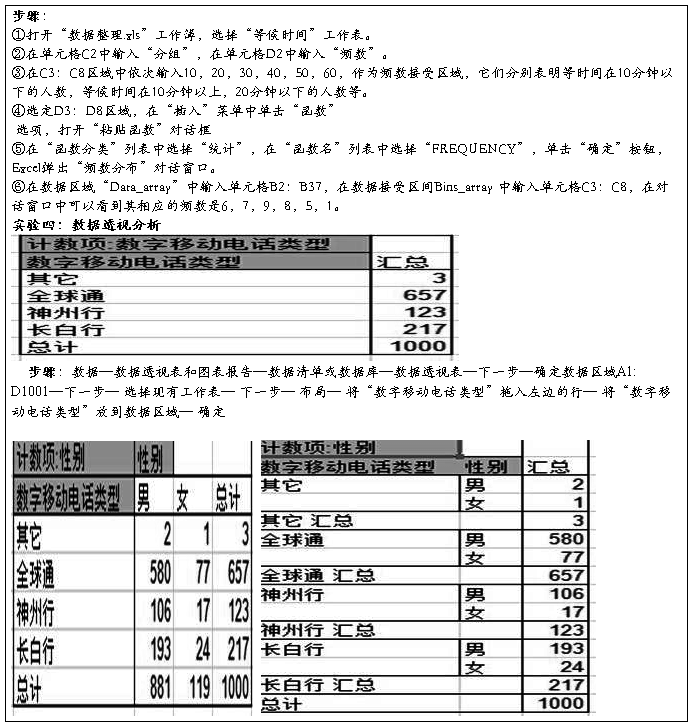
专业班级: 姓 名: 学号: 实验日期:
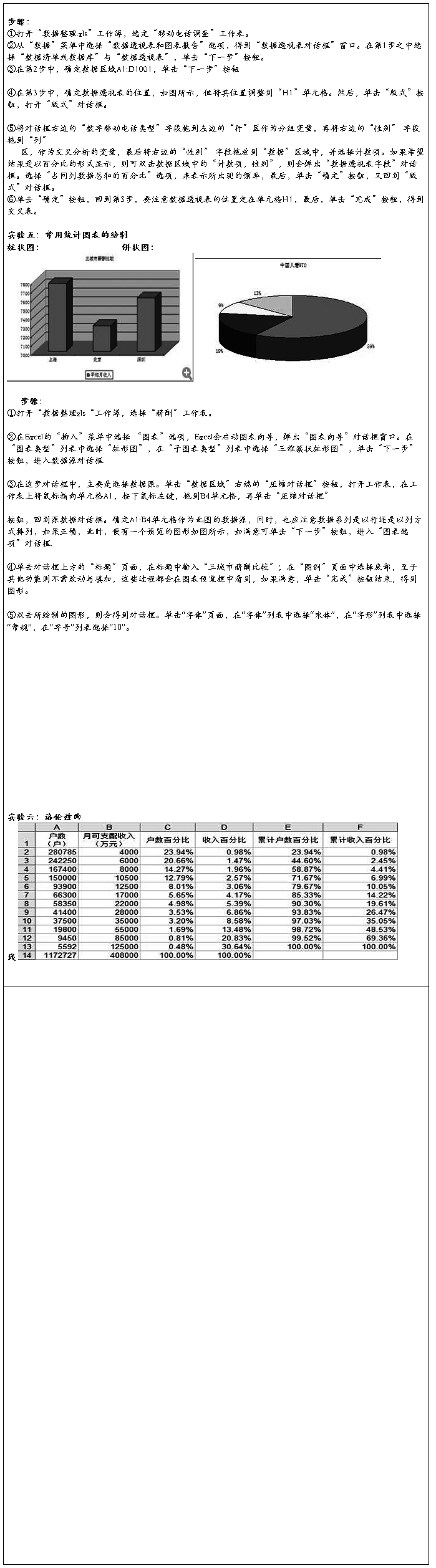
专业班级: 姓 名: 学号: 实验日期:
…… …… 余下全文
篇七 :分析化学实验报告
分析化学实验报告
20##-02-18 20:08:58| 分类: 理工类 | 标签: |字号大中小 订阅
盐酸和氢氧化钠标准溶液的配制和标定
时间:12月15号 指导老师:某某
—、实验目的
1. 熟练减量法称取固体物质的操作,训练滴定操作并学会正确判断滴定终点。
2. 掌握酸碱标准溶液的配制和标定方法。
3.通过实验进一步了解酸碱滴定的基本原理。
二.实验原理
有关反应式如下:
Na2CO3 + 2HCL == 2NaCL + CO2 + H2O
KHC8H4O4 + NaOH ==KNaC8H4O4 + H2O
三.实验步骤
1、 0.1.mol/L HCL溶液的配制
用小量筒量取浓盐酸42mL,倒入预先盛有适量水的试剂瓶中(于通风柜中进行),加水稀释至500mL,摇匀,贴上标签。
2、 0.1mol/L NaOH溶液的配制
用烧杯在台秤上称取2g固体NaOH,加入新鲜的或新煮沸除去CO2的冷蒸馏水,溶解完全后,转入带橡皮塞的试剂瓶中,加水稀释至500ml,充分摇匀,贴上标签。
3、 0.1 mol/L HCL标准溶液浓度的标定
用差减法准确称取 0.15 ~ 0.20 g无水Na2CO3 三份,分别置于三个250mL锥形瓶中,加20~30 ml蒸馏水使之溶解,再加入1~2滴甲基橙指示剂,用待标定的HCL溶液滴定至溶液由黄色恰变为橙色即为终点。平行标定三份,计算HCL溶液的浓度。
…… …… 余下全文