初中化学方程式(上册总结)
一.初中化学方程式(上册)注:按照教材上出现的顺序编写
1.碳酸氢铵受热分解: 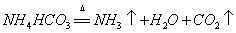
2.二氧化硫使高锰酸钾溶液褪色: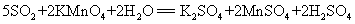
3.石蜡在氧气中燃烧: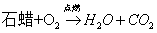
现象:(1)火焰明亮发出白光(2)放出热量(3)烧杯壁出现水雾(4)生成一种能使澄清石灰水变浑浊的气体
4.碳在氧气中燃烧: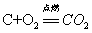
现象:(1)发出白光(2)放出热量(3)生成一种能使澄清石灰水变浑浊的气体
5.氯化氢气体和氨气混合(浓盐酸和浓氨水反应): 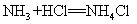
6.碘化钾与硝酸银反应: 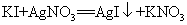
7.铜绿(碱式碳酸铜)与盐酸反应: 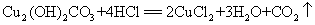
现象:(1)绿色粉末逐渐溶解(2)有气泡产生(3)溶解后液体呈蓝绿色
8.铜绿(碱式碳酸铜)受热分解: 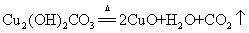
现象:(1)绿色粉末变成黑色(2)试管内壁有水珠生成(3)澄清石灰水变浑浊
9.镁带在空气氧气中燃烧: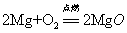
现象:(1)发出耀眼的白光(2)放出热量(3)生成白色粉末
10.铜丝加热: 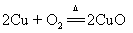
11.红磷白磷在氧气中燃烧(研究空气组成的实验):
现象:(1)发出白光(2)放出热量(3)生成大量白烟
12.硫在空气氧气中燃烧:
现象:A、在纯的氧气中燃烧 (1)发出明亮的蓝紫火焰(2)放出热量(3)生成一种有刺激性气味的气体
B、在空气中燃烧 (1)发出淡蓝色火焰(2)放出热量(3)生成一种有刺激性气味的气体
13.铁丝在氧气中燃烧: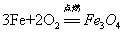
现象:(1)剧烈燃烧,火星四射(2)放出热量(3)生成一种黑色固体
14.加热高锰酸钾(实验室制氧气原理1):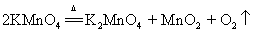
15.过氧化氢在二氧化锰作催化剂条件下分解(实验室制氧气原理2):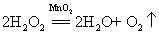
16.植物的光合作用文字表达式: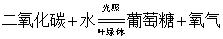
17.二氧化碳与水反应: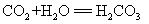
18.碳酸不稳定分解: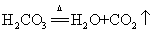
19.大理石和稀盐酸(实验室制二氧化碳原理):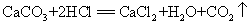
20. 二氧化碳使澄清石灰水变浑浊(鉴别二氧化碳气体):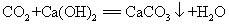
21. 生石灰和水反应: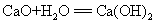
22. 电解水实验(研究水的组成实验):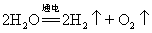
23.氢气和氧气点燃: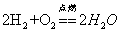
现象:(1)产生淡蓝色火焰(2)放出热量(3)烧杯内壁出现水雾
24.甲烷在空气中燃烧: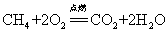
25.乙炔在空气中燃烧: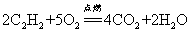
26.碳与氧气反应: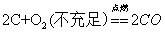
27.一氧化碳点燃:
现象:(1)发出蓝色的火焰(2)放热(3)澄清石灰水变浑浊
28.硫酸铜与氢氧化钠反应: 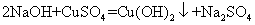
29.玻义耳研究空气的成分实验:氧化汞分解 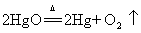 汞加热
汞加热 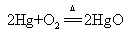
30.铝在空气中形成氧化膜: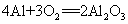
31.锌与盐酸反应: 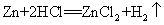
32.氯酸钾用二氧化锰做催化剂分解制氧气(实验室制氧气原理):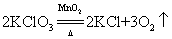
33.氯化铁与氢氧化钠反应: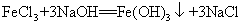
34.电解氯化镁: 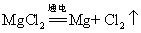
35.锌与稀硫酸反应: 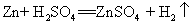
36.石灰石浆吸收废气中的二氧化硫: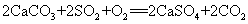
37.乙醇(酒精)在空气中燃烧: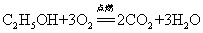
38.氢气还原氧化铜: 
39.镁在二氧化碳中燃烧: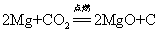
40.高温煅烧石灰石(工业制取二氧化碳原理):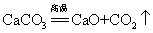
41.碳酸钠和稀盐酸反应(灭火器原理):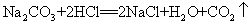
42.铁和盐酸反应: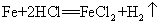
43.铁和稀硫酸反应: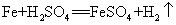
44.铝和盐酸反应: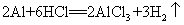
45.铝和稀硫酸: 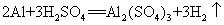
46.锌和盐酸的反应: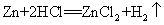
47.锌和稀硫酸反应(实验室制氢气原理)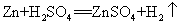
48.铁和硫酸铜溶液反应(湿法炼铜原理):
现象:(1)铁表面覆盖一层红色的物质(2)溶液由蓝色变成浅绿色
49.一氧化碳还原氧化铁: (高炉炼铁原理):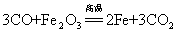
现象:(1)红色粉未变成黑色(2)澄清石灰水变浑浊
50.电解铝: 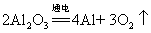
51.碳还原二氧化碳: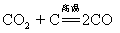
52.锌和硫酸铜溶液反应: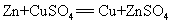
53.氧化铜与稀硫酸反应: 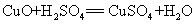
54.焦炭还原氧化铁: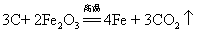
55.用盐酸除去铁锈: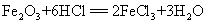
二.常见元素的化合价口诀:
一价氢氯钾钠银, 二价氧钙镁钡锌, 三铝四硅五价磷; 二三铁, 二四碳,
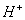


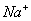
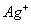

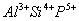
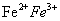
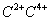
二四六硫, 三五氮; 铜汞二价最常见(一五七氯常常见) 单质零价永不变。
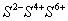
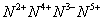
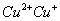
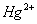
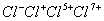
负一硝酸氢氧根 负二硫酸碳酸根 负三记住磷酸根 正一价的是铵根
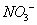
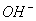
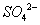
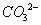
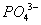

三.常见物质的颜色、气味等:
红色:红P、Cu、Fe2O3
红褐色:Fe(OH)3
浅绿色:Fe2+盐的溶液
黄色:S、Fe3+盐的溶液
绿色:Cu2(OH)2CO3
紫黑色:KMnO4晶体
蓝色:Cu(OH)2、CuCO3、CuSO4·5H2O、Cu2+盐的溶液
紫红色:KMnO4溶液
黑色:C、Fe粉、CuO、MnO2、Fe3O4
白色:BaSO4、AgCl、MgO、P2O5、CaO、NaOH、Ca(OH)2、CaCO3、
KClO3、KCl、NaCl、BaCO3、CuSO4、Na2CO3
无色气体:空气、O2、H2、CO2、CO、CH4、N2、SO2
刺激性气味气体:SO2、HCl、HNO3等
无色透明:金刚石、干冰以及大部分酸、碱、盐的溶液和酒精、乙酸的溶液
四.金属活动性顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
───────────────────────→
金属活动性由强逐渐减弱
小结:1、只有排在H前面的金属才能置换出酸里的氢
2、只有排在前面的金属才能将排在后面的金属从它的盐溶液中置换出来
五.物质的化学名称、俗名和化学式
汞(水银)Hg 硫(硫磺)S 氧化钙(生石灰)CaO
氯化钠(食盐)NaCl 固体二氧化碳(干冰) 氧化铁(铁锈的主要成分)
氧化铁(铁锈的主要成分)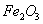
碳酸钙(大理石、石灰石、方解石)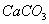 碱式碳酸铜(铜绿、孔雀石)
碱式碳酸铜(铜绿、孔雀石)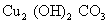
甲烷(沼气)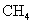 乙醇(酒精)
乙醇(酒精)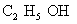 乙酸(醋酸)
乙酸(醋酸)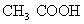
碳酸钠(纯碱) 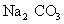 硫酸铜晶体(蓝矾、胆矾)
硫酸铜晶体(蓝矾、胆矾)
氢氧化钠(烧碱、火碱、苛性钠)NaOH 氢氧化钙(熟石灰、消石灰)
水煤气:氢气和一氧化碳的混合物 爆鸣气:氢气和氧气的混合物
碳酸钠 (苏打、纯碱) 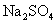 碳酸氢钠 (小苏打、重碱 )
碳酸氢钠 (小苏打、重碱 ) 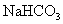
硫代硫酸钠 (大苏打、海波) 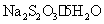 硫酸铝钾 (明矾)
硫酸铝钾 (明矾) 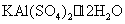
重铬酸钾 (红矾) 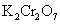 碳酸钾 (钾碱、草碱、草木灰)
碳酸钾 (钾碱、草碱、草木灰) 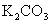
硫酸钙 (生石膏、石膏 )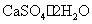 硫酸钙 (熟石膏、烧石膏)
硫酸钙 (熟石膏、烧石膏) 
第二篇:初中化学方程式(上册总结)
初中化学方程式(上册总结)
一.初中化学方程式(上册)
1.加热高锰酸钾(实验室制氧气原理1):2KMnO=KMnOM+ nO O+ 4
?
2
4
2
2
?
OMn
2
2.过氧化氢在二氧化锰作催化剂条件下分解(实验室制氧气原理2):2HO2=2HO+ 2
MnO2
?
22
?
3.氯酸钾用二氧化锰做催化剂分解制氧气(实验室制氧气原理3):2KClO3===2KCl+3O2? 4.碳在氧气中燃烧:C+O2??CO2
现象:(1)发出白光(2)放出热量(3)生成一种能使澄清石灰水变浑浊的气体
??2CO5.碳与氧气反应:2C+O2(不充足)
点燃
点燃
点燃
6.红磷白磷在氧气中燃烧(研究空气组成的实验):4P+5O2??2P2O5
现象:(1)发出黄光(2)生成大量白烟(3)放出热量
7.硫在空气氧气中燃烧:S+O2??SO2
现象:A、在纯的氧气中燃烧 (1)发出明亮的蓝紫火焰(2)放出热量(3)生成一种有刺激性气味的气体
B、在空气中燃烧 (1)发出微弱的淡蓝色火焰(2)放出热量(3)生成一种有刺激性气味的气体
点燃
点燃
8.铁丝在氧气中燃烧:3Fe+2O2??Fe3O4
现象:(1)剧烈燃烧,火星四射(2)放出热量(3)生成一种黑色固体
点燃
9.镁带在空气氧气中燃烧:2Mg+O2??2MgO
现象:(1)发出耀眼的白光(2)放出热量(3)生成白色粉末
10.大理石和稀盐酸(实验室制二氧化碳原理):CaCO3+2HCl == CaCl2+H2O+CO2?
11. 二氧化碳使澄清石灰水变浑浊(鉴别二氧化碳气体):CO2+Ca(OH)2 == CaCO3?+H2O12.二氧化碳与水反应:CO2+H2O == H2CO3 13.碳酸不稳定分解:H2CO3==H2O+CO2?
14.高温煅烧石灰石(工业制取二氧化碳原理):CaCO3==CaO+CO2? 15. 生石灰和水反应:CaO+H2O == Ca(OH)2
16. 电解水实验(研究水的组成实验):2H2O==2H2?+ O2? 17.氢气和氧气点燃:2H2+O2??2H2O
现象:(1)产生淡蓝色火焰(2)放出热量(3)烧杯内壁出现水雾
点燃
通电
高温
?
18.锌与稀硫酸反应(实验室制氢气原理): Zn+ H2SO4==ZnSO4 + H2?
19.一氧化碳点燃:2CO+O2??2CO2
现象:(1)发出蓝色的火焰(2)放热(3)澄清石灰水变浑浊
点燃
20.单质碳的还原性:
(1)炭还原氧化铜:
高温
C+2CuO====2Cu+CO2↑
现象:固体又黑色变为红色,生成能使澄清的石灰水变浑浊的气体 (2)焦炭还原氧化铁:3C+ 2Fe2O3==4Fe + 3CO2?(3)碳还原二氧化碳:CO2 + C==2CO
高温
21.CO还原氧化铜:CuO+CO====Cu+CO2
高温
高温
现象:固体有黑色变为红色,生成能使澄清的石灰水变浑浊的气体
22.氢气还原氧化铜: H2 + CuO==Cu + H2O
23.碳酸钠和稀盐酸反应(灭火器原理):Na2CO3+2HCl==2NaCl+H2O+CO2? 24.铁和硫酸铜溶液反应(湿法炼铜原理):Fe+CuSO4== Cu+FeSO4
现象:(1)铁表面覆盖一层红色的物质(2)溶液由蓝色变成浅绿色
?
25.甲烷在空气中燃烧:CH4+2O2==CO2+2H2O
26.乙醇(酒精)在空气中燃烧:C2H5OH+3O2==2CO2+3H2O
点燃
点燃
二.物质的化学名称、俗名和化学式
汞(水银)Hg 硫(硫磺)S 氧化钙(生石灰)CaO
氯化钠(食盐)NaCl 固体二氧化碳(干冰)CO2 氧化铁(铁锈的主要成分)Fe2O3
碳酸钙(大理石、石灰石、方解石)CaCO3 甲烷(沼气)CH4 乙醇(酒精)C2 H5 OH 碳酸钠(纯碱) Na2 CO3 氢氧化钙(熟石灰、消石灰)Ca(OH)2
第三篇:个人学习和工作情况总结
大学四年,于我而言是人生中非常重要的四年。在领导的关心和照顾下,我不断进步成长,在学习,工作,生活中都收获颇丰。现将我大学四年的学习和工作总结如下。
学习方面
我深知21世纪是知识爆炸的时代,知识改变命运,因此,我从未放松过自己对学习的要求。在学习上,我不断提高自己的学习自制力和自主性,使自己无论处于什么环境,都能拒绝诱惑,积极认真地投入到学习中。我也非常注重学习经验和方法的总结。我认为好的方法可以帮助我们达到事半功倍的效果。所以,我在时间的安排上遵循科学规律,使学习达到效率最大化。大学是富含学习资源的地方,所以我积极阅读涉猎知识,扩大自己的知识面。我坚持独立思考,提高自己的逻辑思维能力,这可以让我们受用一生。
正是凭借这这份对学习的热爱与认真,我大学四年都获得了优异的学习成绩。平均绩点在3.5以上。20xx~20xx学年度,我获得了校级二等奖学金 及“三好学生”称号。20xx~20xx学年度,我获得了“学习优秀生”称号。在英语氛围不浓的生物专业背景下,我通过自己的努力,过了大学英语六级。生命不息,学习不止。
工作方面
从大一刚进大学校园,我便积极投入到校园工作中。很荣幸地,我被吸收成为系文娱部的一名干事。从此开始了我长达三年的学生会工作历程。20xx年,我参与部长竞选,成为了系文娱部部长,组织构建部门文化,培训指导部门成员,多次组织系内大小型文艺汇演活动,歌唱比赛,舞蹈比赛等,丰富同学们的课余生活。这极大地培养和提高了我的组织能力,创新能力及独立思考的能力。
20xx年x月,我从多个竞选者中脱颖而出,成为我系学生会团总支书记。除了协助辅导员完成各类通知和工作的上传下达,我还积极协调学生会各部门的关系,加强部门与部门间的合作与交流,提升学生会的整体凝聚力和集体荣誉感。
除了学生会的职务,我还是班里的一名班干部。20xx年,在同学们的推选下,我成为了班里的文娱委员,负责班级里的文娱活动,策划并组织班级出游活动、各类知识技能竞赛;参与班级综合测评工作,和其他班干部良好互动,共同提高班级凝聚力。
大学四年,我既努力让自己成为一名优秀大学生,也不断尝试走出校园,体验社会带给我们的洗礼。这其中,包括各种志愿者工作,学校实习和支教工作。
20xx年的广东省运动会和20xx年的世界大学生运动会,我都是大学生志愿者中的一员。在志愿者的队伍中,我兢兢业业,认真负责地做好自己岗位上的事情,也因此,我被评为“省运会优秀志愿者”和“大运会优秀志愿者”称号。我将会坚定不移地走在志愿者的道路上,用自己的微薄之力帮助他人。
20xx年,我积极参与学校发起的义教活动,深入偏远地区的小学进行教学。尽管每个星期都要走一段很长很长的路去上课,但内心是快乐充实的,没有什么比看到小孩的笑脸更让人满足的了!
20xx年,我有幸成为一名生物实习教师。我认真向富有教学经验的教师学习,请教,他们也非常乐意地为我指点,传授教学经验。尽管只有短短的两个月,但我的教学技能和教学理论水平都得到了极大的提高!我希望,在教育领域,我可以越走越远,越走越宽广!
思想方面
在思想政治方面,我认真学习贯彻“三个代表”重要思想,坚定不移拥护中国共产党,努力提高思想政治觉悟以及自身修养。20xx年x月,经过一年的考核期,我成为了一名正式党员,从此,我以更高的标准要求自己,时刻提醒自己作为一名党员该有的素养。
以上是我对自己大学四年基本情况的总结。在这即将毕业的时刻,我要以崭新的姿态,走进明天,走向未来!
总结者:
年月日
-
个人学习和工作情况总结
大学四年,于我而言是人生中非常重要的四年。在领导的关心和照顾下,我不断进步成长,在学习,工作,生活中都收获颇丰。现将我大学四年的学…
-
大一学习总结
春去秋来,日复一日,大一学年生活,虽然短暂,但我过得充实而快乐。转眼间,在大学已经呆了一年多了。记得刚进大学时对大学充满了各种憧憬…
-
学习总结
无人旋翼机学习总结第一部分笔记整理无人机基础知识固定翼固定翼机英文Fixedwingaircraft泛指比空气重有动力装置驱动机翼…
-
个人学习总结
我是20xx春乡镇企业管理专业的一名学生,在平湖电大三年的学习时间即将结束。在这里学习的学生基本上都是利用业余时间来进修的,每天除…
-
学习总结
20xx年高考一轮研讨学习总结与反思一瞠目结舌的变局我称之为瞠目结舌或许带有强烈的个人感情色彩但是对突然要面对20xx年全新的高考…
-
行政部工作总结
、上半年工作总结;1继续健全公司各项规章制度,进一步提高公司规范化运作水平;在公司原有制度的基础上,完善了《12小时工作制》、《文…
-
院新闻中心记者团20xx下学期工作总结-
工作总结不知不觉,20xx年已经接近尾声,今年记者团的工作也暂时告一段落了。与上学期相比,这学期显得格外的短。尽管如此,我们办公室…
-
总务工作总结
学校总务后勤工作是学校工作的重要组成部分,与教学一样,是学校的两大支柱之一,同时具有鲜明的服务保障性、经济性和教育性相统一的特征。…
-
20xx年度小继教个人学习总结
20xx年度小继教个人学习总结翁下小学:杨廷刚通过本年度继续教育培训的学习,使我在教育思想,教育理论及业务能力等方面受益。我深切地…
-
纪委监察室 20xx年上半年工作总结
一、认真学习,抓好自身建设认真学习三个代表重要思想和党的十七大会议精神,以及中央纪委第七次全会精神,坚定理想信念,加强道德修养,强…