高考统计知识点总结
第二章:统计
1、抽样方法:
①简单随机抽样(总体个数较少) ②系统抽样(总体个数较多)
③分层抽样(总体中差异明显)
注意:在N个个体的总体中抽取出n个个体组成样本,每个个体被抽到的机会(概率)均为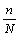 。
。
2、总体分布的估计:
⑴一表二图:
①频率分布表——数据详实 ②频率分布直方图——分布直观③频率分布折线图——便于观察总体分布趋势 注:总体分布的密度曲线与横轴围成的面积为1。
⑵茎叶图:
①茎叶图适用于数据较少的情况,从中便于看出数据的分布,以及中位数、众位数等。
②个位数为叶,十位数为茎,右侧数据按照从小到大书写,相同的数据重复写。
3、总体特征数的估计:
⑴平均数: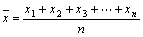 ; 取值为
; 取值为 的频率分别为
的频率分别为 ,则其平均数为
,则其平均数为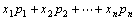 ; 注意:频率分布表计算平均数要取组中值。
; 注意:频率分布表计算平均数要取组中值。
⑵方差与标准差:一组样本数据 方差:
方差: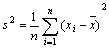 ;标准差:
;标准差: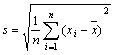
注:方差与标准差越小,说明样本数据越稳定。
平均数反映数据总体水平;方差与标准差反映数据的稳定水平。
⑶线性回归方程
①变量之间的两类关系:函数关系与相关关系; ②制作散点图,判断线性相关关系
③线性回归方程: (最小二乘法)
(最小二乘法)
 注意:线性回归直线经过定点
注意:线性回归直线经过定点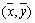 。
。
第三章:概率
1、随机事件及其概率:
⑴事件:试验的每一种可能的结果,用大写英文字母表示;⑵必然事件、不可能事件、随机事件的特点;
⑶随机事件A的概率: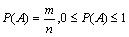 .
.
2、古典概型:
⑴基本事件:一次试验中可能出现的每一个基本结果;⑵古典概型的特点:
①所有的基本事件只有有限个;
②每个基本事件都是等可能发生。
⑶古典概型概率计算公式:一次试验的等可能基本事件共有n个,事件A包含了其中的m个基本事件,则事件A发生的概率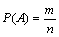 .
.
3、几何概型:⑴几何概型的特点:①所有的基本事件是无限个;②每个基本事件都是等可能发生。
⑵几何概型概率计算公式: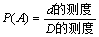 ;
;
其中测度根据题目确定,一般为线段、角度、面积、体积等。
4、互斥事件:
⑴不可能同时发生的两个事件称为互斥事件;
⑵如果事件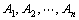 任意两个都是互斥事件,则称事件
任意两个都是互斥事件,则称事件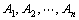 彼此互斥。
彼此互斥。
⑶如果事件A,B互斥,那么事件A+B发生的概率,等于事件A,B发生的概率的和,
即: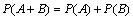
⑷如果事件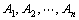 彼此互斥,则有:
彼此互斥,则有: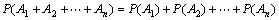
⑸对立事件:两个互斥事件中必有一个要发生,则称这两个事件为对立事件。
①事件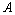 的对立事件记作
的对立事件记作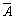
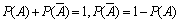
②对立事件一定是互斥事件,互斥事件未必是对立事件。
1、基本概念
⑴互斥事件:不可能同时发生的两个事件.
如果事件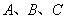 ,其中任何两个都是互斥事件,则说事件
,其中任何两个都是互斥事件,则说事件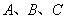 彼此互斥.
彼此互斥.
当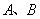 是互斥事件时,那么事件
是互斥事件时,那么事件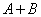 发生(即
发生(即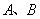 中有一个发生)的概率,等于事件
中有一个发生)的概率,等于事件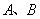 分别发生的概率的和,即
分别发生的概率的和,即 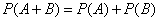 .
.
⑵对立事件:其中必有一个发生的两个互斥事件.事件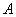 的对立事件通常记着
的对立事件通常记着 .对立事件的概率和等于1.
.对立事件的概率和等于1. 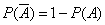 .
.
特别提醒:“互斥事件”与“对立事件”都是就两个事件而言的,互斥事件是不可能同时发生的两个事件,而对立事件是其中必有一个发生的互斥事件,因此,对立事件必然是互斥事件,但互斥事件不一定是对立事件,也就是说“互斥”是“对立”的必要但不充分的条件.
⑶相互独立事件:事件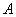 (或
(或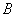 )是否发生对事件
)是否发生对事件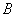 (或
(或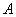 )发生的概率没有影响,(即其中一个事件是否发生对另一个事件发生的概率没有影响).这样的两个事件叫做相互独立事件.
)发生的概率没有影响,(即其中一个事件是否发生对另一个事件发生的概率没有影响).这样的两个事件叫做相互独立事件.
当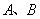 是相互独立事件时,那么事件
是相互独立事件时,那么事件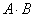 发生(即
发生(即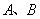 同时发生)的概率,等于事件
同时发生)的概率,等于事件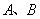 分别发生的概率的积.即
分别发生的概率的积.即 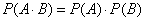 .
.
若A、B两事件相互独立,则A与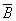 、
、 与B、
与B、 与
与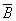 也都是相互独立的.
也都是相互独立的.
⑷独立重复试验
①一般地,在相同条件下重复做的 次试验称为
次试验称为 次独立重复试验.②独立重复试验的概率公式
次独立重复试验.②独立重复试验的概率公式
如果在1次试验中某事件发生的概率是 ,那么在
,那么在 次独立重复试验中这个试验恰好发生
次独立重复试验中这个试验恰好发生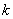 次的概率
次的概率
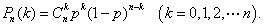
⑸条件概率:对任意事件A和事件B,在已知事件A发生的条件下事件B发生的概率,叫做条件概率.记作P(B|A),读作A发生的条件下B发生的概率.公式: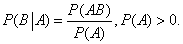
2、离散型随机变量
⑴随机变量:如果随机试验的结果可以用一个变量来表示,那么这样的变量叫做随机变量 随机变量常用字母
随机变量常用字母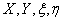 等表示.
等表示.
⑵离散型随机变量:对于随机变量可能取的值,可以按一定次序一一列出,这样的随机变量叫做离散型随机变量.
⑶连续型随机变量: 对于随机变量可能取的值,可以取某一区间内的一切值,这样的变量就叫做连续型随机变量.
⑷离散型随机变量与连续型随机变量的区别与联系: 离散型随机变量与连续型随机变量都是用变量表示随机试验的结果;但是离散型随机变量的结果可以按一定次序一一列出,而连续性随机变量的结果不可以一一列出.
若 是随机变量,
是随机变量,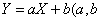 是常数)则
是常数)则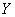 也是随机变量
也是随机变量 并且不改变其属性(离散型、连续型).
并且不改变其属性(离散型、连续型).
3、离散型随机变量的分布列
⑴概率分布(分布列)
设离散型随机变量 可能取的不同值为
可能取的不同值为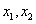 ,…,
,…,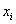 ,…,
,…, ,
,
 的每一个值
的每一个值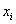 (
( )的概率
)的概率 ,则称表
,则称表

为随机变量 的概率分布,简称
的概率分布,简称 的分布列.性质:①
的分布列.性质:①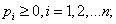 ②
②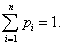
⑵两点分布 如果随机变量 的分布列为
的分布列为

则称 服从两点分布,并称
服从两点分布,并称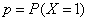 为成功概率.
为成功概率.
⑶二项分布
如果在一次试验中某事件发生的概率是p,那么在n次独立重复试验中这个事件恰好发生k次的概率是
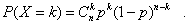
其中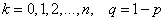 ,于是得到随机变量
,于是得到随机变量 的概率分布如下:
的概率分布如下:

我们称这样的随机变量 服从二项分布,记作
服从二项分布,记作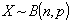 ,并称p为成功概率.
,并称p为成功概率.
判断一个随机变量是否服从二项分布,关键有三点:
①对立性:即一次试验中事件发生与否二者必居其一;②重复性:即试验是独立重复地进行了 次;
次;
③等概率性:在每次试验中事件发生的概率均相等.
注:⑴二项分布的模型是有放回抽样;⑵二项分布中的参数是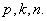
⑷超几何分布 一般地, 在含有 件次品的
件次品的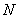 件产品中,任取
件产品中,任取 件,其中恰有
件,其中恰有 件次品数,则事件
件次品数,则事件 发生的概率为
发生的概率为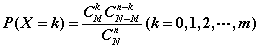 ,于是得到随机变量
,于是得到随机变量 的概率分布如下:
的概率分布如下:

其中 ,
,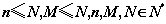 .
.
我们称这样的随机变量 的分布列为超几何分布列,且称随机变量
的分布列为超几何分布列,且称随机变量 服从超几何分布.
服从超几何分布.
注:⑴超几何分布的模型是不放回抽样;
⑵超几何分布中的参数是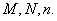 其意义分别是 总体中的个体总数、N中一类的总数、样本容量.
其意义分别是 总体中的个体总数、N中一类的总数、样本容量.
4、离散型随机变量的均值与方差
⑴离散型随机变量的均值 一般地,若离散型随机变量 的分布列为
的分布列为

则称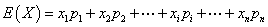 为离散型随机变量
为离散型随机变量 的均值或数学期望(简称期望).它反映了离散型随机变量取值的平均水平.
的均值或数学期望(简称期望).它反映了离散型随机变量取值的平均水平.
性质:①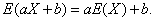 ②若
②若 服从两点分布,则
服从两点分布,则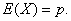
③若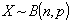 ,则
,则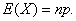
⑵离散型随机变量的方差
一般地,若离散型随机变量 的分布列为
的分布列为

则称
 为离散型随机变量
为离散型随机变量 的方差,并称其算术平方根
的方差,并称其算术平方根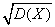 为随机变量
为随机变量 的标准差.它反映了离散型随机变量取值的稳定与波动,集中与离散的程度.
的标准差.它反映了离散型随机变量取值的稳定与波动,集中与离散的程度.

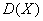 越小,
越小, 的稳定性越高,波动越小,取值越集中;
的稳定性越高,波动越小,取值越集中;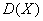 越大,
越大, 的稳定性越差,波动越大,取值越分散.
的稳定性越差,波动越大,取值越分散.
性质:①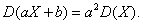
②若 服从两点分布,则
服从两点分布,则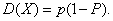
③若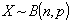 ,则
,则
5、正态分布
正态变量概率密度曲线函数表达式: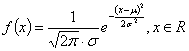 ,其中
,其中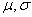 是参数,且
是参数,且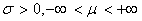 .记作
.记作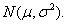 如下图:
如下图:
专题八:统计案例
1、回归分析
回归直线方程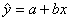 ,
,
其中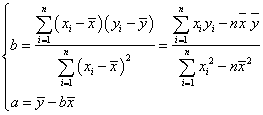
 相关系数:
相关系数: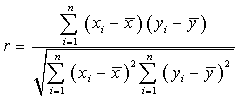
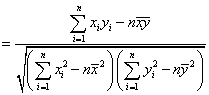
2、独立性检验
假设有两个分类变量X和Y,它们的值域分另为{x1, x2}和{y1, y2},其样本频数2 2列联表为:
2列联表为:
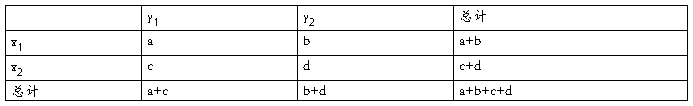
若要推断的论述为H1:“X与Y有关系”,可以利用独立性检验来考察两个变量是否有关系,并且能较精确地给出这种判断的可靠程度.
具体的做法是,由表中的数据算出随机变量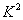 的值
的值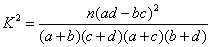 ,其中
,其中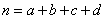 为样本容量,K2的值越大,说明“X与Y有关系”成立的可能性越大.
为样本容量,K2的值越大,说明“X与Y有关系”成立的可能性越大.
随机变量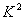 越大,说明两个分类变量,关系越强;反之,越弱。
越大,说明两个分类变量,关系越强;反之,越弱。
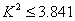 时,X与Y无关;
时,X与Y无关;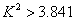 时,X与Y有95%可能性有关;
时,X与Y有95%可能性有关; 时X与Y有99%可能性有关.
时X与Y有99%可能性有关.
第二篇:高考必备重要知识点---有机化学计算总结--((免费下载)
《有机化学计算》
【有机化学计算与基础知识】
化学计算的特点是数学运算和化学知识的有机结合, 计算要在理解化学原理和化学知识的基础上进行。化学计算的正确与否的关键在于对化学概念含义的理解和对化学基础知识的掌握, 并在此基础上掌握化学计算的解题规律。
注意:
1、牢固掌握各有机物的性质、各有机物之间的相互关系、有关有机物之间的化学反应及化学反应方程式
2、有关重要计算公式
(1)根据标准状况下的气体密度 算出该气体的摩尔质量即该气体的分子量
算出该气体的摩尔质量即该气体的分子量
(2)根据气体的相对密度D, 求气体的分子量
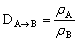
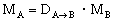
( 密度, M分子量)
密度, M分子量)
(3)求混和气的平均分子量:
①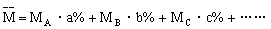 (a%, b%, c%……表示摩尔百分含量)
(a%, b%, c%……表示摩尔百分含量)
②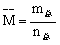 (m为质量, n为物质的量)
(m为质量, n为物质的量)
3、定式思维:
化合物各元素的质量含量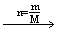 原子个数比
原子个数比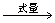 分子式
分子式
4、阿伏加德罗定律及其应用:
阿伏加德罗定律: 在相同的温度和压强下, 相同体积的任何气体都含有相同数目的分子。推知非标况气态方程
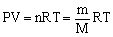 (P为压强、V为体积、n为物质的量、R为常数、T为绝对温度、m为质量、M为摩尔质量)
(P为压强、V为体积、n为物质的量、R为常数、T为绝对温度、m为质量、M为摩尔质量)
定T、定P: 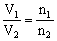 定T定V:
定T定V: 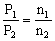
【有机化学计算题型】
1、求分子量
2、求分子式或结构简式
3、有机物燃烧问题
4、混合物组成
5、有机化学计算的综合应用
5、重要有机物的通式要记熟



6、有机物完全燃烧化学方程式为
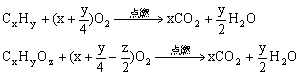
燃烧规律的应用
(1)最简式相同的有机物, 以任意比例混合总质量一定时, 生成的CO2是一定值, 生成水的量也是定值, 消耗氧的量也是定值。
(2)混合物总质量不变, 以任意比例混合时, 生成CO2相等, 即含碳量相等(质量分数), 生成H2O相等, 即含氢量相等(质量分数)
(3)具有相同碳原子数的有机物, 无论以任意比例混合, 只要总物质的量一定, 生成的CO2为一定值。
(4)最简式相同, 无论有多少种有机物, 也无论以何种比例混合, 混合物中元素质量比为定值。
7、记忆常见最简式相同的物质为:
单烯烃、互为同分异构体的有机物、乙炔和苯、甲醛和乙酸、葡萄糖。
8、记熟某些有机物的分子量



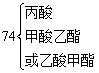

【题型与解法】
(一)求有机物分子量
根据化学方程式的有关计算求物质的分子量
《例1》某饱和一元醇3.2克跟足量的钠反应, 放出的氢气在标况状况下的体积为1120毫升, 求这饱和一元醇的分子量?
解: 设饱和一元醇为R-OH, 分子量为x
2ROH + 2Na®2RONa + H2
2xg 22.4L
3.2g 1.12L
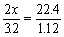 x = 32
x = 32
答: 该饱和一元醇分子量为32。
(二)求有机物的分子式
《例2》某气态烃含碳、氢元素质量比为6∶1, 又知同温、同压下该气体密度为氢气密度的14倍, 求该烃的分子式:
解Ⅰ: 根据分子量、通过最简式求分子式
该烃的摩尔质量M = 14×2g / mol = 28g / mol
该烃n(C)∶n(H) =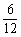 ∶
∶ =1∶2
=1∶2
最简式 CH2 式量 = 12 + 2 = 14
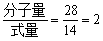 ∴分子式为C2H4
∴分子式为C2H4
解Ⅱ: 根据分子量、通过计算每摩物质分子量所含各元素的原子的“物质的量”求分子式
该烃的摩尔质量M = 14×2g / mol = 28g / mol
1摩该烃分子量n(C) = 
1摩该烃分子量n(H) = 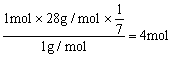
∴该烃分子式为C2H4
《例3》某气态烃有机物标准状况下密度为1.34克/升, 取1.50克该有机物在足量的氧气中燃烧。将所得气体通过装有浓H2SO4的洗气瓶后再通过碱石灰干燥管, 结果洗气瓶和干燥管分别增重0.9克和2.2克, 测得尾气中除氧气外无其它物质, 求该有机物的分子式?
解Ⅰ: 根据有机物燃烧化学方程式(通式)的有关计算求分子式
摩尔质量M = 1.34g / L×22.4L / mol = 30g / mol
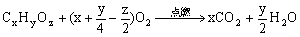
30g xmol 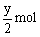
1.50g 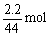
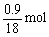
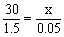 x = 1
x = 1
 y = 2
y = 2
分子量 = 30 1×12 + 1×2 + 16×z = 30 z = 1
∴分子式CH2O 答(略)
解Ⅱ: 根据关系式的有关计算求分子式
摩尔质量M = 1.34g / L×22.4L / mol = 30g / mol
关系式 C~CO2
12g 44g
x 2.2g 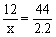 x = 0.6g
x = 0.6g
2H~H2O
2g 18g
y 0.9g 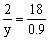 y = 0.1g
y = 0.1g
0.6g + 0.1g<1.50g ∴有机物中含氧元素
n(C)∶n(H)∶n(O) = 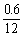 ∶
∶ ∶
∶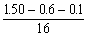 = 1∶2∶1
= 1∶2∶1
最简式 CH2O 式量 = 30
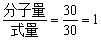 ∴分子式CH2O 答(略)
∴分子式CH2O 答(略)
《例4》某气态不饱和烃在标准状况下的密度为2.41克/升。取0.54克该烃恰与浓度为0.2摩/升的溴水100毫升完全反应, 使溴水完全褪色。求该烃的分子式、结构简式及名称?
根据有机物分子式通式求有机物分子式
解: 摩尔质量M = 2.41g / L×22.4L / mol = 54g / mol
n(CxHy) = 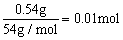
n(Br2) = 0.2mol / L×0.1L = 0.02mol
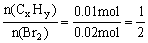
∴该烃为炔烃或二烯烃
依据CnH2n-2通式 12n + 2n-2 = 54 n = 4
∴分子式为C4H6
结构简式  名称: 1—丁炔
名称: 1—丁炔
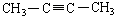 名称: 2—丁炔
名称: 2—丁炔
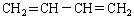 名称: 1, 3—丁二烯
名称: 1, 3—丁二烯
《例5》标准状况下10毫升某气态烷烃跟80毫升过量的氧气混合, 通入一个容积为90毫升的密闭容器中点火爆炸后, 恢复到原状态, 测得的压强为原来的55.56%。求烷烃的分子式?
解Ⅰ: 利用燃烧化学方程式计算
CnH2n+2 + 
 nCO2 + (n + 1) H2O (标况下水为液态)
nCO2 + (n + 1) H2O (标况下水为液态)
1mL 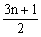 mL nmL
mL nmL
10mL x 10nmL
 x = 5(3n + 1)mL
x = 5(3n + 1)mL
依据题意 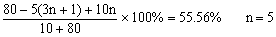
∴烷烃的分子式为C5H12
解Ⅱ: 根据反应前后压强变化, 通过差量法解题求有机物分子式
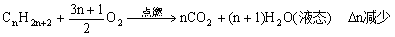
1mol 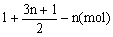
10mol (10 + 80)·(1-55.56%)(mol)
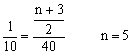
∴烷烃分子式为C5H12
《例6》某有机物由C、H、O三种元素组成, 分子中含有8个原子。1摩该有机物含有46摩质子, 完全燃烧该有机物在相同条件下测定CO2和水蒸气体积比为2∶1。取2.7克该有机物恰好与1摩/升的碳酸钠溶液30毫升完全反应, 求(1)有机物分子式?(2)有机物结构简式?
利用解联立方程组法求有机物分子式
解: 设有机物分子式CxHyOz
根据题意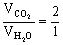 ∴
∴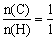
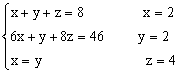 ∴分子式C2H2O4
∴分子式C2H2O4
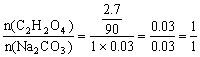
∴有机物为二元羧酸 结构简式
(三)有机物燃烧问题
《例7》一定量的甲烷不完全燃烧, 生成由CO、CO2和H2O(气)组成的混合气体49.6克, 将混合气体缓慢通过无水CaCl2并作用完全、CaCl2质量增加25.2克, 计算混合气中CO、CO2和H2O(气)的物质的量?若将此甲烷完全燃烧还缺少标准状况下多少升氧气?
解Ⅰ: 通过联立方程组法解题:
由题意得知m(H2O) = 25.2g ∴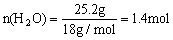
m(CO) + m(CO2) = 49.6g-25.2g = 24.4g
∵关系式 CH4~2H2O
1mol 2mol
0.7mol 1.4mol
∴n(CO) + n(CO2) = 0.7mol
设: 生成CO的物质的量为x、生成CO2物质的量为y。
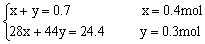
设: 此甲烷完全燃烧还需标况下氧气体积为z
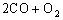
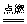 2CO2
2CO2
2mol 22.4L
0.4mol z 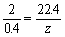
z = 4.48(L) 答(略)
解Ⅱ: 通过平均值法解题
由题意得知m(H2O) = 25.2g ∴n(H2O) =  = 1.4mol
= 1.4mol
∴m(CO) + m(CO2) = 49.6g-25.2g = 24.4g
∵关系式 CH4~2H2O
1mol 2mol
0.7mol 1.4mol
∴n(CO) + n(CO2) = 0.7mol
∴CO与CO2混合气平均摩尔质量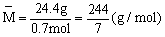
十字交叉法

∴n(CO) = 0.7mol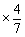 = 0.4mol
= 0.4mol
n(CO2)= 0.7mol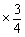 = 0.3mol
= 0.3mol
设此甲烷完全燃烧还需标况下氧气体积为x
2CO + O2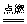 2CO2
2CO2
2mol 22.4L
0.4mol x 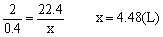 答(略)
答(略)
《例8》把MmolH2和NmolC2G4混合, 在一定条件下使它们一部分发生反应生成WmolC2H6, 将反应后所得的混合气体完全燃烧, 消耗氧气的物质的量为多少?
利用守恒法解决可燃物完全燃烧时耗氧量
分析: 反应过程
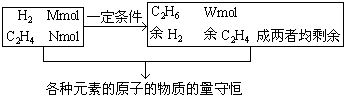
∴不用讨论和计算多少H2、多少C2H4参加了反应及剩余多少H2、C2H4再按混合物各成分计算耗氧量。可按反应物各组分, 分别计算它们完全燃烧耗氧量即为答案。
解: 2H2 + O2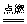 2H2O C2H4 + 3O2
2H2O C2H4 + 3O2 2CO2 + 2H2O
2CO2 + 2H2O
2mol 1mol 1mol 3mol
Mmol Nmol 3Nmol
Nmol 3Nmol
∴耗氧量为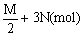
《例9》标准状况下, 将1升CH4、2升C2H6的混合气体, 向该混合气体通入相同状况下50升的空气, 完全燃烧后, 所得气体经干燥恢复到原状态, 气体总体积为多少升?
利用差量法解题
解: 
CH4~2O2 C2H6~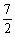 O2
O2
1升 2升 2升 7升
2升 + 7升<10.5升 ∴CH4、C2H6适量
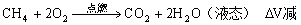
1升 (3-1)升 = 2升

2升 (2 + 7-4)升= 5升
∴V气体总 = 1 + 2 + 50-(2 + 5)= 46升 答(略)
《例10》平均分子量为30.4CO、C2H4和O2混合气体经点燃完全反应后, 测知反应后混合气体不再含CO和C2H4。试推算原混合气体各成分的体积分数?(确定体积组成范围)
利用含不等式联立方程组法及平均值法解题。
解: 认真分析混合气组成中各组分的分子量, 可以看出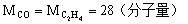
∴平均值法解出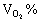 (体积分数)
(体积分数)
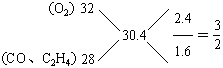 ∴
∴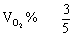 ×100% = 60%
×100% = 60%
∵2CO + O2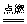 2CO2 C2H4 + 3O2
2CO2 C2H4 + 3O2 2CO2 + 2H2O
2CO2 + 2H2O
2V V 1V 3V
x 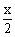 y 3y
y 3y
CO、C2H4共占40%
采用整体设“一”法解题
设混合气总体积为100(L)、CO气体积为x, C2H4气体积为y。
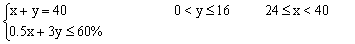
答: 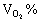 为60% 24%
为60% 24%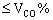 <40%
<40% 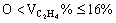
(四)有关混合物组成有机计算:
《例11》相同状况下9升甲烷与6升某烯烃混合, 所得混合气的密度等于相同条件下氧气的密度, 求该烯烃的分子式、可能的结构简式?
平均值法解题
解: 混合气平均摩尔质量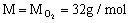
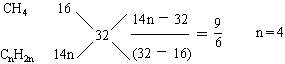
∴烯烃分子式为C4H8
可能结构简式 CH3-CH = CH-CH3 CH3-CH2-CH = CH2

《例12》丁烷、甲烷、二氧化碳的混合气体其密度是同条件下氢气的22倍, 又知其中二氧化碳占混合气体体积的62.5%, 则三种气体的体积比是
A.1∶2∶5 B.5∶2∶1
C.5∶1∶5 D.2∶1∶5
答案: D
解: 混合气平均摩尔质量M = 22×2g / mol = 44g / mol
∵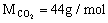
∴CO2气体体积分数不影响混合气平均摩尔质量, 因此应由丁烷、甲烷的体积分数确定答案, 它们体积分数必须满足下列关系

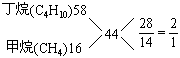
∴D为答案
《例13》两种气态烃组成的混合物(分子中碳原子数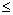 4)20毫升, 与过量氧气混合充分燃烧, 燃烧所得气体产物通过浓H2SO4时, 体积减少了30毫升, 剩余气体再通过碱石灰时体积又减少了40毫升(以上气体均在相同状况下测定的), 求这两种气态烃的可能组成及体积百分含量?
4)20毫升, 与过量氧气混合充分燃烧, 燃烧所得气体产物通过浓H2SO4时, 体积减少了30毫升, 剩余气体再通过碱石灰时体积又减少了40毫升(以上气体均在相同状况下测定的), 求这两种气态烃的可能组成及体积百分含量?
根据混合物平均分子组成来确定混合物中各成分及体积百分含量?
解: 设混合气态烃的平均分子组成为CxHy

1mL xmL 
20mL 40mL 30mL
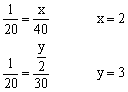
∴平均分子组成C2H3
讨论
(1)一种烃的碳原子数1即CH4, 则另一种烃的碳原子数为3或4。但混合烃氢原子数为3, 那么这种烃的氢原子数必须小于3, 如C3H2、C3H1、C4H2,、C4H1是不存在的。
(2)一种烃的碳原子数为2, 则另一种烃的碳原子数也必须为2, 碳原子数为2的烃C2H2、C2H4、C2H6 其中合理的组合为
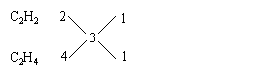


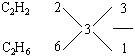
答:(略)
《例14》a毫升A、B、C三种气态烃的混合物跟足量氧气混合点燃后, 恢复到原常温常压状态, 气体体积共缩小了2a毫升, 那么A、B、C三种烃可能是
A.CH4、C2H6、C3H8 B.C2H4、C2H2、CH4
C.CH4、C2H4、C3H4 D.C2H6、C3H6、C4H6
答案: C
解: 依据题意做出敏捷判断解题方法为差量法、平均值法, 设混合气态烃平均分子组成CxHy。
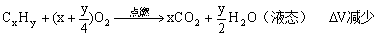
1mL 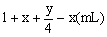
amL 2amL
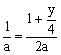 ∴y = 4
∴y = 4
满足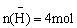 合理
合理
A.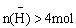 B.
B.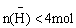
C.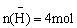 D.
D.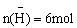
∴选C
-
高考知识点总结
知识点一商周主要政治制度1.分封制(概念解释:又称分封建国、封邦建国、封建)(1)目的:巩固周王朝、奴隶主贵族的统治。(阶级利益…
-
高二小高考知识点总结
江苏省马坝高级中学20xx年学业水平测试化学考前指导八考点二十:化学与生活专题一洁净安全的生存环境一、大气质量的改善1、空气质量报…
-
化学高考知识点总结1
化学高考知识点总结一、俗名无机部分:纯碱、食用碱:Na2CO3小苏打:NaHCO3石膏(生石膏):CaSO4·.2H2O熟石膏:2…
-
高考理综知识点总结
目标理综200物理一静力学二运动学2匀变速直线运动用平均速度思考匀变速直线运动问题总是带来方便VVV1V2S1S2t222T3匀变…
-
高考语文知识点汇总
第一版块古诗文阅读与鉴赏7题33分1名句名篇默写题与文学常识题知识范围课标建议的60个背诵篇目文学常识以中国古代作家为主及60个背…
-
高二小高考知识点总结
江苏省马坝高级中学20xx年学业水平测试化学考前指导八考点二十:化学与生活专题一洁净安全的生存环境一、大气质量的改善1、空气质量报…
-
高考知识点总结
知识点一商周主要政治制度1.分封制(概念解释:又称分封建国、封邦建国、封建)(1)目的:巩固周王朝、奴隶主贵族的统治。(阶级利益…
-
高考不等式知识点总结
①(对称性)a?b?b?a②(传递性)a?b,b?c?a?c③(可加性)a?b?a?c?b?c(同向可加性)a?b,c?d?a?c…
-
高考电化学知识点总结
20xx届高考电化学知识点总结直击高考考点-电化学知识是理论部分的一个重要内容,也是历年高考考查的一个重点。电化学知识既可以综合学…
-
20xx年我校考点工作总结
精心组织无纰漏、齐心协力促圆满——20xx年全国普通高考孝感市综合高中考点工作总结20xx我校继续承担高考考试组织工作,本次高考我…