�����ˮ�� ������
1����0.2mol��LHCN��Һ��0.1mol��L
�� ��
��
������1��1��NaOH��Һ�������Ϻ���Һ�Լ��ԣ����й�ϵʽ����ȷ���� ��A [HCN]��[CN] B [Na]��[CN] C [HCN]��[CN]��[OH] D [HCN]��[CN]��0.1mol��L
2.Ũ�Ⱦ�Ϊ0.1 mol��L�ļ��������������Һ��������Ϻ����й�ϵʽ��ȷ����
( )
A��(Na)��c(HCOO)��c(OH)��c(H) B��c(HCOO)��c(Na)��c(OH)��c(H)
C��c(HCOO)��c(Na)��c(H)��c(OH) D��c(Na)��c(HCOO)��c(OH)��c(H)
�����⿼����ѧ��������ǿ���ε�ˮ����ɵ����գ�
3��������ʵ��NaHCO3��Һ�ʼ��� ��NaHSO4��Һ������ �۳���ʹ�û���(NH4)2SO4��ʹ����������������� �ܼ��������Ӵ����ȥ������ ������CuCl2��Һ����ϡ�����ܽ�CuCl2���� �������ܾ�ˮ ���Ȼ����Һ������ҩȥ��������Ʒ����ģ�++��+����++����+��+��+��1������1��� �����FeCl3��6H2O���壬�����ò���FeCl3���� ��NH4F��Һ�����ò���ƿʢ�š�����������ˮ���йص��� �� ��
A.ȫ�� B.���ڢ����� C.�������� D.��������
�����⿼��ѧ����ȷ��������ˮ��Ĺ��ɺ�Ӧ�ã�
4�ڴ�����Һ�е����̪����Һ��졣���ڸ���Һ���ٵ���������Ȼ�����Һ�����۲쵽�������� ����ԭ����(�����ӷ���ʽ�ͼ�Ҫ����˵��)�� ��
�����⿼����ѧ����Ӱ������ˮ�������֪ʶ�����⣬�漰��ƽ���ƶ��Լ�ָʾ����֪ʶ��
�»�����վ
1����ͬ���ʵ�����������Һ��������ǿ���� �� ��
A.Na2CO3 B.NaNO3 C.Na2SiO3 D.Na2SO3
�����⿼��ѧ�������ˮ���������Һ����ԣ�
2����0.1mol������������1Lˮ�г�ֽ������Һ���������������� �� ��
A.KCl B.Mg(OH)2
C.Na2CO3 D. MgSO4
�����⿼���֪ʶ�������ˮ���������ܽ���ɣ�
3����ͬ�¶ȡ���ͬ���ʵ���Ũ�ȵ�������Һ����CH3COONa ��NaHSO4 ��NaCl ��NaClO����PH�ɴ�С��˳�����У���ȷ���� �� ��
A.�ܢ٢ۢ� B.�٢ܢۢ�
C.�٢ڢۢ� D.�ܢۢڢ�
�������漰����ˮ����ɺ���Һ�������pH��֪ʶ������������������
4��CH3COOH��CH3COONa�����ʵ���������Ƴɵ�ϡ��Һ��PH=4.7������˵���д������ �� ��
A. CH3COOH�ĵ������ô���CH3COONa��ˮ������
B. CH3COONa��ˮ�����ô���CH3COOH�ĵ�������
C. CH3COOH�Ĵ���������CH3COONa��ˮ��
D. CH3COONa�Ĵ���������CH3COOH�ĵ���
�����⿼����ѧ���������⣬����ѧ������ˮ��͵����֪ʶ��������������
5�������ʵ���Ũ�ȵ�����������Һ�У�NH4��Ũ�������ǣ� ��
A��NH4Cl B��NH4HCO3
C��NH4HSO4 D��NH4NO3
�����⿼����Һ����Զ�NH4ˮ���Ӱ�죩
6������ͬ�¶��£�����������ʵ�����Ũ�ȵ�4��ϡ��Һ����Na2SO4����H2SO4����NaHSO4����Na2S���������������ɶൽ�ٵ�˳���� �� ��
A ��=��>��=�� B ��=��>��>��
C ��>��>��>�� D ��>��>��>��
�������ǿ���ѧ���йص���ʵĵ��������ˮ���֪ʶ��
7��ͬʱ��ũ����ʩ�ú�N,P,K�����ֻ���,�Ը������л���:��K2CO3 ��KCl ��Ca(H2PO4)2 �� (NH4)2SO4 �ݰ�ˮ���������������Ϸ�ʽ�� �� ��
A.�٢ۢ� B.�ڢۢ� C.�٢ۢ� D.�ڢۢ� ++
�����⿼�麬N,P,K�����ֻ����ڻ��ʱ�Ƿ�Ӧ����ˮ���������Ӧ�����ͷ�Ч�� 8���ڳ�����,��ˮ�д��ڵ���ƽ�� H2

OA.NaHSO4 B.KAl(SO4)2 C.NaHCO3 D.NaAc
�����⿼������ˮ���ˮ�ĵ����Ӱ�죩
9������Al2(SO4)3,HAc,NaCl,BaCl2������Һ,���Խ���������һ���Լ��� �� �� A.H2SO4 B.AgNO3 C.Na2CO3 D.NaHCO3 �����⿼��ѧ�����ʵļ���
10�����Ȼ����Һ�У����й�ϵʽ��ȷ���� �� ��
-++-A��c��Cl����c��NH4����c��H����c��OH�� B��c��NH4����c��Cl����c��H����c��OH��
C��c��Cl����c��NH4����c��H����c��OH�� D��c��NH4����c��Cl����c��H����c��OH�� �����⿼������Ũ�ȴ�С�Ƚϣ�
11�����������0.4mol/LCH3COONa��0.2mol/LHNO3��Һ��ͣ�����Һ�����й�ϵ��ȷ���� �� �� A��c��Na]>c��CH3COO]>c��NO3]>c��H]>c��OH�� B��c��Na]>c��CH3COO��>c��H]>c��NO3��>c�� OH�� C���������Һ��ˮϡ�����У��ı�ֵ��С D���������Һϡ��10���Ժ�
10
+
-+
+
-+
-+
--+
+
-+
-+
-
H+OH,��Ҫʹˮ�ĵ���̶�����,��ʹc��H������,Ӧ����������ǣ� ��
+-+
?
+-
?
-
[H?]
[CH3COO?]
��Һ��PHֵ�ӽ�7��[NO3]=10mol/L
?
-11
12�������й�˵����ȷ�� �� ��
����ĭ������ڵ���Ͱ��ʢ̼��������Һ�����ܰ���������Һʢ����Ͱ���ԭ����Alˮ�������H�ḯʴ��Ͱ
�ڰ�AlCl3��Һ���ɺ�������,���õ��Ĺ��������Ҫ��Al2O3������AlCl3���������ڼ��ȴٽ�Al��ˮ��,��ʹ���ɵ�HCl��������ʽ��ɢ,��ʹAlˮ����ȫ����Al(OH)3,Al(OH)3���ȷֽ�����Al2O3��
��ˮ������Ҫ�ɷ���CaCO3��Mg(OH)2,�����ϲ���MgCO3,������ΪMgCO3����ˮ,��ʱ�����,ˮ�������˸����ܵ�Mg(OH)2�� ��Na2CO3��Һ��Ӧ�����ڲ������Լ�ƿ��,��������Na2CO3ˮ�����ɼ�,ʹ���������䷴Ӧ���ᡣ ��FeCl3��Һ���þ��˻������������,��������FeCl3ˮ��������Fe(OH)3��Ե�� A.�٢ڢۢ� B. �٢ڢܢ� C. �ڢۢܢ� D.ȫ�� �����⿼��ѧ������ˮ���Ӧ�ã�
13���ε�ˮ��ƽ����ܵ��¶ȡ�Ũ�ȼ�����������ص�Ӱ�죬��������ˮ�ⷴӦ��Fe3++3H2O
3+
3+
3+
+
Fe(OH)3+3H+�����
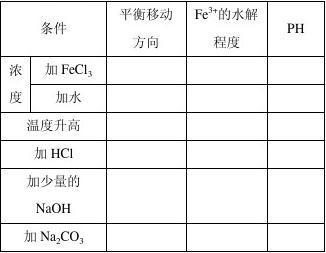
�����⿼��Ӱ��ˮ������أ�
14���ڵ������Һ�У����۴��ڶ������ӣ����������غ��ϵ��
��1������غ㣺�������Һ�����ۺ����������ӣ�����Һ���dzʵ����Եġ���������Һ��________�����ĸ��������һ������_____���������������
����Na2CO3��Һ����__________________ __
��2��ԭ���غ㣨�����غ㣩���������Һ�о�����Щ����ˮ�⡢�����ԭ�����ı䣬��ijԭ�������DZ��ֲ���ġ� ��Na2CO3�д���___________________ _.
��3�������غ㣺�ڶ�Ԫ����������У����ڴ���������ӵĶಽˮ�⣬ÿ��ˮ��Ĺ������������ÿ���һ��H����Һ��
+
�ض����һ��OH������ˮ�ĵ�����һ��������ϵ�� ��Na2CO3�д���___________________ �����⿼��ѧ������Һ�е������غ��Ӧ��������
15��CuCl2��Һ�к���������FeCl2Ϊ�Ʊ�����CuCl2��2H2O���ⶨʵ�鲽����ͼ��ʾ
��

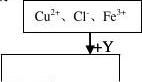

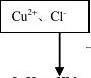
22��ش��������⣺
��1�� �����˵��������� A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4 ��2������Y�� ��3����ȥFe���й����ӷ���ʽ��
��4��Ϊ�˷�ֹˮ�⣬Ҫ�õ�CuCl2��2H2OӦ���Ƶ�һ�������� �� �������ۺϿ����ε�ˮ�⡢������ԭ��Ӧ�����ӷ���ʽ��д��
A. Na2FeO4����Һ����ǿ���ԣ�������ɱ��
B.��Na2FeO4��FeΪ+6�ۣ�����ǿ�����ԣ�������ɱ�� C.Na2FeO4�Ļ�ԭ����Fe3+ˮ��Ϊ Fe(OH)3���壬��ʹˮ�����������۳���
D.Na2FeO4�Ļ�ԭ����Fe2+ˮ��ΪPe(OH)2���壬��ʹˮ�����������۳���
6.þ�۷���NH4Cl��Һ���ܷų�H2��NH3���������������ԭ���� �� �� A.�ǽ���þ��NH3�û�����
B.��þ����ǿ��ԭ�ԣ�NH4���������ԣ�����������ԭ��Ӧ C.����ΪNH4ˮ�������ԣ�Mg��H��Ӧ�ų�H2��ƽ������ D.����ΪMg��ˮ��Ӧ�����ɵ�Mg��OH��2��NH4Cl��Ӧ 7����0.1Ħ/������������Һ�У���������Ũ�ȹ�ϵ����ȷ���� �� �� A.c��Na+��=c��CH3COO-��+c��CH3COOH��
B.c��Na+��+c��OH-��=c��CH3COO-��+2c��CH3COOH��+ c��H+��
C.c��Na+��>c��CH3COO-�� >c��OH-)>c��CH3COOH��> c��H+��
D.c��Na+��>c��OH-��=c��CH3COOH��>c��CH3COO-��> c��H+��
8�������ʵ�������0.1 mol��CH3COOH��CH3COONa���Ƴ�1L�����Һ����֪����c��CH3COO����c��Na�����Ըû��A.c(H)��c(OH)
B.c(CH3COOH)��c(CH3COO)��0.2 mol/L C.c(CH3COOH)��c(CH3COO) D.c(CH3COO)��c(OH)��0.2 mol/L
9����������Һ��ˮ��������Ե���( ) A.Na2S B.NaHCO3 C.Na2HPO4 D.NH4Cl 10��һԪ��HA��Һ�У�����һ����ǿ��MOH��Һ��ǡ��
----+
--+
+
+
+
3+
��B����
1����Na2S��Һ�д����Ŷ������Ӻͷ��ӣ����й�ϵ��ȷ���� �� �� A.��OH��=��HS��+��H��+��H2S�� B.��OH��=��HS��+��H��+2��H2S�� C.��OH��=��HS��+2��H]+��H2S�� D.��Na��>��S��>��OH��>��HS��
2�����ʵĵ�Ũ�ȡ��������ͬ��NaF��NaCN��Һ�У����������Ĺ�ϵ��ȷ����(��֪HF��HCN����) ( B) A.NaF=NaCN B. NaF>NaCN C. NaF<NaCN D.��ȷ��
+
2-----+
--+
--+
������
1���ܹ�˵����ˮ���������ʵ�� �� �� A.��ˮ���лӷ���
B.1mol��L-1��ˮ��Һ��pH=10 C. 1mol��L-1NH4Cl��Һ��pH=5 D.��ˮ��AlCl3��Һ��Ӧ����Al(OH)3
2��Ϊ��ʹ(NH4)2SO4��Һ��c(NH4)��c(SO4)֮�ȸ��ӽ���2��1��������Һ�еμ������� �� �� A. H2SO4 B.���� C.NaOH��Һ D.NaCl��Һ 3����֪���ʵ���Ũ����ͬ����������Һ:NaX,NaY,NaZ,���ǵ�PH����Ϊ:8,9,10,,���֪��Ӧ�������ǿ��˳��Ϊ�� ��
A.HX > HY> HZ B.HX > HZ > HY C. HY> HZ > HX D. HZ > HY > HX
4���������ʵ���Һ�������������������� �� �� A.Na2S B.Na3PO4 C.Na2CO3 D.AlCl3 5���������ƣ�Na2FeO4����δ���Ӻ��ĵ�ˮ�����dz�������ˮ������һ���¼��������ж�Na2FeO4��������ˮ���������ķ�����ȷ���� �� ��
+
2-
��Һ�������ж���ȷ���� �� ��
��ȫ��Ӧ����Ӧ�����Һ�У������ж���ȷ���ǣ� �� A.c(A-)��c(M+
) B.c(A-)��c(M+
)
C.��MA��ˮ�⣬��c(OH-)<c(H+
) D.��MAˮ�⣬��c(OH-)>c(H+
)
11����100������2Ħ/����NaOH��Һ��100������2Ħ/����H2SO4��Һ�Լ�һ�����İ�ˮ��ϣ����õ���Һʹ��̪��Һ��dz��ɫ������Һ������Ũ�ȹ�ϵ��ȷ���� ( ) A.[SO2-]=[Na+
]>[NH+
-+
4
4]>[OH]>[H] B.[Na+
]>[SO2-]>[NH+
-+
4
4]>[OH]>[H] C.[NH+]>[SO2-+
-+
4
4]=[Na]>[OH]>[H] D.[H+
]+[NH+]+[Na+
] = [OH-]+2[SO2-4
4]
12����һ��IA���������ʽ��AHB��H2B��Һ������ͬ�����£�AHB��Һ��HB-�ĵ���̶�С��HB-��ˮ��̶ȡ�����˵����ȷ���� ( ) A.AHB����Һ��������
B.�����£�ͬŨ�ȵ�AOH��H2B��Һ����ȶ�ǰ��С�ں��� C.���εĵ��뷽��ʽΪAHBA++H++B2-
D.��Һ�����ӵ�Ħ��Ũ�ȴ�С˳��Ϊ��
[A+
]>[HB-]>[OH-]>[H+]
13��ij�����ʽ��NaHY��ˮ��Һ�У�HY-�ĵ����С��HY-��ˮ��̶ȡ��й���������ȷ���ǣ� �� A.H2Y�ڵ���ʱΪ��H2Y+H2O
HY-+H3O+
B.�ڸ��ε���Һ�У�����Ũ��Ϊ�� c(Na+
)>c(Y2-)>c(HY-)>c(OH-)>c(H+
) C.�ڸ��ε���Һ�У�����Ũ��Ϊ�� c(Na+
)>c(HY-)>c(Y2-)>c(OH-)>c(H) D.HY-ˮ�ⷽ��ʽΪ��HY-+H
+
2-2O
Y+H3O+
14����֪PH=5��MgCl2��Һ�к�������FeCl3,Ϊ��ȥ���ʿɼ�����Լ��� �� �� A.MgO B.MgCO3 C.NaOH D.NaHCO
15�����ʵ���Ũ����ͬ�����и������ʵ���Һ�У���ָ�������ӵ�Ũ������С�Ƚϣ����д� ����� �� �� A.c��PO3-
4����Na3PO4��Na2HPO4��NaH2PO4��H3PO4 B.c��CO2-3����(NH4)2CO3��Na2CO3��NaHCO3��NH4HCO3 C.c��NH+4����(NH4)2SO4��(NH4)2CO3��NH4HSO4��NH4Cl D.c��S2-����Na2S��H2S��NaHS
16����ͬ�����²�â�NaHCO3 ��CH3COONa ��NaClO����ϡ
��Һ��pHֵ��ͬ,�����ǵ�Ħ��Ũ���ɴ�С�Ĺ�ϵ�� �� �� A.�٢ڢ� B.�ۢ٢� C.�ڢ٢� D.�ۢڢ� 17��FeCl3���������ʵķ�Ӧ,������ˮ���ص������� (1)��ɫʯ����Һ(2)�⻯��(3)��е�����ˮ(4)������(5)ƫ��������Һ(6)��������Һ(7)���軯��(8)ͭ��(9)С�մ���Һ �� �� A.(1)(2)(4)(6) B.(2)(4)(7)(8) C.(3)(5)(8)(9) D.(2)(4)(6)(8)
18��ij��Ԫ��H--
2A��ˮ�з�������: H2A = H+
+ HA��HA
H+
+ A2-, ���������в���ȷ����������: �� �� A. ��NaHA��Һ��: [Na+
] > [HA-] > [OH-] > [H+
] B. ��Na+
2--+
2A��Һ��: [Na] > [A] > [OH] > [H]
C. ��NaHA��Һ��: [Na+] > [H+] = [HA-] + 2[A2-] > [OH-
] D. ��H+
-2--
2A��Һ��: [H] = [HA] + 2[A] + [OH]
19��0.1mol/L Na2CO3��Һ�У��������������ʵ���Ũ���ɴ�С��˳��Ϊ��____>____>____�� 20��BiCl3ˮ������BiOCl��
��д��ˮ�ⷽ��ʽ �� ��ҽҩ�ϰ�BiOCl�����������顣��ͬ��������� ����ǡ������� ��
���������BiCl3��Һ�� �� �Ȱ���������BiCl3����ŨNaCl��Һ�пɵó���Һ����˵�����ܵ�ԭ�� ��
21�����е������Һ����Na2CO3��NaHCO3��NaAlO2��CH3COONa ��NaOH ����֪��CO2+3H2O+2AlO-2-2=2Al(OH)3��+CO3 �ٵ�������Һ��pH��ͬʱ�������ʵ���Ũ���ɴ�С��˳�� (����,��ͬ) �ڽ��������ʵ���Ũ�Ⱦ�Ϊ0.1mol/L��������Һ��ϡ����ͬ����ʱ����pH�仯������ �����������ֵ������Һ�У��ֱ����AlCl3��Һ��������������� �ܽ������٢ڢ������ֵ������Һ��ϣ�������Ӧ�����ӷ���ʽΪ 22����һԪǿ��MOH��Һ�м���һԪ��HA��Һ����ַ�Ӧ����Һ�����ԡ���ͬѧ��Ϊ��Һ��c(A-)=c(M+
)������ͬ
ѧ��Ϊc(A-)��c(M+
)�Ƿ���ȣ�Ҫ��һԪ��HA��ǿ�ỹ�����ᡣ����Ϊ_______ͬѧ��˵����ȷ��������__________________________________��
23.�ڳ��µ������£�Ϊ�˱�ʾ������ʵ����ǿ��������Һ���ѵ���ĵ���ʷ�����ռԭ���ܷ������İٷ�����������ȡ���ijpHֵ��������Һ��ˮ�ĵ����Ϊ��1����ͬpHֵ����������Һ��ˮ�ĵ����Ϊ��2�� ��ô��1�ͦ�2����ֵ��Ƚϣ���1
��2�����������������������
ij�����������������Һ��pHֵ����3����ô������ˮ�������c��H+
������������ˮ�����c��H+
����
����
����ijpHֵ��������ˮ�������c��H+����1.0��
10-amol/l������ͬpHֵ����������ˮ�������c��H+����1.0��10-b
mol/l��(a��b����С��14������)����ôa��b֮�� ����Ĺ�ϵʽ��
��
(��һ����ʽ��һ������ʽ��ʾ)��
24��Ũ����ͬ�����и�����ҺPHֵ��С�����˳���ǣ�
________ __��
��HNO3 ��H2SO4 ��H2CO3 ��KOH ��Ba(OH)2 ��Na2CO3 ��KNO3 ��AlCl3 ��CuCl2
25.��NaH2PO4��Һ�д��ڵ�ƽ���У������ӷ���ʽ��ʾ����____________________ _�� ���һʵ��˵��NaH2PO4�ĵ���̶ȱ�ˮ��̶ȴ�
_________________________ �� 26����Ԫ����(��дΪH2A)��Һ������ʽ����һ���Ͷ������룺H+
��
��
+
2��
2A=H+HA�� HA=H+A��֪��ͬŨ��ʱ�ĵ���Ȧ�(H2A)����(HA��)����������������Һ�� A.0.01 mol��L��1
��H2A��Һ B.0.01 mol��L��1��NaHA��Һ
C.0.02 mol��L��1
��HCl��0.04 mol��L��1
��NaHA��Һ��������Һ
D.0.02 mol��L��1
��NaOH��0.02 mol��L��1
��NaHA��Һ��������Һ
�ݴˣ���д���пհ�(�����)�� (1)c(H+
)������ , ������ �� (2)c(H2A)������ , ������ ��
(3)c(A2��)������ , ������ ��
��A����
��������
1��B D 2.A 3.C
2������Һǡ����ȫ��Ӧ��õ���������Һ�����ڼ����
��ˮ�⣬HCOO����Ũ�ȱ�Na+
��Ũ�ȱ�С����Һ�ʼ��ԣ���ӦѡA�� 3�� NaHSO4��ǿ�����ʽ�Σ����Բ�����ˮ�⡣������ζ�Ҫ�����ε�ˮ��
4������Ϊ��������ɫ�������Һ�ɫ��ȥ��
ԭ���ڴ�����Һ�У�CO2?
3��ˮ�⣬
������CO2?3?H2O?HCO?3?OH?����Һ�ʼ��ԣ������̪����Һ�ʺ�ɫ������BaCl2��Ba2??CO2?3?BaCO3? (��ɫ)������c(CO2?3)��С��ˮ��ƽ�����ƣ�c(OH��
)��С����̪��ɫ��
�»�����վ
1.C 2. C 3. A 4.C 5.C 6.D 7.B 8.B 9.C 10.A 11.AD 12.D 13
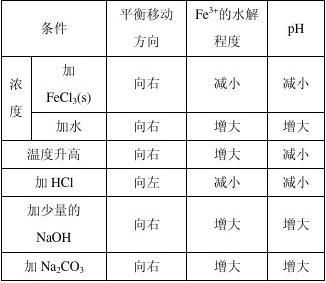

14��
��1�������� ������ 2c��Na+
��+c��H+
��=2c��CO2��
3��
��2��2c��Na+��=2c��CO2--
3��+2c��HCO3��+2H2CO3 ��3��c��OH-��=c��H+
��+c��HCO-
3��+2c��H2CO3�� 15��
��1��C ��2��CuCO3��CuO��Cu(OH)2��3��
Fe3??3H2OFe(OH)3?3H?
CuCO3?2HCl?CuCl2?CO2??H2O
��4������Ũ�������HCl������.
��16��ʱ ��B���� ����ѵ��
1��BD 2.B
������
1. BC 2.B 3. A 4.B 5.BC 6.C 7.D 8.B 9.D 10. BD 11. CD 12. D 13. A 14.AB 15. B 16.C 17.B 18.AC
19. c��CO2---
3�� c��OH�� c��HCO3��
20.��1��BiCl3?H2O?????
?BiOCl??2HCl ��2����ͬ�⣬��BiOCl��ClΪ-1�۶�����+1�� ��3����BiCl3�ܽ��ں�����HCl������ˮ�� ��4��������Һ��Cl-
Ũ�ȣ�������BiCl3��ˮ�� 21. (1)��>��>��>��>�� (2) �� (3) �ۢܢ�
��4��HCO??
3?AlO2?H2O?Al(OH)?3?CO23
22.��ͬѧ��ȷ�����ݵ���غ�ԭ����c��M+��+c��H+��=c��A-
��+c��OH-��������Һ�����ԣ���c��H+
��=c��OH-��������(M+
)=(A-
)��23. �� 10-8
a+b=14 b��7��a 24. �ڢ٢ۢ��ߢޢܢ� 25.
H???
2PO4?HPO2?2?
4��HPO3?
44?H
??
HPO2?
4?H22PO4?OH
H?2PO4?H2H3PO4?OH?��H2O
H??OH?
ȡNaH2PO4��Һ����
pH
��ֽ����Һ��pH����
pH?7��˵��H?2PO4�ĵ���̶ȴ�����ˮ��̶ȡ�
26��(1)A D (2) C D (3)D A
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
- �����ˮ��֪ʶ��(ѧ����)
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
-
�����ˮ��֪ʶ���ܽ�
�����ˮ��֪ʶ���ܽ�1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn���Ρ�
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һ�ε�ˮ��ʵ��H2OHOHnnn����AB��
-
��ѧѡ��4�����µ����ڡ������ˮ�⡷֪ʶ�ܽ�
��ѧѡ���ĵ����µ�3�ڡ������ˮ�⡷֪ʶ�ܽ�һ��̽������Һ�������ǿ�������ε�ˮ��Һ���ʼ��ԣ�ǿ�������ε�ˮ��Һ�������ԣ�ǿ��ǿ�
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
- ����ˮ��֪ʶ���ܽ�
-
�����ˮ��֪ʶ���ܽ�
1�����ˮ��1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn����AB�ܵ硭
-
�����ˮ��֪ʶ���ܽ�
�����ˮ��֪ʶ���ܽ�1��ϰ�ص�1�����ˮ��ԭ������Ӧ��2��Һ����������ϵ���غ�ԭ��2�ѵ�۽�һH2OH�ε�ˮ��ʵ��nnn���Ρ�