盐类水解的规律实验
盐类水解规律的探究
编写:李锋志 时间:20XX.4.18
实验目的:
1、认识盐类水解的原理、盐类水解的规律。
2、认识外界条件对盐类水解的影响。
实验方法
实验探究、小组合作、讨论、归纳的方法。
仪器、用品
pH试纸、比色卡、玻璃棒、表面皿、酒精灯、石棉网等
药品:NaCl、KNO3\CH3COONa、NH4Cl、Al2(SO4)3、Na2CO3(均为溶液)。
实验过程及步骤
(一)盐类水解规律的探究
1、选择合适的方法测出以下盐溶液的酸碱性。(分组实验)
2、根据形成该盐的酸和碱的强弱,将下表中盐按强酸弱碱盐、强碱弱酸盐、强酸强碱盐分类。
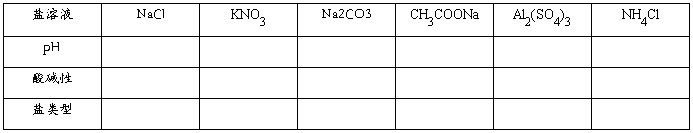
3、分析上述实验结果,归纳其与盐类型间的关系,并从电离平衡的角度寻找原因。
4、25℃,浓度均为0.1mol/L的几种盐溶液 ,用pH计精确测定其溶液的pH,
【思考与交流】
(1)盐溶液中存在哪些粒子?
(2)哪些粒子间可能结合?
(3)对水的电离平衡有何影响?
(4)相关的电离方程式、化学方程式?
第一小组以NH4Cl溶液为例,讨论:为什么强酸弱碱盐显酸性?选择一名中心发言人宣读讨论结果。其他组员补充。
第二小组以CH3COONa为例,讨论:为什么强碱弱酸盐显碱性?选择一名中心发言人宣读讨论结果。其他组员补充。
第三小组以NaCl为例,讨论:为什么强碱强酸盐显中性?选择一名中心发言人宣读讨论结果。其他组员补充。
【规律总结】1、盐类水解的定义
2、盐类水解反应的实质
3、水解方程式的表示方法:
① 先找“弱”
② 由于水解程度小,水解产物少。一般书写可逆符号,不写“ = ”、“↑”、“↓”,也不把生成物(如NH3·H2O、H2CO3)写成分解产物的形式
③多元弱酸盐分步水解,但以第一步水解为主,故只写第一步即可;多元弱碱盐也是分步水解,但不分步书写。
4、盐类水解的规律
无______不水解;有_____才水解
谁______谁水解;谁_____显谁性
越______越水解。
盐类水解与酸碱中和反应的关系:盐+水_____酸+碱
(二)外界条件对盐类水解的影响
1、第一小组
取少量NaCl溶液加热后测pH的变化情况。
再取少量NaCl溶液稀释大约10倍后测pH的变化情况。
2、第二小组
取少量KNO3溶液加热后测pH的变化情况。
再取少量KNO3溶液稀释大约10倍后测pH的变化情况。
3、第三小组
取少量Na2CO3溶液加热后测pH的变化情况。
再取少量Na2CO3溶液稀释大约10倍后测pH的变化情况。
4、第四小组
取少量CH3COONa溶液加热后测pH的变化情况。
再取少量CH3COONa溶液稀释大约10倍后测pH的变化情况。
5、第五小组
取少量Al2(SO4)3溶液加热后测pH的变化情况。
再取少量Al2(SO4)3溶液稀释大约10倍后测pH的变化情况。
6、第六小组
取少量NH4Cl溶液加热后测pH的变化情况。
再取少量NH4Cl溶液稀释大约10倍后测pH的变化情况。
【规律总结】
升高温度盐类水解的程度__________,升高温度盐类水解的程度__________,
稀释溶液盐类水解的程度__________,稀释溶液盐类水解的程度__________.
课后交流探讨
1:书写下列物质水解的方程式:
NaF、Na2SO3、(NH4)2SO4、CuCl2
2、书写相关物质水解的方程式
3、向水中加入下列相应物质,试填表:
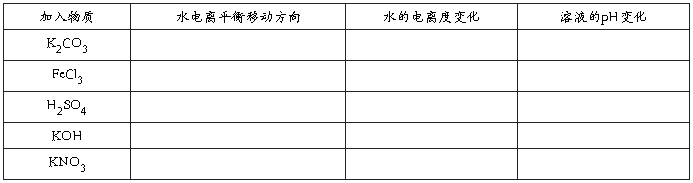
第六部分 课后小记

第七部分 教学设计

第二篇:盐类水解的实质与规律练习题及答案
盐类水解的实质与规律练习题及答案
20##-07-12
[基础过关]
一、盐类水解的概念
1. 在盐类水解的过程中,下列说法正确的是 ( )
A.盐的电离平衡被破坏
B.水的电离程度一定会增大
C.溶液的pH一定会增大
D.c(H+)与c(OH-)的乘积一定会增大
2. 下列物质的水溶液中,除了水分子外,不存在其他分子的是 ( )
A.HCl B.NH4NO3 C.Na2S D.HClO
3. 下列各物质的溶液显酸性的是 ( )
A.NaHCO3 B.(NH4)2SO4
C.NaCl D.CH3COOK
4. 下列操作会促进H2O的电离,且使溶液pH>7的是 ( )
A.将纯水加热到90 ℃
B.向水中加少量NaOH溶液
C.向水中加少量Na2CO3溶液
D.向水中加少量FeCl3溶液
5. 实验室有下列试剂,其中必须用带橡胶塞的试剂瓶保存的是 ( )
①NaOH溶液 ②水玻璃 ③Na2S溶液 ④Na2CO3溶液
⑤NH4Cl溶液 ⑥澄清石灰水 ⑦浓HNO3
⑧浓H2SO4
A.①⑥ B.①②③④⑥
C.①②③⑥⑦⑧ D.⑤⑦⑧
二、盐类水解离子方程式的书写
6. 下列物质在常温下发生水解时,对应的离子方程式正确的是 ( )
①Na2CO3:CO2-3+2H2O H2O+CO2↑+2OH-
②NH4Cl:NH+4+H2O NH3·H2O+H+
③CuSO4:Cu2++2H2O Cu(OH)2+2H+
④NaF:F-+H2O===HF+OH-
A.①④ B.②③ C.①③ D.②④
7. 下列各项中的离子方程式,书写正确的是 ( )
A.AlCl3水解:Al3++3H2O===Al(OH)3+3H+
B.NaHCO3电离:NaHCO3 Na++HCO-3
C.固体Ca(OH)2与NH4Cl共热:NH+4+OH-===NH3+H2O
D.过量的CO2气体通入饱和石灰水中:CO2+OH-===HCO-3
三、盐类水解规律的综合应用
8. 下列各组溶液混合后,溶液显碱性的是 ( )
A.10 mL 0.1 mol·L-1 NH3·H2O与10 mL 0.1 mol·L-1 HCl
B.10 mL 0.1 mol·L-1 K2S与10 mL 0.1 mol·L-1 K2SO4
C.10 mL 0.1 mol·L-1 KOH与10 mL 0.1 mol·L-1 KHCO3,再加入10 mL 0.1 mol·L-1 BaCl2
D.10 mL 0.1 mol·L-1 NaOH与5 mL 0.1 mol·L-1 H2SO4
9. 等物质的量浓度的下列五种溶液:①CH3COOH
②(NH4)2CO3 ③NaHSO4 ④NaHCO3 ⑤Ba(OH)2,溶液中水的电离程度由大到小排列正确的是 ( )
A.⑤③①④② B.⑤③①②④
C.②④③①⑤ D.②④①③⑤
10.有四种物质的量浓度相等且都由一价阳离子A+和B+及一价阴离子X-和Y-组成的盐溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7,由此判断不水解的盐是 ( )
A.BX B.AX C.AY D.BY
[能力提升]
11.(1)某二元酸(化学式用H2A表示)在水中的电离方程式是H2A===H++HA- HA- H++A2-
试完成下列问题:
Na2A溶液显 (填“酸性”、“中性”或“碱性”)。理由是
(用离子方程式表示)。
(2)pH=5的NH4Cl溶液与pH=5的HCl溶液中由水电离出的c(H+)分别是 、 。
12.室温下,pH=2的某酸HnA(A为酸根)与pH=12的某碱B(OH)m等体积混合,混合液的pH变为8。
(1)写出生成的正盐的分子式: 。
(2)该盐中存在着一种水解的离子,该离子的水解方程式为 。
(3)简述该混合液呈碱性的原因:
。
13.常温下,如果取0.1 mol·L-1 HA溶液与0.1 mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因(用离子方程式表示):
。
(2)混合溶液中由水电离出的c(H+) (填“>”、“<”或“=”)0.1 mol·L-1 NaOH溶液中由水电离出的c(H+)。
(3)已知NH4A溶液为中性,HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH 7(填“>”、“<”或“=”)。
[拓展探究]
14.某实验小组拟定用pH试纸验证醋酸是弱酸。甲、乙两同学的方案分别是
甲:①准确配制0.1 mol·L-1的醋酸钠溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明醋酸是弱酸。
乙:①量取一定量的冰醋酸准确配制pH=1的醋酸溶液100 mL;
②取醋酸溶液1 mL,加水稀释为10 mL;
③用pH试纸测出②中溶液的pH,即可证明醋酸是弱酸。
(1)两个方案的第①步中,都要用到的定量仪器是 ,
简要说明pH试纸的使用方法:
。
(2)甲方案中,说明醋酸是弱酸的理由是测得醋酸钠溶液的pH 7(选填“<”、“>”或“=”,下同),乙方案中,说明醋酸是弱酸的理由是测得醋酸溶液的pH 2。
(3)请你评价乙方案的不妥之处: _。
答案
1.B 2.A 3.B 4.C 5.B 6.B 7.D 8.B 9.D 10.B
11.(1)碱性 A2-+H2O HA-+OH-
(2)10-5 mol·L-1 10-9 mol·L-1
12.(1)BnAm(或BAmn)
(2)Bm++mH2O B(OH)m+mH+
(3)酸与碱等体积反应,碱过量,则最后混合液中溶质是正盐BnAm与碱B(OH)m的混合物,呈碱性
13.(1)A-+H2O HA+OH- (2)> (3)>
14.(1)100 mL容量瓶 把小块pH试纸放在表面皿上,用洁净的玻璃棒蘸取待测液点在试纸中部,试纸变色后,与标准比色卡比较来确定溶液的pH
(2)> <
(3)难以配制pH=1的醋酸溶液,稀释之后用pH试纸测量不易读出准确数值
-
盐类水解规律总结
盐类水解规律总结盐溶液中的离子跟水所电离出来的H或OH结合生成弱电解质的反应叫做盐类的水解其实质是水解反应破坏了水的电离平衡改变了…
-
盐类水解规律总结 学生练习
规律总结1必须有正确的思路2掌握解此类题的三个思维基点电离水解和守恒3分清他们的主要地位和次要地位常见题型一溶质单一型关注三个守恒…
-
总结水解规律
总结水解规律:谁弱谁水解,都弱双水解,谁强显谁性,同强显中性,越弱越水解,越热越水解,越稀越水解.水解的相互促进——双水解互相促进…
-
盐类的水解知识点总结
1盐类的水解1复习重点1盐类的水解原理及其应用2溶液中微粒间的相互关系及守恒原理2难点聚焦一H2OH盐的水解实质nnn当盐AB能电…
-
盐类的水解规律(教案)
教学目标盐类的水解规律教案1使学生理解盐类水解的实质能解释强碱弱酸盐和强酸弱碱盐的水解2能通过比较分类归纳概括等方法得出盐类水解的…
-
总结水解规律
总结水解规律:谁弱谁水解,都弱双水解,谁强显谁性,同强显中性,越弱越水解,越热越水解,越稀越水解.水解的相互促进——双水解互相促进…
-
盐类的水解知识点总结
1盐类的水解1复习重点1盐类的水解原理及其应用2溶液中微粒间的相互关系及守恒原理2难点聚焦一H2OH盐的水解实质nnn当盐AB能电…
-
盐类水解知识点总结
盐类水解基础知识点在溶液中盐的离子跟水所电离出来的H或OH生成弱电解质的过程叫做盐类的水解盐类的水解所条件盐必须溶于水盐必须能电离…
-
盐类的水解知识点总结
盐类水解的应用考点1判断或解释盐溶液的酸碱性例如正盐KXKYKZ的溶液物质的量浓度相同其pH值分别为789则HXHYHZ的酸性强弱…
-
盐类水解规律总结
盐类水解规律总结盐溶液中的离子跟水所电离出来的H或OH结合生成弱电解质的反应叫做盐类的水解其实质是水解反应破坏了水的电离平衡改变了…