预习报告 苯甲酸和萘的分离与提纯
预习报告 苯甲酸和萘的分离与提纯
一、实验目的
1.了解苯甲酸和萘的基本性质
2.掌握固体有机混合物的分离原理及方法
3.复习萃取、蒸馏及重结晶等纯化技术
二、实验基本原理(或主、副反应式)
苯甲酸和萘在常温下均为白色固体有机物,并且均不溶于水而易溶于醇、醚等有机溶剂。所以不能根据两物质在不同溶剂中溶解度不同来达到分离的目的。
但是,苯甲酸可以和氢氧化钠作用得到苯甲酸钠,而苯甲酸钠易溶于水。可将混合物溶于乙醚后加入氢氧化钠水溶液萃取并洗涤,乙醚层经洗涤、干燥、蒸馏得到萘;水层经酸化、减压过滤得到苯甲酸。从而达到分离的目的。
反应方程式:
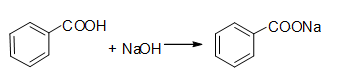
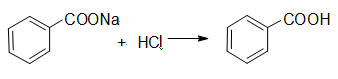
四、主要试剂及主、副产物的物理常数

五、主要试剂规格及用量

六、实验操作步骤
称取2g苯甲酸和萘的混合物于100mL锥形瓶中,加入20mL乙醚使之充分溶解。
将以上溶液转移至分液漏斗中,每次加入10mL 5%NaOH水溶液洗涤三次。水层从分液漏斗活塞放出,乙醚层从分液漏斗上口倒出。
乙醚层中加入无水氯化钙干燥30min左右,过滤。将所得滤液转移至蒸馏瓶中,水浴加热蒸馏,收集34~38℃馏分(乙醚),剩余液体(萘)倒在表面皿上。乙醚测量体积,回收。待表面皿上的液体结晶后即为纯净的萘,收集固体,称量。
水层加入浓盐酸酸化至溶液呈明显酸性为止,充分冷却,待晶体全部析出后,抽滤,所得晶体即为苯甲酸。干燥,称量。
实验步骤流程图

七、实验注意事项
1.用氢氧化钠萃取时震摇使两相充分接触,继而使苯甲酸反应完全
2.用分液漏斗分液时,水层从活塞放出,乙醚层从上口倒出,否则会影响后面的操作。注意提取过的水层要保存好,供下步制苯甲酸用
3. 乙醚层用无水氯化钙干燥时,震摇后要静置片刻至澄清;并充分静置干燥约30min。干燥后的乙醚层慢慢滤入干燥的蒸馏烧瓶中。
4.蒸馏不能蒸干,留小部分乙醚以防萘在蒸馏瓶中结晶,无法收集。乙醚蒸完后立即回收。
5.水层如果酸化不完全,会使苯甲酸不能充分析出,导致产物损失,酸化程度为能使pH试纸变红即可。
首先利用萃取的原理:苯甲醇和苯甲酸钠在乙醚中的溶解度不同,以乙醚为萃取剂,将苯甲醇萃取至乙醚层中,从而使两者分离。再分别处理醚层和水层,利用蒸馏和重结晶,分离得到较纯净的两种产物。
应该酸性至比较强一点的酸性,即盐酸过量一点。
可以不用测PH值,取水层,加酸,不再出现混浊,就差不多了。如果不放心,可以再多少加一点点。
第二篇:第十三周化学实验报告苯甲酸的提纯和测定
华南农业大学实验报告
专业班次 11农学一班 组别* *
题目 苯甲酸的提纯和测定
姓 名 **
日期
【实验目的】
1、 了解固体有机物的分离和提纯方法;
2、 掌握回流,重结晶,测熔点的操作。
【实验原理】
重结晶:固体物质在溶剂中的溶解度随温度升高而增大,如果把固体物质溶解在热的溶剂中制成饱和或接近饱和的溶液,然后冷却至室温或室温以下,则溶解度下降,溶液过饱和,这时就会有晶体析出;
熔点测定原理:熔点是晶体物质的固相和液相在正常大气压下成平衡的温度,纯净的固态有机化合物都有固定的熔点,而且一般不高,用简单的一起就可以测定,有机化合物的熔点通常用毛细管发测定,纯净的有机化合物固液两相之间的变化非常敏锐,熔点范围很少,当含有杂质的时候,会使熔点变小,并且熔点范围增大。
【实验步骤】
1、 将粗苯甲酸用热水进行重结晶,烘干产品得到纯苯甲酸,
2、 测定产率,
3、 测定苯甲酸的熔点: 去一直径为1-2mm,长度7-8cm的毛细管,将其一端放在火焰上烧融,使之封闭,将少许的苯甲酸放在洁净的表面皿上,用玻璃棒研成粉末并束成一堆,然后将熔点管的开口端插入到试样中,装取试样后,将端口向上,把熔点管竖起来,在台面上轻顿几下,再取30~40cm的干燥玻璃管,垂直于台面上,让熔点管自由下落,重复几次,使试样落到管的底部,并且结实均匀,
去一直径为1-2mm,长度7-8cm的毛细管,将其一端放在火焰上烧融,使之封闭,将少许的苯甲酸放在洁净的表面皿上,用玻璃棒研成粉末并束成一堆,然后将熔点管的开口端插入到试样中,装取试样后,将端口向上,把熔点管竖起来,在台面上轻顿几下,再取30~40cm的干燥玻璃管,垂直于台面上,让熔点管自由下落,重复几次,使试样落到管的底部,并且结实均匀,
4、 加热,每分钟升温5到6摄氏度,熔点前二十摄氏度前减为每分钟0.3到0.5摄氏度,当试样开始出现塌落,湿润出现小液滴,表示开始融化,记录温度,完全融化后再记录一次温度。
【实验数据记录】
苯甲酸粗产品的质量为1.56-0.7=0.86g,纯产量为0.62,产率为75.6%
熔点测定
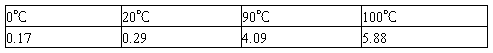

【讨论】
-
苯甲酸重结晶实验报告
苯甲酸的重结晶实验目的了解重结晶提纯粗苯甲酸的原理和方法实验原理苯甲酸在水中的溶解度随温度的变化较大通过重结晶可以使它与杂质分离从…
-
苯甲酸重结晶实验报告作业
实验二苯甲酸的重结晶及测熔点10级班1一实验目的1了解重结晶原理初步学会用重结晶方法提纯固体有机化合物2掌握热过滤和抽滤操作二基本…
- 化学实验报告 粗苯甲酸提纯
-
有机化学实验报告 苯甲酸的重结晶
苯甲酸的重结晶一、实验目的:1、了解重结晶原理,初步学会用重结晶方法提纯固体有机化合物;2、掌握热过滤和抽滤操作。二、基本原理:1…
-
苯甲酸和萘的分离预习实验报告
考核实验项目名称苯甲酸和萘的分离一实验设计基本原理苯甲酸和萘在常温下均为白色固体有机物并且均不溶于水而易溶于醇醚等有机溶剂所以不能…
-
有机化学实验报告 苯甲酸的重结晶
苯甲酸的重结晶一、实验目的:1、了解重结晶原理,初步学会用重结晶方法提纯固体有机化合物;2、掌握热过滤和抽滤操作。二、基本原理:1…
-
苯甲酸重结晶实验报告
苯甲酸的重结晶实验目的了解重结晶提纯粗苯甲酸的原理和方法实验原理苯甲酸在水中的溶解度随温度的变化较大通过重结晶可以使它与杂质分离从…
-
苯甲酸重结晶实验报告作业
实验二苯甲酸的重结晶及测熔点10级班1一实验目的1了解重结晶原理初步学会用重结晶方法提纯固体有机化合物2掌握热过滤和抽滤操作二基本…
- 化学实验报告 粗苯甲酸提纯
-
分析实验报告 红外光谱测定苯甲酸 - 最终版
华南师范大学实验报告学号专业年级班级实验时间实验指导老师郭长娟老师实验评分红外光谱法测定苯甲酸一实验目的1了解苯甲酸的红外光谱特征…