篇一 :第十三周化学实验报告苯甲酸的提纯和测定
华南农业大学实验报告
专业班次 11农学一班 组别* *
题目 苯甲酸的提纯和测定
姓 名 **
日期
【实验目的】
1、 了解固体有机物的分离和提纯方法;
2、 掌握回流,重结晶,测熔点的操作。
【实验原理】
重结晶:固体物质在溶剂中的溶解度随温度升高而增大,如果把固体物质溶解在热的溶剂中制成饱和或接近饱和的溶液,然后冷却至室温或室温以下,则溶解度下降,溶液过饱和,这时就会有晶体析出;
熔点测定原理:熔点是晶体物质的固相和液相在正常大气压下成平衡的温度,纯净的固态有机化合物都有固定的熔点,而且一般不高,用简单的一起就可以测定,有机化合物的熔点通常用毛细管发测定,纯净的有机化合物固液两相之间的变化非常敏锐,熔点范围很少,当含有杂质的时候,会使熔点变小,并且熔点范围增大。
【实验步骤】
1、 将粗苯甲酸用热水进行重结晶,烘干产品得到纯苯甲酸,
2、 测定产率,
3、 测定苯甲酸的熔点: 去一直径为1-2mm,长度7-8cm的毛细管,将其一端放在火焰上烧融,使之封闭,将少许的苯甲酸放在洁净的表面皿上,用玻璃棒研成粉末并束成一堆,然后将熔点管的开口端插入到试样中,装取试样后,将端口向上,把熔点管竖起来,在台面上轻顿几下,再取30~40cm的干燥玻璃管,垂直于台面上,让熔点管自由下落,重复几次,使试样落到管的底部,并且结实均匀,
去一直径为1-2mm,长度7-8cm的毛细管,将其一端放在火焰上烧融,使之封闭,将少许的苯甲酸放在洁净的表面皿上,用玻璃棒研成粉末并束成一堆,然后将熔点管的开口端插入到试样中,装取试样后,将端口向上,把熔点管竖起来,在台面上轻顿几下,再取30~40cm的干燥玻璃管,垂直于台面上,让熔点管自由下落,重复几次,使试样落到管的底部,并且结实均匀,
…… …… 余下全文
篇二 :苯甲酸重结晶实验报告
苯甲酸的重结晶
实验目的:了解重结晶提纯粗苯甲酸的原理和方法。
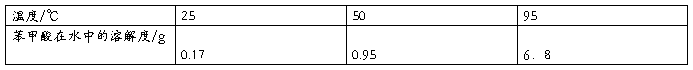
实验原理:苯甲酸在水中的溶解度随温度的变化较大,通过重结晶可以使它与杂质分离,从而达到分离提纯的目的。
实验试剂:粗苯甲酸(本实验中的药品混有氯化钠和少量泥沙)、AgNO3溶液、蒸馏水
实验仪器、用品:烧杯、铁架台(带铁圈)、酒精灯、普通漏斗、玻璃棒、坩埚钳、滤纸、石棉网、药匙、三脚架、试管、胶头滴管、火柴。
实验步骤:
一、热溶解
①取约0.5g粗苯甲酸晶体置于100mL烧杯中,加入50mL蒸馏水。
②在三脚架上垫一石棉网,将烧杯放在石棉网上,点燃酒精灯加热,不时用玻璃棒搅拌(注意:搅拌时玻璃棒不要触及烧杯内壁)。
③待粗苯甲酸全部溶解,停止加热。
二、热过滤
①将准备好的过滤器放在铁架台的铁圈上,过滤器下放一小烧杯。
②将烧杯中的混合液趁热过滤。(过滤时可用坩埚钳夹住烧杯,避免烫手),使滤液沿玻璃棒缓缓注入过滤器中。
三、冷却结晶
将滤液静置冷却,观察烧杯中晶体的析出。(在静置冷却的同时,再准备好一个过滤器)。
四、过滤洗涤
①将析出苯甲酸晶体的混合液过滤,滤纸上为苯甲酸晶体。
②取2mL滤液于一支试管中,检验其中的氯离子。
…… …… 余下全文
篇三 :苯甲酸重结晶实验报告作业
实验二 苯甲酸的重结晶及测熔点
——10级 班 1
一、实验目的:
1、了解重结晶原理,初步学会用重结晶方法提纯固体有机化合物;
2、 掌握热过滤和抽滤操作。
二、基本原理:
1、重结晶的原理是利用固体混合物中各组分在某种溶剂中的溶解度不同,使它们相互分离,达到提纯精制的目的(把固体有机物溶解在热的溶剂中使之饱和,冷却时由于溶解度降低,有机物又重新析出晶体。——利用溶剂对被提纯物质及杂质的溶解度不同,使被提纯物质从过饱和溶液中析出。让杂质全部或大部分留在溶液中,从而达到提纯的目的)。
注意——重结晶只适宜杂质含量在5%以下的固体有机混合物的提纯。从反应粗产物直接重结晶是不适宜的,必须先采取其他方法初步提纯,然后再重结晶提纯。
2、溶剂的选择:
1)被提纯物质,高温下溶解度大,低温下溶解度小。
2)与被提纯的物质不发生化学反应。
3)杂质溶解度要么非常大要么非常小。
…… …… 余下全文
篇四 :化学实验报告 粗苯甲酸提纯
粗 苯 甲 酸 提 纯
[实验原理]
粗苯甲酸为同时混有难溶性和可溶性杂质的固体苯甲酸。实验目的在于依据苯甲酸和杂质在水中溶解度的差别使之分离并获得纯净的苯甲酸晶体。采用两次分离操作。难溶性杂质的分离采用加热后过滤分离法方案,易溶性杂质(如硫酸钾、氯化钠等)的分离则采用重结晶分离法方案来完成。结晶法分离基于在同一温度下,溶液中所含物质到达饱和浓度的先后次序的不同,因为溶液中苯甲酸的量远大于其他杂质,并且其溶解度在某一温度远低于其他可溶性物质,降温后就先得到苯甲酸晶体,其它可溶性的杂质留在母液中,再通过过滤将它们分离出来。
[实验目标]
1. 通过“粗苯甲酸提纯”,学会熟练利用重结晶法从混合物中分离出某纯净物的方法,体会通过观察以及一些物理或化学方法区别混合物和纯净物。
2.熟悉溶解、加热、过滤和降温结晶等基本操作。
[实验用品]
烧杯、玻璃棒、量筒(20mL)、手套、漏斗、铁架台(带铁圈)、石棉网、酒精灯、托盘天平、砝码、药匙;
粗苯甲酸、蒸馏水、Ba(NO3)2溶液、AgNO3溶液、稀硝酸。
[实验步骤]
1.溶解
用量筒量取50mL水倒入烧杯里。用托盘天平称量1g粗苯甲酸加入水中。把石棉网垫在铁架台的铁圈上,然后将烧杯置于石棉网上。用酒精灯给烧杯加热,边加热边用玻璃棒搅拌。用玻璃棒搅拌至水沸腾且苯甲酸全部溶解为止,观察此时溶液是否浑浊。
…… …… 余下全文
篇五 :有机化学实验报告 苯甲酸的重结晶
苯甲酸的重结晶
一、实验目的:
1、了解重结晶原理,初步学会用重结晶方法提纯固体有机化合物;
2、 掌握热过滤和抽滤操作。
二、基本原理:
1、重结晶的原理是利用固体混合物中各组分在某种溶剂中的溶解度不同,使它们相互分离,达到提纯精制的目的(把固体有机物溶解在热的溶剂中使之饱和,冷却时由于溶解度降低,有机物又重新析出晶体。——利用溶剂对被提纯物质及杂质的溶解度不同,使被提纯物质从过饱和溶液中析出。让杂质全部或大部分留在溶液中,从而达到提纯的目的)。
注意:重结晶只适宜杂质含量在5%以下的固体有机混合物的提纯。从反应粗产物直接重结晶是不适宜的,必须先采取其他方法初步提纯,然后再重结晶提纯。
2、溶剂的选择:
1)被提纯物质,高温下溶解度大,低温下溶解度小。
2)与被提纯的物质不发生化学反应。
3)杂质溶解度要么非常大要么非常小。
4)溶剂易挥发。(相对被提纯物质)
5)能形成较好的晶体。
6)无毒无害,价廉易得。
三、实验试剂与仪器:
药品:苯甲酸、活性炭。
仪器:烧杯、玻璃棒、吸滤瓶、布氏漏斗、滤纸、加热器。
四、实验步骤:
…… …… 余下全文
篇六 :苯甲酸和萘的分离预习实验报告
考核实验项目名称:苯甲酸和萘的分离
一、 实验设计基本原理
苯甲酸和萘在常温下均为白色固体有机物,并且均不溶于水而易溶于醇、醚等有机溶剂。所以不能根据两物质在不同溶剂中溶解度不同来达到分离的目的。 但是,苯甲酸可以和氢氧化钠作用得到苯甲酸钠,而苯甲酸钠易溶于水。可将混合物溶于乙醚后加入氢氧化钠水溶液萃取并洗涤,乙醚层经洗涤、干燥、蒸馏得到萘;水层经酸化、减压过滤得到苯甲酸。从而达到分离的目的。
C6H5COOH + NaOH → C6H5COONa
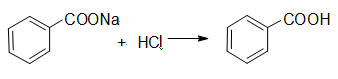
C6H5COONa +HCl →C6H5COOH
1、萃取原理:萃取是利用物质在两种不互溶(或微溶)溶剂中溶解度或分配比的不同来达到分离、提取或纯化的一种操作。
2、蒸馏原理:当液体被加热至沸腾,是液体变为蒸气,然后是蒸气冷却再凝结为液体,这两个过程的联合即为蒸馏。蒸馏可将易挥发的物质分离开来,也可将沸点不同的液体混合物(各组分的沸点必须相差至少30度以上)分离开来。
…… …… 余下全文
篇七 :苯甲酸和萘的分离实验报告
苯甲酸和萘的分离实验报告
一、实验目的
1.了解苯甲酸和萘的基本性质
2.掌握固体有机混合物的分离原理及方法
3.复习萃取、蒸馏及重结晶等纯化技术
二、实验基本原理
苯甲酸和萘在常温下均为白色固体有机物,并且均不溶于水而易溶于醇、醚
等有机溶剂。所以不能根据两物质在不同溶剂中溶解度不同来达到分离的目的。
但是,苯甲酸可以和氢氧化钠作用得到苯甲酸钠,而苯甲酸钠易溶于水。可
将混合物溶于乙醚后加入氢氧化钠水溶液萃取并洗涤,乙醚层经洗涤、干燥、蒸
馏得到萘;水层经酸化、减压过滤得到苯甲酸。从而达到分离的目的。
反应方程式:
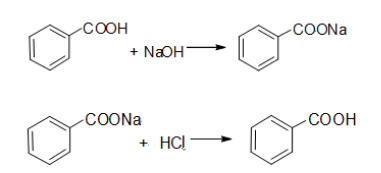
三、主要试剂及主、副产物的物理常数
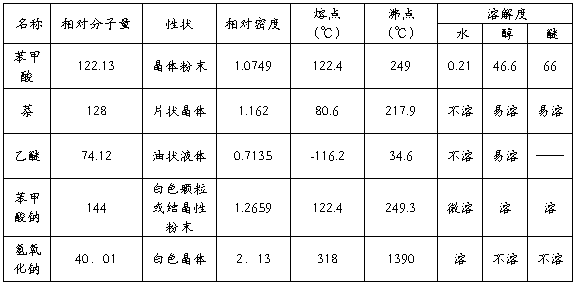
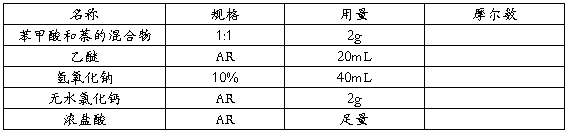
四、主要试剂规格及用量
五、实验装置图
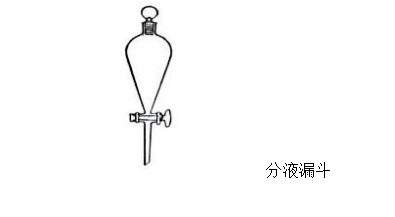

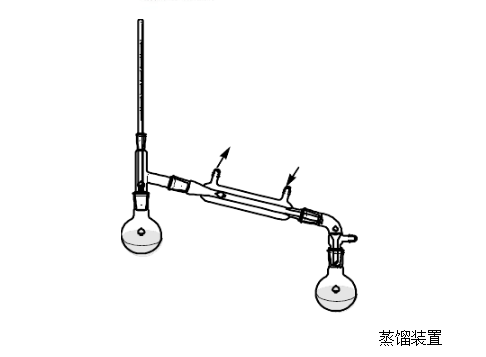
六、实验操作步骤
1、称取2g苯甲酸和萘的混合物于100mL锥形瓶中,加入20mL乙醚使之
充分溶解。
2、把混合物的乙醚溶液倒入分液漏斗中,然后量取20ml 10%氢氧化钠溶
…… …… 余下全文
篇八 :预习报告 苯甲酸和萘的分离与提纯
预习报告 苯甲酸和萘的分离与提纯
一、实验目的
1.了解苯甲酸和萘的基本性质
2.掌握固体有机混合物的分离原理及方法
3.复习萃取、蒸馏及重结晶等纯化技术
二、实验基本原理(或主、副反应式)
苯甲酸和萘在常温下均为白色固体有机物,并且均不溶于水而易溶于醇、醚等有机溶剂。所以不能根据两物质在不同溶剂中溶解度不同来达到分离的目的。
但是,苯甲酸可以和氢氧化钠作用得到苯甲酸钠,而苯甲酸钠易溶于水。可将混合物溶于乙醚后加入氢氧化钠水溶液萃取并洗涤,乙醚层经洗涤、干燥、蒸馏得到萘;水层经酸化、减压过滤得到苯甲酸。从而达到分离的目的。
反应方程式:
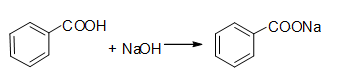
四、主要试剂及主、副产物的物理常数

五、主要试剂规格及用量

六、实验操作步骤
称取2g苯甲酸和萘的混合物于100mL锥形瓶中,加入20mL乙醚使之充分溶解。
将以上溶液转移至分液漏斗中,每次加入10mL 5%NaOH水溶液洗涤三次。水层从分液漏斗活塞放出,乙醚层从分液漏斗上口倒出。
…… …… 余下全文